Материал: Хромосомы эукариот
Теломеры - концевые
структуры линейных хромосом, состоящие из повторяющихся последовательностей
ДНК. У человека теломерные участки хромосом образованы тысячами повторов
последовательности TTAGGG. Среди растений наиболее часто в
теломерах повторяется последовательность TTTAGGG. Известно,
что растения семейства луковичных имеют иные теломерные последовательности.
Теломерные последовательности у Sacharomyces cerevisia
представляют собой вариабельные повторы TG. У дрожжей
теломера находится в ненуклеосомном хроматине, защищённом от действия нуклеаз,
и называется телосомой.
Рисунок 10. Теломеры хромосомы
Теломерные районы хромосом имеют общие с гетерохроматином свойства, в том числе: наличие высокоповторяющихся последовательностей, способность образовывать ассоциаты, инактивация генов, попавших в зону гетерохроматина или теломерного хроматина.
Теломеры хромосом собраны в несколько кластеров, которые располагаются по периферии ядра. Предполагают, что теломерные последовательности заякориваются на ядерной оболочке с помощью ДНК-белковых взаимодействий. Кроме того, теломеры взаимодействуют друг с другом. При этом плечи хромосом никогда не переплетаются. Ещё в 30-е годы Барбара Мак-Клинток показала, что теломеры защищают хромосомы от деградации и препятствуют слипанию хромосом.
Сейчас известно, что в результате «концевой недорепликации» в 3-нити молекулы ДНК образуется одноцепочечный конец, который специфическим образом сворачивается и взаимодействует с двунитевым районом теломеры, образую Т-петлю. Т-петля стабилизируется белковыми факторами. Этот процесс обеспечивает защиту молекулы ДНК от экзонуклеаз и называется кэппингом. Нарушение кэппинга может приводить к теломерным слияниям плеч хромосом. Нарушение кэппинга теломер распознается как разрыв, который должен репарироваться. Это приводит к теломера-теломерному слипанию хромосом с образованием дицентриков.
Специфические элементы теломер необходимы для расхождения сестринских хроматид в митозе. На Tetrachymena показано, что введение мутации в последовательность теломерного повтора блокирует расхождение хроматид в анафазе митоза. Предполагают, что теломеры сестринских хроматид соединены друг с другом на протяжении G2 - фазы клеточного цикла и в митозе до метафазы включительно. Ассоциаты теломер создаются с помощью теломерсвязывающих белков. В норме ассоциаты теломер должны распадаться перед расхождением хроматид в анафазе. Возможно, что при мутации в теломерной ДНК изменяется узнавание теломерного комплекса топоизомеразой 2. Этот фермент необходим для разделения хромосом в анафазе.
У дрожжей выделен мейоз - специфический, теломерсвязывающий белок NDS1/TAM1. Мутация гена данного белка приводит к тому, что каждая теломера оказывается неспаренной, в первом делении мейоза возрастает число случаев нерасхождения и преждевременного разделения сестринских хроматид.
Теломеры необходимы для начала
репликации ДНК: к ним прикрепляется РНК-затравка, с которой на каждой из нитей
двойной спирали ДНК начинается синтез нити, комплементарной первой. После
каждого деления клетки часть концевых нуклеотидов на каждой из вновь
образованных хромосом безвозвратно теряется вместе с РНК-затравкой. При каждом
цикле репликации дочерняя цепь ДНК теряет часть повторов теломеры -8-16
нуклеотидов. Предполагают, что как только теломеры укорачиваются ниже некой критической
длины, происходит остановка клеточного цикла и старение клетки. Предложена
модель старения, которая основывается на том, что гены, расположенные рядом с
теломерой, подвергаются нестабильной транскрипционной репрессии. Предполагают,
что транскрипция локуса «AGE» также подавлена благодаря
теломерному эффекту положения. По мере старения клеток и укорочения теломер эта
репрессия снимается и данный локус становится транскрипционно активным.
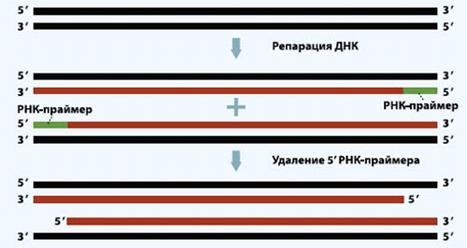
Рисунок 11. Процесс укорочения длины
теломер после цикла репликации ДНК
Наличие постоянно делящихся клеток у животных, тотипотентность растительных клеток предполагает, что они должны либо поддерживать, либо синтезировать полный комплемент теломерных повторов. В 1971 году Оловников предположил существование особого механизма, предотвращающего недорепликацию линейных молекул ДНК прежде всего в половых и раковых клетках, в тоже время данный механизм не действует в большинстве соматических клетках.
Грэйдер и Блэкберн на Tetrachymena впервые в 1985 году обнаружили рибонуклеопротеидный фермент, названный теломеразой. Фермент достраивает 3-конец теломер, т.е. удлиняет их. В состав фермента входит РНК - субъединица, содержащая короткую матричную последовательность РНК, комплементарную теломерной ДНК. Длина теломеразной РНК колеблется от 150 нуклеотидов у простейших до 1400 у дрожжей и 450 у человека.
На последних этапах удвоения хромосом теломераза присоединяется к началу обреченного на гибель участка ДНК, достраивает небольшой отрезок из комплементарных ему нуклеотидов, передвигается на шаг к концу хромосомы - и так до тех пор, пока не восстановит исходную длину теломеры. Таким образом, теломераза - это обратная транскриптаза.
Вторую, комплементарную нить
концевого участка ДНК достраивают ДНК-полимераза и остальной комплекс
ферментов, за счет которых происходит удвоение нитей ДНК при делении клетки.
Теломеразная активность необходима для поддержания теломер в пролиферирующих
клетках. У человека это клетки плода, стволовые клетки костного мозга, клетки
семенников, эпидермиса кожи. У растений теломеразная активность обнаружена в
клетках корневой меристемы, сосудистом камбии, в бутонах, т.е. в клетках с
высоким темпом обновления или находящихся в постоянно размножающемся пуле
дифференцирующихся клеток.
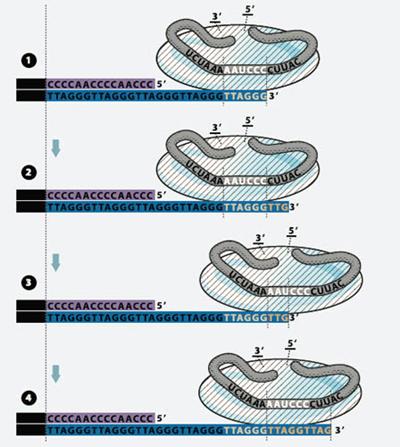
Рисунок 12. Схема работы теломеразы
Клетки имеют систему гомеостаза теломерной длины, которая включает работу теломеразы и механизм проверки теломерной длины. В контроле длины теломер участвует белок Rap 1 (у млекопитающих - TRF1), который специфически связывается с теломерными повторами. Число молекул данного белка на теломере является сигналом аппарату регуляции длины теломер. Например, у дрожжей в теломерах в среднем на каждые 20 оснований TG-последовательности встречается Rap1 - связывающий мотив. Rap1, связываясь с крайним повтором, ограничивает доступ теломеразы к концу хромосомы, следовательно не происходит удлинения теломерной ДНК. Согласно другому предположению Rap1-белок прямо взаимодействует с теломеразой и негативно регулирует работу фермента.
Длина теломер является величиной, характерной для вида. У млекопитающих она колеблется от 5 до нескольких десятков тпн. Но в некоторых случаях (инбридинг, опухолевая трансформация) размер теломер может резко изменяться (как увеличиваться, так и уменьшаться). Длина теломер может изменяться в зависимости от стадии развития. На ячмене показано, что в процессе развития зародыша теломеры укорачиваются с 75 т.п.н. до 25 т.п.н.
У дрозофилы и растений семейства луковичных фермент теломераза отсутствует. У луковичных клетки поддерживают длину хромосом с помощью механизма рекомбинации. Предполагают, что при этом используются внутренние TG-участки.
В клетках дрозофилы для удлинения концов хромосом используется теломерспецифическая транспозиция двух семейств ретротранспозонов.
Теломеры дрозофилы. В 80-е гг. было установлено, что в теломерных участках хромосом дрозофилы локализовано семейство повторов HeT-A. Теломерных повторов типа TG у дрозофилы нет. НеТ-А - повторы являются ретротранспозонами типа LINE, которые не содержат длинных концевых повторов и заканчиваются на 3-конце poly-A-последовательностью. Концы хромосом представляют собой цепочку мигрирующих элементов, присоединённых друг к другу с помощью поли-А.
В объеме интерфазного ядра каждое
плечо хромосомы располагается в определенной зоне, объем которой не перекрывает
объем соседних хромосом, хотя они примыкают друг к другу. Каждая из хромосом в
нескольких местах связана с ядерной оболочкой. Все теломерные участки фиксированы
на ядерной мембране на одном полюсе интерфазного ядра; на противоположном
полюсе ядра располагаются (тоже фиксированные на мембране) центромерные районы
хромосом. В последнее время показано, что в нормальных клетках богатые генами
хромосомы располагаются ближе к центру ядра, а бедные генами хромосомы - на
периферии ядра. Область, прилежащая к ядерной оболочке, и области, прилежащие к
конститутивному (н-р, прицентромерному) гетерохроматину, являются в ядре
неактивными компартментами. Простое перемещение генов в эти компартменты
приводит к их долговременной инактивации. Пример: в эритроидных клетках
глобиновые гены располагаются далеко от конститутивного гетерохроматина, тогда
как в неэритроидных клетках они практически контактируют с конститутивным гетерохроматином.
4. Половые хромосомы
Половые хромосомы, в отличие от аутосом <#"870758.files/image012.jpg">
Рисунок 13. Карта Х-хромосомы
человека
На стрекозах показано, что форма XY эволюционно более поздняя, чем ХО. Другая точка зрения - половые хромосомы произошли от обычной пары аутосом, несущей гены, определяющие пол. Поэтому у одних видов (более примитивных) Y-хромосома такая же по размерам, как и Х-хромосома, конъюгирует с ней полностью или частично, участвует в кроссинговере. А у других видов - она маленькая, с Х-хромосомой соединяется конец в конец, без кроссинговера. В процессе эволюции Y- хромосома почему-то теряет активные гены, деградирует и исчезает, потому форма XY предшествует ХО.
Рисунок 14. Половые хромосомы (Х и Y)
Y-хромосома
Y-хромосома - самая вариабельная хромосома генома. У человека она генетически почти пустая (ген волосатости ушей и перепонок между пальцами ног). У других видов может содержать много активных генов - у гуппи - около 30 Y-генов окраски самцов (и только 1 аутосомный ген).
Y-хромосома Drosophila. Содержит 9 генов: 6 определяют фертильность самцов, 3 bobbed кластер генов рРНК. Активность bb генов приводит к формированию ядрышка. Ядрышкообразующий bb ген есть и в Х-хромосоме - сайт спаривания Х и Y хромосом - сайт collohaes. Ответственными за конъюгацию являются короткие последовательности нуклеотидов (240 п.н.), расположенные между генами рРНК в Х и Y - хромосомах. Удаление bb локуса - нет конъюгации половых хромосом. Ещё один ген - crystal - влияет на поведение хромосом в мейозе. Его делеция - нарушается расщепление хромосом в мейозе.
У дрозофилы 6 факторов фертильности самцов. Из них 3 очень большие - занимают по 10% Y- хромосомы каждый, т.е. по 4000 т.п.н.
В составе ДНК Y-хромосомы 2 типа последовательностей:
Y - специфичные - семейства из 200-2000 копий, организованы в кластеры тандемно повторенных единиц длиной 200-400 п.н. Расположены, вероятно, в петлях.
Y-ассоциированные (встречаются в других хромосомах).
Y-хромосома человекахромосома является наименьшей по размеру из 24 хромосом у человека и содержит около 2-3% ДНК гаплоидного генома, составляя приблизительно 51 Mb. Из всего объема ДНК Y-хромосомы на данный момент секвенировано 21.8 Mb. Короткое плечо Y-хромосомы (Yp) содержит примерно 11 Mb, а длинное плечо (Yq) - 40 Mb ДНК, из которых около 7 Mb приходятся на эухроматиновую часть Yq и около 3 Mb ДНК на центромерную область хромосомы. Большая часть (~60%) длинного плеча Y-хромосомы представляет собой функционально неактивный гетерохроматин, имеющий размер около 24 Mb. В Y-хромосоме выделяют несколько областей: псевдоаутосомные области (PARs); - эухроматиновую область короткого плеча (Yp11); - эухроматиновую область проксимальной части длинного плеча (Yq11); - гетерохроматиновую область дистальной части длинного плеча (Yq12); - область прицентромерного гетерохроматина.хромосома содержит около 100 функциональных генов. Из-за наличия на Х и Y-хромосомах (на теломерах) гомологичных PAR-регионов, половые хромосомы регулярно конъюгируют и рекомбинируют участками этих регионов в зиготене и пахитене профазы I мейоза. Однако большая часть (~95%) Y-хромосомы не принимает участия в рекомбинации, и поэтому называется нерекомбинирующей областью Y-хромосомы (NRY - Non Recombinant Region Y chromosome).
Гетерохроматиновая область длинного плеча Y-хромосомы является генетически инертной и содержит различные типы повторов, в том числе высокоповторяющиеся последовательности двух семейств DYZ1 и DYZ2, каждый из которых представлен приблизительно 5000 и 2000 копиями соответственно.
На основе сравнительного анализа генов гоносом X и Y в Y-хромосоме выделяют три группы генов:
1. PAR-гены (PAR - Pseudoautosomal Region; гены псевдоаутосомных областей PAR1 и PAR2), локализованные в теломерных областях Y-хромосомы;
2. X-Y гомологичные гены, локализованные в нерекомбинирующих областях Yp и Yq;
. 3. Y-специфичные гены, расположенные в
нерекомбинирующих областях Yp и Yq.
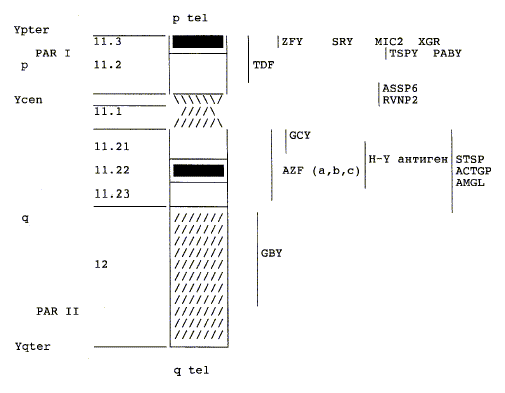
Рисунок 15. Y-хромосома
Первая группа представлена генами псевдоаутосомных областей (регионов). Они являются идентичными для X- и Y-хромосом и наследуются как аутосомные гены. PAR1-регион расположен на конце короткого плеча Y-хромосомы, он больше по размеру, чем PAR2-регион, локализованный на конце длинного плеча Y-хромосомы, и его размер приблизительно оценивается в 2,6 Mb. Так как делеции PAR1 приводят к нарушениям конъюгации гоносом во время мейоза у мужчин и могут привести к мужскому бесплодию, предполагается, что PAR-регионы имеют существенное значение для нормального протекания сперматогенеза у мужчин.
Вторая группа генов содержит X-Y-гомологичные, но не идентичные гены, которые локализованы в нерекомбинирующих районах Y-хромосомы (на Yp и Yq). В нее включены 10 генов, представленных на Y-хромосоме одной копией, большинство из них экспрессируются у человека во многих тканях и органах, включая яички и предстательную железу. До сих пор неизвестно, являются ли эти X-Y-гомологичные гены функционально взаимозаменяемыми.
Третью группу генов составляют 11 генов, которые расположены в нерекомбинирующем районе Y-гоносомы (NRY). Все эти гены, за исключением гена SRY (Sex-Determining Region Y Chromosome, пол-детерминирующий регион Y-хромосомы), представленного одной копией, являются мультикопийными, и их копии расположены на обоих плечах Y-хромосомы. Некоторые из них являются генами-кандидатами на AZF-фактор (Azoospermia factor, или фактор азооспермии).
О точных функциях большинства этих генов известно мало. Продукты, кодируемые генами нерекомбинирующего региона Y-хромосомы, выполняют различные функции, например, среди них имеются факторы транскрипции, цитокиновые рецепторы, протеинкиназы и фосфатазы, которые могут влиять на клеточную пролиферацию и/или передачу сигналов в клетке.
На длинном плече Y-хромосомы расположен AZF (Azoospermia Factor) локус - содержит гены, контролирующие процесс дифференцировки половых клеток, т.е. сперматогенез. В данном локусе выделяют 3 региона - a (800 т.п.н.), b (3,2 млн пн), c (3,5 млн. пн). Микроделеции участков данного локуса являются одной из основных генетических причин мужского бесплодия. Микроделеции длинного плеча Y-хромосомы обнаруживаются у 11% мужчин с азооспермией и у 8% мужчин с олигозооспермией тяжелой степени. При делеции всего с-региона AZF локуса возможно возникновение блока в митозе и мейозе при сперматогенезе; на гистологических препаратах у таких больных в большинстве семенных канальцев отсутствуют половые клетки.