Материал: Хромосомы эукариот
Хромосомы эукариот
Контрольная работа
Хромосомы
эукариот
Содержание
1. Химический состав хроматина
. Уровни организации хроматина. Гетерохроматин и эухроматин
. Строение хромосом эукариот
. Половые хромосомы
. Эволюция хромосом млекопитающих
. Номенклатура хромосом человека
Литература
1. Химический состав хроматина
Главная количественная особенность генетического материала эукариот - наличие избыточной ДНК. Этот факт легко выявляется при анализе отношения числа генов к количеству ДНК в геноме бактерий и млекопитающих. Около 95% генома бактерий состоит из кодирующих последовательностей. Остальные 5%, по-видимому, заняты регуляторными элементами. Иная картина наблюдается у эукариотических организмов. Например, у человека насчитывают приблизительно 50 тысяч генов (имеется в виду только суммарная длина кодирующих участков ДНК - экзонов). В то же время размер генома человека 3×109 (три миллиарда) п.н. Это означает, что кодирующая часть его генома составляет всего 15 - 20 % от тотальной ДНК. Существует значительное число видов, геном которых в десятки раз больше генома человека, например некоторые рыбы, хвостатые амфибии, лилейные. Избыточная ДНК характерна для всех эукариот.
По химическому составу хроматин представляет собой комплекс ДНК и белков. В ДНК эукариот выделяют 3 фракции:
уникальные последовательности - у животных составляют 40-90% от всей ядерной ДНК; у растений - 12-60%. У человека около 50% ядерной ДНК представлено уникальными последовательностями длиной 1-2 тпн. Эти фрагменты разделены между собой умеренно повторяющимися последовательностями длиной 0,1-0,3 тпн. Большая часть уникальной ДНК является «некодирующей», так, например, в геноме человека из 50% уникальной ДНК на кодирующие участки приходится только 5%.
Умеренно повторяющиеся последовательности ДНК кодируют, как правило, тРНК, рРНК, гистоны. Пример, гены 18S и 28S рРНК образуют тандемные пары (мономерные единицы расположены по типу «голова к хвосту»). Спейсер тоже транскрибируется, в его состав входит ген 5,8S рРНК. У человека и мыши гены рРНК располагаются в нескольких кластерах в акроцентрических хромосомах. Каждый кластер генов рРНК соответствует ядрышковому организатору. Гены ранних гистонов у морского ежа входят в состав одной единицы, в результате повторения которой образуется кластер тандемных генов, разделяемых спейсерами - Н1 Н4 Н2В Н3 Н2А. У дрозофилы порядок расположения гистоновых генов иной - Н1 Н3 Н4 Н2А Н2В. У некоторых млекопитающих гены гистонов располагаются по отдельности.
Сателлитная ДНК - высокоповторяющиеся последовательности ДНК. Располагаются в центромерных, теломерных районах и в участках интеркалярного гетерохроматина. У разных видов на долю сателлитной ДНК приходится от 0,3% до 28% от всей ядерной ДНК. Близкие виды, например мышь и крыса, имеют совершенно различные высокочастотные последовательности, у крысы их нуклеотидный состав не отличается от основной ДНК, тогда как геном мыши содержит четкий АТ-богатый сателлит. Это означает, что высокочастотная ДНК способна к быстрым изменениям в ходе видообразования.
Последовательности сателлитной ДНК - это короткие тандемные повторы. У человека сателлитная ДНК делится на I, II, III классы (с длиной повторяющейся последовательности 1-20 п.н.). Также выделяют альфа, бета и гамма типы (с длиной повтора 170 п.н., 68 п.н. и 220 п.н. соответственно). Сателлитные повторы имеют различную степень обогащенности АТ- и ГЦ -пар (тип 1 обогащен парами АТ). Сателлитная ДНК специфично распределена по разным хромосома. Так, в прицентромерном гетерохроматине хромосом 3 и 4 представлен сат ДНК 1. В прицентромерном гетерохроматине хромосом групп Д и G локализованы сатДНК1 и 3 классов. Распределение альфа, бета и гамма сателлитных ДНК также хромосом специфично. Альфа сателлитные повторы располагаются в основном в центромерных участках хромосом. Имеют элементапрную единицу повтора около 170 п.н. и могут присутствовать в тандеме, достигающем длины до 1 млн.п.н.
В сателлитной ДНК выделяют 2 типа последовательностей:
микросателлиты - единица повтора состоит из 1-5 нуклеотидов. Общая длина кластера - несколько десятков нуклеотидов. Пример: (АТ)n; (A)n; (AC)n. В кодирующей части генов чаще встречаются тринуклеотидные повторы. Ди-, тетра- и пентануклеотидные повторы редки в кодирующей части генома, так как увеличение их числа обязательно приведет к сдвигу рамки считывания. Микросателлитные последовательности обнаружены в геноме как прокариот, так и эукариот. Из-за высокой скорости мутирования микросателлиты обеспечивают генетическое разнообразие геномов.
минисателлиты - единица повтора состоит из 10-100 пн. Общий размер кластера 0,5-100 тпн.
Общий размер кластера 0,5-100 тпн. Их еще называют VNTR - вариабельные по числу тандемные повторы. Они могут находиться внутри или между генами. Число копий каждой специфической последовательности в разных локусах варьирует от 1000 до 5000 п.н. Вариации длин таких областей лежат в основе метода ДНК-фингерпринтинга (метод отпечатков).
По локализации выделяют:
сателлитные повторы в области промотора - (А)n - стимулирует экспрессию гена, т.к. обуславливает жесткую структуру двойной спирали - на этом участке не образуются нуклеосомы, что облегчает доступ ДНК-полимераз и факторов транскрипции к промотору. Длина полипролиновых, полиаланиновых и полиглутаминовых участков, кодируемых микросателлитными тринуклеотидными повторами, влияет на белок-белковые взаимодействия, в том числе и с факторами активации транскрипции.
сателлитные повторы в интронах - часто ингибируют экспрессию гена. (АС)21 в интроне гена рецептора эпидермального фактора роста снижает транскрипцию гена на 80%.
сателлитные повторы в нетранслируемой 5-области гена (между промотором и геном) - (С)n, (AC)n, (GC)n, (AT)n - ингибируют экспрессию гена.
повторы в транслируемой области гена. Пример - хорея Гентингтона - увеличение длины повтора (CAG)n в первом экзоне гена белка гентингтина приводит к удлинению полиглутаминового участка в белке. Синтезируется токсичная форма белка, что приводит к гибели нейронов. Это пример динамических мутаций или экспансии тринуклеотидных повторов - связаны с изменением длины тринуклеотидных повторов. Скорость мутирования связана с числом копий триплета. После превышения определенного порога длины эти повторы становятся нестабильными и их длина увеличивается в последующих поколениях. У здоровых людей число повторов колеблется от 6 до 39. У больных - 36-180. У взрослых болезнь проявляется при 40-55 повторах, при числе повторов больше 70 заболевание проявляется уже у детей. То есть для данных мутаций характерно явление антиципации - возрастание пенетрантности заболевания в ряду поколений, более раннее начало заболевания.
Впервые динамические мутации описаны в 1991 году. Известны они только у людей. Всего пока описано 16 наследственных заболеваний (табл. 1). Все они связаны с поражением головного мозга и подкорковых структур. Экспансия происходит как в мейозе, так и в митозе, затрагивает чаще аллели с изначально большим числом повторов.
Динамические мутации являются причиной развития
синдрома фрагильной Х-хромосомы или синдрома Мартина-Белл. Синдром Мартина-Белл
- одна из наиболее частых наследственных форм умственной отсталости (частота
заболевания составляет 1 случай на 4000 мужчин и 1 случай на 8000 женщин).
Синдром связан с образованием ломкого сайта в Х-хромосоме из-за увеличения
повторов (CGG) в
5-нетранслируемой области гена FMR1,
который экспрессируется в мозге и семенниках. Ген кодирует РНК-связывающий
белок, циркулирующий в клетке между ядром и цитоплазмой. У здоровых людей ген
содержит 2-54 триплета (CGG).
Увеличение длины до 200 триплетов - это предмутационное состояние, не
изменяющее фенотип человека. Увеличение числа копий свыше 200 триплетов -
полная мутация и проявление синдрома. Увеличение числа копий триплета приводит
к гиперметилированию регуляторной зоны гена (промотора), в результате резко
снижается или полностью ингибируется транскрипция ген.
Таблица 1
Болезни экспансии повторяющихся последовательностей
|
Заболевание |
Ген |
Локус |
Тип повтора |
|
Болезни экспансии некодирующих повторов |
|||
|
Синдром Мартина-Белл |
FMR1 |
Xq27.3 |
CGG |
|
Атаксия Фридрейха |
X25 |
Xq13-21.1 |
GAA |
|
Миотоническая дистрофия, тип 1 |
DMPK |
19q13.3 |
CTG |
|
Спиноцеребеллярная атаксия, тип 8 |
SCA8 |
13q21 |
CTG |
|
Спиноцеребеллярная атаксия, тип 12 |
SCA12 |
5q31-33 |
CAG |
|
Спиноцеребеллярная атаксия, тип 10 |
SCA10 |
22q13 |
ATTCT |
|
Миотоническая дистрофия, тип 2 |
ZNF9 |
3q21 |
CCTG |
|
Болезни экспансии кодирующих повторов |
|||
|
Спинобульбарная мышечная атрофия (болезнь Кеннеди) |
AR |
Xq13-21 |
CAG |
|
Хорея Гентингтона |
HD |
CAG |
|
|
Дентато-рубро-паллидо-льюисова атрофия |
DRPLA |
12p13.31 |
CAG |
|
Спиноцеребеллярная атаксия, тип 1 |
SCA1 |
6p23 |
CAG |
|
Спиноцеребеллярная атаксия, тип 2 |
SCA2 |
12q24.1 |
CAG |
|
Спиноцеребеллярная атаксия, тип 3 |
SCA3 |
14q32.1 |
CAG |
|
Спиноцеребеллярная атаксия, тип 6 |
CACNL1A4 |
19p13 |
CAG |
|
Спиноцеребеллярная атаксия, тип 7 |
SCA7 |
13p12-13 |
CAG |
|
Спиноцеребеллярная атаксия, тип 17 |
TBP |
6q27 |
CAG |
Другими наследственными заболеваниями, обусловленными динамическими мутациями, являются атаксия Фридрейха, миотоническая дистрофия первого и второго типа, болезнь Кеннеди, спиноцеребеллярная атаксия, прогрессирующая миоклонус-эпилепсия.
Еще одна категория повторов в геноме эукариот - короткие и длинные разбросанные по геному ДНК-повторы (не тандемные).
Короткие рассеянные по геному элементы - SINE - последовательности длиной менее 500 п.н. Их копийность в геноме человека составляет не менее 500 000. К этой группе повторов относится семейство Alu-повторов (они содержат сайты рестрикции для эндонуклеазы AluI). Alu-повторы в геноме человека составляют более 5% от суммарного количества ДНК. Функция их не ясна.
Другая группа рассеянных повторов - LINE. У человека обнаружено одно семейство этих повторов - L1-повторы. Длина повтора около 6400 п.н., суммарно представлены в геноме до 100000 раз. Проявляет свойства ретротранспозонов (транскрипция последовательности, синтез на мРНК с помощью обратной транскриптазы новой копии ДНК повтора, новая копия интегрирует в хромососму на новом месте).
Эухроматическая часть генома построена по принципу чередования (интерсперсии) уникальных и повторяющихся последовательностей. Условно выделяют два основных типа интерсперсии, получивших названия по тем видам, у которых они впервые были описаны: интерсперсия типа «ксенопус» и типа «дрозофила».
Примерно в 50 % генома Xenopus laevis уникальные последовательности из 800-1200 п.н. чередуются с повторяющимися, средний размер которых 300 п.н. В остальной части геномов типа «ксенопус» расстояния между соседними повторами значительно превышают 1-2 п.н. Структура генома типа «ксенопус» широко распространена, особенно среди животных. Млекопитающие и человек также относятся к этому типу организации генома. Особенность генома человека и других приматов составляют интерсперсные высокочастотные повторы длиной около 300 п.н. У человека эти повторы содержат сайт, разрезаемый ферментом рестрикции Alu I.
У D. melanogaster параметры интерсперсии резко отличаются от видов с типом генома «ксенопус»: повторяющиеся последовательности длиной 5600 п.н. чередуются с уникальными, длина которых не менее 13000 п.н. Интересно отметить, что у домашней мухи геном устроен по типу «ксенопус». Этот факт прямо указывает на то, что в ходе эволюции возможны очень быстрые преобразования характера чередования последовательностей и в эухроматической части генома. Птицы по параметрам интерсперсии занимают промежуточное положение между типом «ксенопус» и типом «дрозофила».
Как показывают результаты исследований последних
лет, многие виды животных и растений по организации генома не могут быть строго
отнесены ни к тому, ни к другому типу. Так, в геномах млекопитающих встречаются
длинные повторы - в несколько тысяч пар нуклеотидов, в геномах лилейных до 90%
ДНК может быть представлено повторяющимися последовательностями. Например,
геном гороха не содержит уникальных последовательностей, превышающих по длине
300 п.н.
2. Уровни организации хроматина.
Гетерохроматин и эухроматин
В ядре ДНК всегда находится в комплексе с белками и упакована в той или иной степени в нуклеопротеиновые структуры.
В хромосомах ДНК (около 40% от всего хроматина) находится в комплексе с основными и кислыми белками, что обеспечивает многоступенчатую компактизацию молекулы ДНК. Первые уровни компактизации осуществляются при взаимодействии ДНК с основными белками - гистонами. Гистоны имеют повышенное содержание основных аминокислот - лизина и аргинина. Пять типов гистонов отличаются друг от друга относительным содержанием этих двух аминокислот. Гистоны Н3 и Н4 очень консервативны. Секвенирование гена гистона Н4 показало, что у теленка и гороха этот белок отличается всего двумя аминокислотами. Наиболее изменчивы гистоны Н2А и Н2В. Комплекс между ДНК и гистонами формирует нуклеосомную структуру хроматина. Пары молекул гистонов Н2А, Н2В, Н3 и Н4 формируют гистоновый октамер клиновидной формы (рис. 1). Узкая часть образована тетрамером Н3-Н4, а широкая состоит из Н2А-Н2В. N-концевые части гистонов свободно расходятся в стороны. Участок ДНК в 146 пн связывается с октамером, делая 1,75 оборота вокруг него. Комплекс данного участка ДНК с гистоновым октамером называют нуклеосомой. Участок ДНК между соседними нуклеосомами называют линкерным (около 60 пн). Более 90% ДНК в клетке присутствует в виде нуклеосом, при этом длина нити ДНК уменьшается в 7 раз, а толщина сформированной нуклеопротеиновой нити составляет 10 нм.
Гистоны контактируют с фосфодиэфирным остовом
молекулы ДНК. Существуют и гидрофобные взаимодействия с остатками рибозы.
Азотистые основания во взаимодействии с гистонами не участвуют. Поэтому
связывание ДНК с нуклеосомной глобулой не является специфичным в отношении
нуклеотидной последовательности.
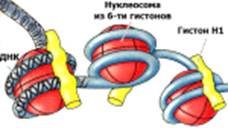
Рисунок 1. Строение нуклеосом
Гистон Н1 взаимодействует с обоими концами ДНК,
входящей в состав нуклеосомы, в районе тетрамера Н3-Н4, т.е. Н1 как бы
обозначает границы линкерной ДНК. В молекуле гистона Н1 можно выделить
глобулярную сердцевину, N-конец
и С-конец. Взаимодействие между N-
и С-концами соседних молекул гистона Н1 обеспечивает сближение нуклеосом. При
этом нуклеосомная нить сворачивается в спираль или образует зигзагообразную
нить толщиной 30 нм, состоящую из сближенных нуклеосом - нуклеомеров.
Каждая нуклеомера состоит из 8-10 нуклеосом.
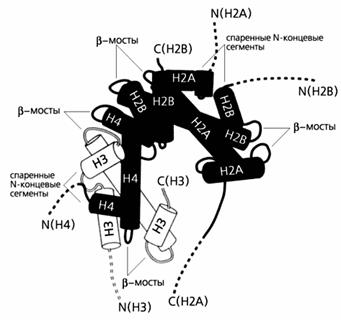
Рисунок 2. Взаимодействие гистонов в составе
нуклеосом
Исследования последних лет подтверждают
зигзагообразную модель организации 30 нм фибриллы. В стабилизации этой фибриллы
большую роль играют взаимодействия N-концевых
доменов гистонов соседних нуклеосом. Архитектура фибриллы может существенно
меняться при модификации N-концевых
доменов гистонов, что может стимулировать либо дальнейшую конденсацию, либо
деконденсацию фибриллы. Есть данные о том, что ацетилирование гистонов
способствует разворачиванию компактной 30 нм хроматиновой фибриллы до
нуклеосомной нити.