Материал: Хромосомы эукариот
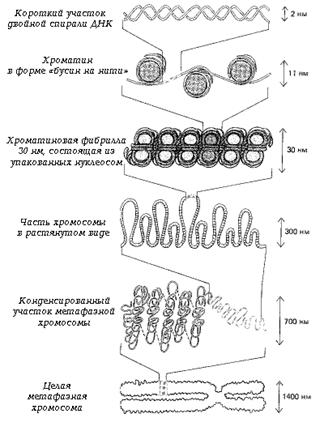
Рисунок 3. Уровни компактизации хроматина
У ксенопуса выделены белки, контролирующие взаимодействие ДНК с гистоновыми белками. Например, белок нуклеоплазмин - состоит из 5 идентичных субъединиц, контролирует образование нуклеосом. Этот белок кислый, он не связывается со свободной ДНК, связывается только с гистонами.
Экспрессия генов основных гистонов происходит только в S -фазу чтобы обеспечить упаковку вновь синтезированной ДНК. Но ограничение синтеза гистонов может грозить нарушением целостности хромосом, например, при репарации поврежденной ДНК. Поэтому многие организмы имеют альтернативные копии гистоновых генов, которые кодируют варианты гистонов и экспрессируются конститутивно на низком уровне в течение всего клеточного цикла.
Описаны вариантные формы гистонов (табл. 2), которые кодируются отдельными генами. Включение в нуклеосомную частицу вариантных форм гистонов может существенно изменять структуру гистонового октамера. Существует четкая корреляция между присутствием в нуклеосомах вариантных форм гистонов и осуществлением тех или иных функциональных процессов. Например, ряд вариантных форм гистона Н3 (CENP-A) участвует в формировании центромер. Некоторые варианты обмениваются с уже существующими гистонами в ходе развития и дифференцировки - их называют замещающими гистонами. Такое замещение часто приводит к тому, что варианты становятся доминируюшщими в дифференцированной клетке. Предположение - варианты гистонов выполняют спец. функции в клетках.
Имеется много вариантов гистона Н1, например,
Н10, Н5, варианты, специфичные для сперматозоидов (SpH1)
и яичек (H1t).
Наибольшее число вариантов описано для гистона Н2А. Варианты гистона Н2А отличаются
по размеру и последовательности хвоста, а также по характеру распределения в
геноме. Например, H2A-Bbd
локализуется в активной Х-хромосоме и аутосомах, а Macro
Н2А находится в основном в Xi.
У гистона Н3 есть два основных варианта - Н3ю3 и центромерный Н3 (СеnH3),
а также тканеспецифичный вариант Н3.4 (яички млекопитающих). Гистон СеnH3
способствует образованию белковой структуры кинетохоров. Гистон Н3.3 служит
меткой активного хроматина, азмещение Н3 на Н3.3 это динамичный механизм
быстрой активации хроматина. Вариантов гистона Н4 пока не известно.
Таблица 2
Основные варианты гистонов и их действие на хроматин
|
Вариант |
Основной гистон |
Действие на хроматин |
||
|
Н1о |
Н1 |
Конденсация хроматина |
||
|
Н5 |
Н1 |
Конденсация хроматина |
||
|
SpH1 |
Н1 |
Конденсация хроматина |
||
|
H1t |
Н1 |
Открытая структура хроматина |
Н2А |
Конденсация хроматина |
|
H2ABbd |
Н2А |
Открытая структура хроматина |
||
|
H2AvD |
Н2А |
|
||
|
H2A.X |
Н2А |
Конденсация хроматина |
||
|
H2A.Z |
Н2А |
Открытая/закрытая структура хроматина |
||
|
SpH2B |
Н2В |
Конденсация хроматина |
||
|
CenH3 |
Н3 |
|
||
|
H3.3 |
Н3 |
Открытая структура хроматина |
||
|
H3.4 |
Н3 |
|
Дальнейшая упаковка хроматина достигается за счет взаимодействия ДНК с негистоновыми белками. Они разнообразны - более 500, составляют до 2/3 всех белков хроматина. Многие из этих белков участвуют в репликации, репарации ДНК, транскрипции. Часть из них выполняет структурную функцию - образуют ядерную мембрану, поровые комплексы. Часть белков формирует белковый каркас хромосом. На белках ядерной мембраны в интерфазу закреплены расположенные розетками петли 30-нм фибриллы. Это третий уровень компактизации хроматина - хромомерный. Средний размер розеток достигает 120-150 нм. Каждый хромомер состоит из нескольких, содержащих нуклеомеры петель, которые связаны в одном центре. Хромомеры связаны друг с другом участками нуклеосомного хроматина. Размер отдельной петли совпадает с размером среднего репликона и может соответствовать одному или нескольким генам (50-100 тпн). На хромосому в среднем приходится более 2000 таких петельных доменов ДНК. Петельно-доменная структура хроматина организует функциональные единицы хромосом - репликоны и транскрибируемые гены. Наряду с участками начала репликации в области прикрепления ДНК к ядерному матриксу часто локализуются и другие регуляторные элементы - энхансеры, сайленсеры, промоторы и т.д. Помещение того или иного промотора, гена или генного домена на ядерный матрикс способствует его активации. Далее - хромонемный уровень компактизации - нитчатая структура толщиной 0,1-0,2 мкм. Полагают, что отрезок примерно с 18-20 петлевыми доменами образует вокруг осевого элемента хромосомы один виток.
Компактизация метафазных хромосом оценивается как 10000-кратная. К стадии зиготены мейоза наружная поверхность хроматиновой нити содержит всего около 1% ДНК. Механизм не известен. Доказано, что укладка ДНК в митотическую хромосому осуществляется комплексом белков, называемым 13S-конденсином. Комплекс обладает АТФ-азной активностью, способен связываться с ДНК и, вероятно, наматывает ее на себя. 13S-конденсин лягушки состоит из двух структурных субъединиц - ассоциированных с хромосомами белков ХСАР-С и ХСАР-Е и трех регуляторных субъединиц. Вне комплекса ни одна из субъединиц не индуцирует конденсацию хромосом. Мутации в генах, кодирующих белки конденсинового комплекса, нарушают конденсацию и сегрегацию хромосом, блокируют клетки в митозе. В процессе упаковки хромосом конденсин локализуется в районах, где гистон Н3 фосфорилирован. По мере фосфорилирования гистона Н3 ДНК становится более доступной для связывания с конденсином. Конденсация хромосом и фосфорилирование гистона Н3 начинается с центромерных областей и распространяется к теломерным.
К стадии зиготены мейоза на наружней поверхности хроматиновой нити остается всего около 1% ДНК.
Степень деконденсации хроматина в интерфазном ядре отражает его функциональную нагрузку. Чем более диффузен хроматин, тем он активнее. В составе хромосом выделяют участки гетерохроматина и эухроматина. Эухроматин в интерфазе находится в деспирализованном состоянии, в нем находятся структурные активные гены. В эухроматиновых участках, помимо элементарных дезоксирибонуклеопротеидных нитей, имеются рибонуклеопротеидные частицы диаметром 200-500 анстрем, называемые РНП-гранулами. Эти частицы представляют собой форму упаковки молекул РНК, синтезированных на ДНК и соединённых с белком, и служат для завершения образования информационной РНК и переноса её в цитоплазму
Термин «гетерохроматин» был предложен Хейцом в 1928 году. Гетерохроматин расположен в районе центромеры, теломер и внутри плеч хромосом - интеркалярный гетерохроматин. Гетерохроматиновые участки значительно дольше представлены в клеточном цикле в виде плотно спирализованных фрагментов. Они деспирализуются значительно позже, чем эухроматин или совсем не деспирализуются, сохраняясь в интерфазном ядре в виде плотно окрашенных глыбок - хромоцентров. Гетерохроматиновые районы хромосом могут ассоциироваться друг с другом - эктопическая конъюгация. В результате здесь возможна повышенная частота хромосомных перестроек. Еще одной особенностью гетерохроматина является варьирование его количества в геноме.
Гетерохроматиновые участки ДНК содержат долгоживущие разрывы, тогда как в эухроматине разрывы возникают редко и быстро репарируются. Ядра лимфоцитов периферической крови почти полностью состоят из гетерохроматина и неактивны в транскрипции. В них обнаружено около 3000 разрывов на диплоидный геном мыши. Установлено, что после активации лимфоцитов разрывы репарируются. Очень плотно упакованная ДНК сперматозоидов содержит 107 разрывов на геном. Таким образом, наличие разрывов ДНК позволяет плотную упаковку, но несовместимо с транскрипцией.
Стабильно выявляемые гетерохроматиновые районы называют конститутивным гетерохроматином. Эти районы, как правило, генетически не активны. Пример - сателлитная ДНК прицентромерного гетерохроматина. Конститутивный гетерохроматин располагается в одних и тех же положениях на обеих хромосомах из пары гомологов. Гены в гетерохроматине все-таки есть, но их гораздо меньше, чем в эухроматине. Пример - гены рРНК.
Факультативный гетерохроматин формируется при конденсации хроматина на определенных стадиях жизненного цикла и обычно присутствует лишь в одной хромосоме из пары гомологов. Яркий пример - мучнистый червец. У самок этого вида нет факультативного гетерохроматина. У самцов весь отцовский гаплоидный набор хромосом целиком становится гетерохроматиновым. В итоге самец имеет эухроматиновые хромосомы, полученные от матери, и гетерохроматиновые, полученные от отца. В ходе мейоза у самцов гетерохроматиновые хромосомы деспирализуются, в спермии попадает уже эухроматиновый материал. Если потомок окажется самцом, то эти хромосомы конденсируются. Таким образом, у самцов экспрессируются только материнские гены.
У млекопитающих факультативный хроматин проявляется при инактивации Х-хромосомы. В 1949 г Барр и Бертрам обнаружили в ядрах нейронов кошки интенсивно окрашенные тельца, названные тельцами Барра. Они представляют собой неактивную Х-хромосому. Различают три возможных расположения полового хроматина в ядре: тесное соприкосновение его с ядрышком; свободное расположение в кариоплазме и контакт с ядерной ембраной.
Таким образом, у самок млекопитающих транскрипционно активна только одна Х-хромосома - это феномен компенсации дозы гена. Факультативный гетерохроматин обогащен повторами типа LINE, которые способствуют конденсации хроматина.
В ходе раннего развития самок млекопитающих обе Х-хромосомы активны. На предимплантационных стадиях развития эмбриона происходит инактивация Х-хромосомы, унаследованной от отца. Во время имплантации зародыша происходит реактивация и последующая инактивация случайно либо отцовской, либо материнской Х-хромосомы. Иногда наблюдается предпочтительная инактивация отцовской Х-хромосомы (у сумчатых). Процесс инактивации контролируется сложным локусом Х-хромосомы - центром инактивации Xiс. Данный локус содержит ген Xist (Х inactive specific transcript). Продуктом этого гена является некодирующая ядерная РНК размером 16 тн.
Ген Xist имеет 3 промотора - Р0, Р1 и Р2. Если транскрипция идет с прототоров Р1 или Р2 - образуется стабильный продукт размером 15 т.п.н., если с промотора Р0 - возникает нестабильный продукт. Переключение транскрипции с Ро на Р1/Р2 коррелирует с началом инактивации Х-хромосомы. В функционально активной Х-хромосоме ген Xist инактивирован за счет метилирования ЦГ-динуклеотидов в промоторе гена.
РНК гена Xist не способна переходить с одной Х-хромосомы на другую. РНК Xist присоединяет различные белки, образуя комплексы, которые распределяются вдоль всей Х-хромосомы, запуская ее инактивацию. Они, несомненно, принимают участие в установлении неактивного состояния, так как Х-хромосома, у которой отсутствует район гена Xist, никогда не инактивируется. Если же ген Xist искусственно перенести на аутосому, то она инактивируется.
В период инициации инактивации продукт гена Xist становится стабильным и распространяется вдоль по всей длине Х-хромосомы. Это подавляет транскрипцию генов и приводит к модификации гистонов. После отделения линии герминальных клеток в соматических клетках происходит гиперметилирование инактивируемой хромосомы; неактивное состояние становится необратимым и наследуется в ряду клеточных поколений. В линии герминальных клеток самок ДНК инактивированной Х-хромосомы остается неметилированной и впоследствии хромосома реактивируется незадолго до вхождения клеток в мейоз. В зрелых ооцитах обе Х-хромосомы активны.
Выбор того, какая Х-хромосома инактивируется, случаен, но это может регулироваться аллелями Xce (X-linced X controlling element). На линиях мышей было обнаружено три аллеля Хсе - «слабый» Xcea, «промежуточный» Xceb и «сильный» Xcec. В гетерозиготах наиболее часто инактивируются те Х-хромосомы, которые несут более слабый аллель. У гомозигот выбор происходит случайно. Xce локус расположен вблизи Xic. Предполагается, что Xce связывают транс-факторы, регулирующие работу генов в Xic, предопределяя выбор между Х-хромосомами.
Ряд генов неактивной Х-хромосомы ускользает от инактивации. Например, избегает инактивации район спаривания с Y-хромосомой. В данном локусе находятся гены, присутствующие и на Х- и на Y-хромосомах: то есть и у XY-самцов таких генов по паре, и у XX-самок их столько же - этим генам не нужна компенсация дозы.
Формирование гетерохроматина строго детерминировано и происходит на определенной стадии эмбрионального развития, когда начинается транскрипция на хромосомах развивающегося эмбриона. Формирование гетерохроматиновых доменов надежно защищает организм от экспрессии генетического материала, которая не нужна в соматических клетках.
Образование факультативного гетерохроматина - механизм регуляции активности генов. Пример - мозаичное проявление признаков, контролируемых сцепленными с полом генами у самок млекопитающих - кошки с черепаховой окраской (пятна черной и желтой шерсти); женщины, гетерозиготные по сцепленной с полом мутации эктодермальной дисплазии (на некоторых участках челюсти нет зубов; на теле чередуются участки кожи с наличием и отсутствием потовых желез).
Эпигенетика занимается изучением механизмов наследственности, которые модифицируют работу генов без изменения их структуры. Причем эти модификации сохраняются при митотическом делении клеток. Наиболее часто эпигенетические механизмы обеспечивают долговременную репрессию значительной части генома в специализированных клетках многоклеточного организма. Эпигенетические механизмы обеспечивают и импринтинг - инактивацию ряда генов в одной из родительских хромосом. Наиболее изученным механизмом является метилирование ДНК. В последние годы показана роль модификации гистонов, их ацетилирования (лизина) и метилирования (лизина и аргинина), а также включения в нуклеосомы неканонических форм гистонов. Модифицируются в основном свободные N-концы гистонов. Добавление ацетильных групп нейтрализует положительный заряд молекулы гистона, это изменяет конформацию нуклеосомы и изменяет доступность ДНК для различных белков. Другой вариант - с модифицированными остатками аминокислот гистонов могут специфически связываться определенные белки, запуская цепочку реакций. Метилирование лизина и аргинина участвует в образовании гетерохроматина, репарации и регуляции транскрипции. Причем разное число метильных групп у одного остатка выполняет разные биологические функции. Метилирование осуществляется ферментами гистон-метилтрансферазами, а удаление метильных групп обеспечивают гистон-деметилазы. В отличие от метилирования ацетильная группа на остатке лизина может быть только одна. Ее присоединение осуществляют гистон-ацетилтрансферазы, а удаление - гистон-деацетилазы. Эухроматиновые домены характеризуются гиперацетилированной формой гистонов; в гетерохроматине гистоны гипоацетилированы.
Ацетилирование гистонов ослабляет межнуклеосомное взаимодействие, а также взаимодействие хвостов нуклеосомы с линкерной ДНК. Доступность ДНК при этом увеличивается, то есть ацетилирование гистонов связано с активацией транскрипции.
Активный промотор гена должен быть свободен от нуклеосом. Важную роль в этом играет ацетилирование гистонов, в том числе гистона H2A.Z в промоторной области. Гистон H2A.Z присутствует как в активных, так и в неактивных промоторах и именно его ацетилирование существенно для активации промотора.
Метилирование гистонов не изменяет суммарный заряд нуклеосомы. Но ковалентно модифицированные гистоны служат «метками» для связывания белковых факторов, которые стимулируют определенные события. Наиболее распространенный вариант метилирования гистонов - это метилирование лизина.