Материал: Барановский
•стерилизация насыщенным паром под давлением (автоклавирование),
•дробная стерилизация (тиндализация), кипячение.
Методы холодной стерилизации:
•стерилизация фильтрованием,
•газообразными средствами,
•ультрафиолетовыми лучами и другими видами излучений
26. Основные требования к работе с главным и рабочим банками культуры клеток.
Главный банк клеток (ГБК) ― запас клеток, полученных из одного посевного пула клеток, сохраняемых в контейнерах в равных частях однородного состава на определенном уровне пассажа при температуре не выше минус 70 оС. Предназначен для последующего создания рабочего банка клеток.
Рабочий банк клеток (РБК) ― запас клеток однородного состава, полученных из ГБК на определенном уровне пассажа, сохраняемых в контейнерах в равных частях при температуре не выше минус 70 оС. Используются для получения производственной клеточной культуры.
Во время аттестации проверяют следующие показали ГБК и РБК
•Наименование клеточной культуры;
•Коллекционный шифр (клеточной линии, ГБК, РБК);
•История получения (происхождение) клеточной культуры и создания ГБК и РБК;
•Запас клеток (количество сохраняемых контейнеров в банках клеток, количество клеток в емкости);
•Номер пассажа и дата закладки клеток на хранение;
•Условия криоконсервации, режим хранения и жизнеспособность клеток после размораживания;
•Ростовые свойства (способ культивирования, питательная среда, посевная концентрация, метод снятия клеток, кратность рассева, температура культивирования, частота пассирования);
•Подлинность (морфология, кариологическая характеристика, молекулярно-генетические методы исследования);
•Стерильность (отсутствие микробных агентов, в том числе микоплазм);
•Присутствие посторонних вирусов, в том числе эндогенных;
•Туморогенность (если применимо);
•Онкогенность (если применимо);
•Стабильность биологических свойств (количество рекомендованных для производства пассажей
•Сфера применения, чувствительность к производственному штамму вируса.
28.Технология получения посевного материала и используемое оборудование. Микробиологический и химический контроль на данной стадии
При подготовке посевного материала необходимо пройти 3 стадии (на каждой стадии должны соблюдаться методы асептики и предотвращения заражения):
1)Подготовка и стерилизация оборудования и растворов
2)Приготовление посевного инокулята
3)Мероприятия по микробиологическому контролю
На первом этапе, мы подготавливаем всю необходимую нам лабораторную посуду (колбы, шпатели, пипетки, цилиндры и тд.). Они стерилизуются в автоклаве. Далее производят подготовку растворов и сред (фосфатный буфер, железо, магний, м.э и тд.), которые также стерилизуются.
Далее в ламинарном шкафу мы вносим в пробирку со скошенным агаром небольшое количество среды и петлёй смываем культуру с поверхности агара в колбу. Далее добавляем растворы и источник углерода (масла, глюкоза, фруктоза). И ставим на мешалку.
Во время подготовки инокулята микробиологический контроль проводят 2 раза. Первый после смыва музейной культуры в колбу, второй – перед посевом бактерий в ферментёр. Микробиологический контроль проводят методом посева в чашки петри на плотную питательную среду, предварительно при этом разводя культуру.
При необходимости проводят исследование био/химических показателей в инокуляте (концентрации азота, глюкозы, фруктозы, оптической плотности и тд.)
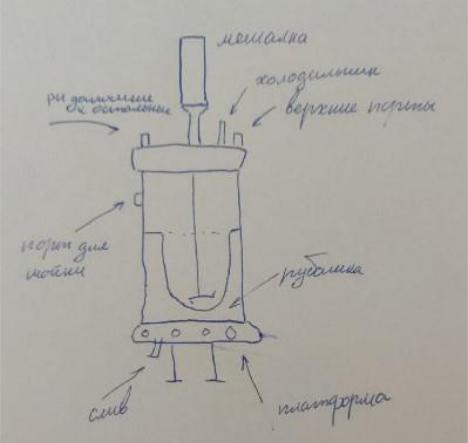
29. Устройство и эксплуатация ферментера. Основные параметры процесса биосинтеза и их контроль.
Эксплуатация. Программа BioSCADA Lab оборудование:
•термодатчик,
•pH-датчик,
•датчик растворённого кислорода,
•монометр,
•обороты мешалки,
•подача воздуха и питательных веществ,
•антипенная система.
30.Стерилизация ферментера, калибровка контрольно-измерительного
ианалитического оборудования. Технология стерильной подачи питательных растворов. Отбор и анализ проб, основные методики.
Для подготовки ферментера к процессу стерилизации, необходимо
провести следующие последовательные процедуры:
•помыть ферментер мыльным раствором с ополаскиванием дистиллированной водой;
•залить в ферментёр фосфатного буфера;
•поставить датчик pH, место присоединение кабеля закрыть колпачком;
•поставить датчик DO, место прикрепления кабеля закрыть фольгой;
•взять из ремкомплекта ферментера резиновую/силиконовую мембрану,
поставить в порт технологический и закрепить с помощью шестигранника на 2 мм;
•поставить пробоотборник;
•поставить воздушные фильтры PTFE 0.2 µm ø73 mm (воздух должен подаваться от направления надписи на фильтре) на систему подачи и выпуска воздуха;
•поставить на трипорт подачи питательных сред отрезки шлангов и обернуть фольгой;
•закрыть фольгой гнездо двигателя мешалки;
•закрыть зажимы на пробоотборнике;
•поставить ферментёр на стерилизацию в автоклав. Для предотвращения избыточного давления - гайки ферментёра завинтить не плотно;
•стерилизовать ферментер в автоклаве при давлении 1 атм., температуре
121°С, продолжительности 30 минут, после чего оставить остывать в автоклаве до комнатной температуры;
•извлечь ферментер из автоклава после остывания, предварительно закрутив гайки на крышке ферментера, и поставить на рабочую платформу.
Датчик pH калибруется по двум буферным растворам с известной величиной pH (4,00 и 7,00).
Для стерильной подачи во всех ферментационных системах предусмотрены перистальтические насосы, которые не позволяют осуществлять прямой контакт с подаваемыми питательными средами:
устанавливается шланг с иголкой, которая пробитием вставляется через стерильный вкладыш в верхний порт.
Для отбора пробы необходимо:
•подсоединить емкость для сбора пробы;
•открыть зажим перед шприцом и шприцом создать вакуум в емкости для сбора пробы;
•открыть зажим возле штуцера пробоотборника;
•после наполнения емкости, закрыть зажим возле штуцера пробоотборника, затем закрыть зажим перед шприцом;
•отсоединить емкость для сбора пробы от пробоотборника.
Анализ пробы включает в себя:
•Определение сухого веса;
•Входной контроль биомассы;
•Определение оптической плотности растущей культуры;
•Определение концентрации глюкозы в процессе ферментации;
•Определение содержание азота;
•Анализ выполняется не реже одного раза в два часа, аналогично стадии;
•Микробиологический контроль.