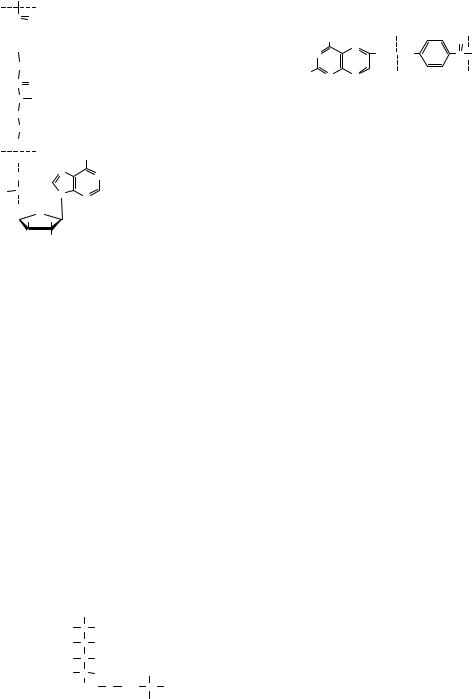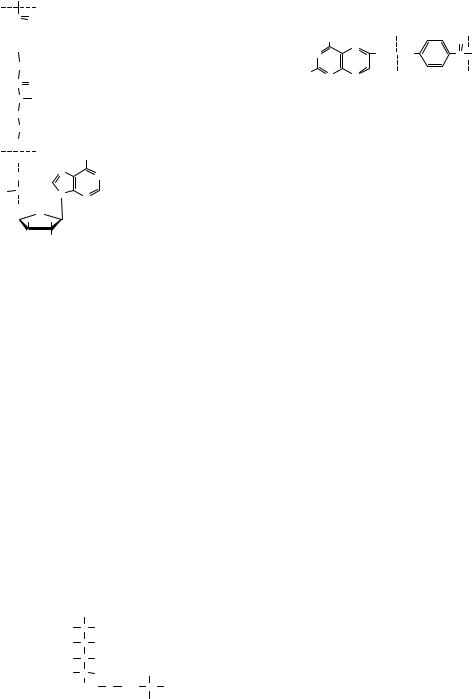|
|
|
HS |
|
|
|
|
|
|
|
|
|
|
|
|
|
Фолієва (птероїлглутамінова) кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
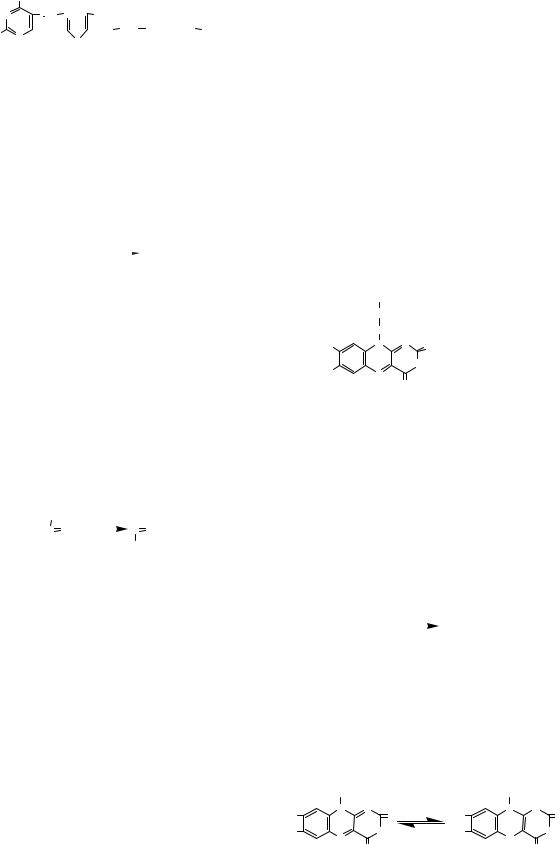
Хімічна структура. Фолієва кислота скла- |
|
|
|
|
|
|
|
|
|
|
|
|
|
Меркаптоетиламін |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дається із залишків птеридину, параамінобензе- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
нової та глутамінової кислот: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
N |
|
CH2 NH |
C |
NH CH CH2 CH2 COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пантотенова кислота |
H2N |
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N N |
|
|
|
|
|
|
|
|
|
|
|
C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Птеридин |
|
Параамінобен- |
|
|
Глутамінова |
|
|
|
HC |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
H3C |
|
|
C |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
зенова кислота |
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
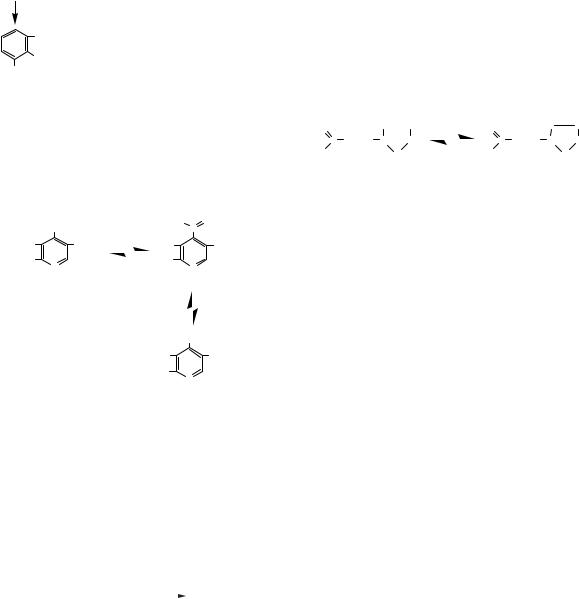
Коферментні функції. Фолієва кислота утво- |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
рює ряд біологічно активних сполук. Так, під |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
HO |
|
|
|
P |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
дією редуктаз, що містять відновлений НАДФ, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
N |
|
|
|
вона перетворюється на кофермент — тетрагідро- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
P |
|
|
|
|
O |
|
N |
N |
|
3-Фосфоаденозин- |
фолієву кислоту (ТГФК): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5′-дифосфат |
ФК + 2НАДФН + Н+ → |
ТГФК + 2НАДФ+. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Відновлення ФК до ТГФК полягає у при- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
P |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
єднанні чотирьох атомів Гідрогену в положеннях |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
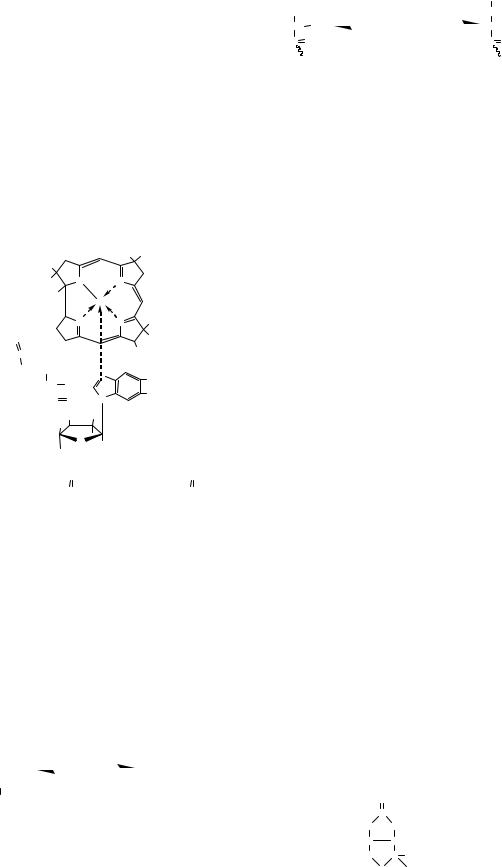
Коензим А |
|
|
|
|
|
5, 6, 7, 8. ТГФК як кофермент |
входить до скла- |
|
Отже, КоА бере участь у фундаментальних |
ду ферментів, що каталізують перенос одновуг- |
|
лецевих фрагментів (наприклад, метильних груп |
|
біохімічних процесах: окисне декарбоксилюван- |
(–СН3), гідроксиметильних груп (–СН2–ОН), |
|
ня α -кетокислот, окиснення і біосинтез вищих |
формільних груп та ін.). Приєднання цих фраг- |
|
жирних кислот, цикл трикарбонових кислот, біо- |
ментів до ТГФК є ферментативною реакцією ко- |
|
синтез ліпідів, стероїдних гормонів, гемоглобіну, |
валентного зв’язування їх із 5-им або 10-им ато- |
|
ацетилхоліну і т. ін. Добова потреба — 7–12 мг. |
мом Нітрогену або з обома атомами разом. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метил-ТГФК є донором метильних груп для |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
біосинтезу метіоніну з гомоцистеїну. Метіонін є |
|
Вітамін В15 (пангамова кислота) |
донором метильних груп для синтезу холіну, ти- |
|
Хімічна структура. Пангамова кислота — |
міну з урацилу, креатину, адреналіну. |
|
складний ефір глюконової та метильованої амі- |
Гідроксиметил-ТГФК є донором оксиметиль- |
|
них груп для синтезу серину з гліцину. |
|
нооцтової кислот. |
|
|
|
|
|
Форміл-ТГФК є донором формільних груп для |
|
Донатор метильних груп для утворення ме- |
|
біосинтезу пуринових нуклеотидів і т. ін. Наве- |
|
тил-ТГФК, яка через етап метил-кобаламіну бере |
дені дані свідчать про винятково важливу роль |
|
участь у біосинтезі метіоніну з гомоцистеїну (ос- |
фолієвої кислоти в обміні нуклеїнових кислот і |
|
танній у формі S-аденозилметіоніну забезпечує |
білків. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
процеси метилування). Міститься у печінці, |
Гіповітаміноз пов’язаний з порушенням ендо- |
|
дріжджах. Ефективний при жировій дистрофії пе- |
|
генного синтезу мікрофлорою кишечнику і |
|
чінки, |
гіпоксіях. |
|
|
|
|
|
всмоктування внаслідок гіпоацидних гастритів |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
і ентеритів, прийому сульфаніламідів, антибіо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тиків, через що розвиваються макроцитарні, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гіпохромні й гіпопластичні анемії, агранулоци- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
C H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тоз, |
тромбоцитопенія. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Токсичність великих доз фолієвої кислоти |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C OH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
вища, ніж інших вітамінів групи В. Так, розви- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
O |
CH |
N+ CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
2 |
3 |
ток алергічних реакцій пов’язаний з участю |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТГФК в утворенні гістаміну з гістидину. Диспеп- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пангамова кислота |
тичні явища пов’язані з активацією мікрофлори |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кишечнику. Стимуляція росту пухлин пов’язана |
|
Біологічна дія. Пангамова кислота містить ме- |
з участю ТГФК в обміні нуклеотидів, який у пух- |
|
тильні групи, які можуть використовуватися при |
линах є посиленим. |
|
|
|
|
|
|
|
|
|
|
|
|
синтезі метіоніну, холіну, креатину й ін. |
Добова потреба — 0,5 мг. Фолієва кислота |
|
Відомо, що вітамін В15 стимулює енергетичний |
міститься у листі салату, петрушки, кропу, може |
|
обмін клітини, активуючи ферменти піруват- і |
синтезуватися мікрофлорою кишечнику, іншими |
|
сукцинатдегідрогеназу, а це сприяє біосинтезу |
мікроорганізмами тільки у разі наявності ПАБК. |
|
АТФ. У вигляді кальцієвої солі використовуєть- |
Глутамінова кислота, сполучаючись із фолієвою |
|
ся в клініці. Гіповітаміноз досліджений недостат- |
кислотою, затримує всмоктування надлишку її у |
|
ньо. Добова потреба |
не встановлена. |
ШКТ. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|