|
|
|
|
|
|
|
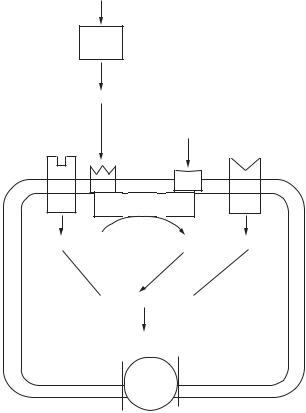
Трипсин |
|
|
|
рювання, аналогічне поліневриту (бері-бері) у |
|
|
|
|
|
|
|
|
|
|
|
Пепсин (шлунок) |
Хімотрипсин |
|
Амінокислоти |
людини. При додаванні до очищеного рису ри- |
|
Білки |
|
|
Карбокси- |
|
(тонкий |
сових висівок у людей і курчат захворювання не |
|
|
|
|
|
|
|
пептидази |
|
|
кишечник) |
розвивалося, а виготовлений із висівок рису екс- |
|
|
|
|
|
|
|
Амінопептидази |
|
|
|
|
|
|
|
|
|
тракт мав лікувальний ефект у людей, хворих на |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бері-бері. Ці спостереження довели, що в оболонці |
|
Білки в шлунку і тонкiй кишцi пiддаються |
рису містяться якісь речовини, необхідні для нор- |
|
гідролізу до амінокислот, що всмоктуються в ки- |
мальної життєдіяльності організму. У 1911 р. |
|
шечнику. |
|
|
|
|
|
|
польський учений К. Функ виділив у крис- |
|
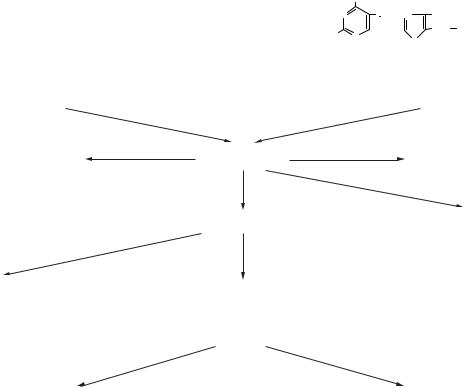
Нуклеїновi кислоти під дією ферментів нукле- |
талічній формі з рисових висівок речовину, що |
|
аз тонкого кишечнику і підшлункової залози |
охороняла від розвитку бері-бері. При аналізі |
|
розщеплюються до олiгонуклеотидiв і полiнук- |
хімічного складу цієї речовини вчений виявив |
|
леотидiв, а далі — до мононуклеотидiв: |
аміногрупу. З огляду на важливе значення подіб- |
|
|
|
|
|
|
|
|
|
|
|
|
|
них речовин для життя й наявність аміногрупи |
|
|
|
|
|
|
|
|
|
|
|
Олігонуклеотиди |
в складі виділеної ним речовини, К. Функ запро- |
|
|
|
|
|
|
|
|
|
|
|
|
Нуклеїнові кислоти |
|
Ендонуклеази |
|
понував називати ці невідомі речовини «вітамі- |
|
|
|
нами», що означає «аміни життя». Згодом ви- |
|
|
|
|
|
|
|
|
|
|
|
Полінуклеотиди |
|
|
|
|
|
|
|
|
|
|
|
явилося, що деякі з вітамінів не містять аміногру- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пу і взагалі азот, однак термін «вітаміни» міцно |
|
Мононуклеотиди під дією ферментів тонкої |
вкорінився в біології та медицині. |
|
кишки нуклеотидаз розпадаються на нуклеози- |
Вітаміни — це різноманітні за хімічною струк- |
|
ди і неорганічний фосфат: |
|
|
|
турою речовини. Більшість із них швидко руйну- |
|
|
|
|
|
|
|
|
|
|
|
|
|
ються під дією високих температур, сильних кис- |
|
Нуклеотид |
Нуклеозидаза |
Нуклеозид + Н3РО4 |
лот і лугів, іонізуючого випромінювання та |
|
|
|
|
|
|
інших факторів, що необхідно враховувати при |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
зберіганні та консервуванні продуктів, виготов- |
|
Нуклеозиди далі розщеплюються під дією нук- |
ленні лікарських форм, які містять вітаміни. |
|
леозидаз: |
|
|
|
|
|
|
Більшість вітамінів синтезуються не в організмі |
|
|
|
|
Нуклеозидаза |
|
|
|
людини, а рослинами і кишковими бактеріями, |
|
|
|
|
|
|
|
тому джерелом вітамінів для людини є продукти |
|
Нуклеозид |
|
|
|
|
|
Азотиста основа + Пентоза |
|
|
|
|
переважно рослинного походження. Деякі вітамі- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ни (РР, D, К) утворюються в організмі людини в |
|
Однак внаслідок малої активності нуклеози- |
таких незначних кількостях, які не забезпечують |
|
даз основними продуктами, що всмоктуються че- |
потреб організму. Вітаміни А i D людина одер- |
|
рез слизову оболонку тонкої кишки, є мононук- |
жує разом із продуктами тваринного походжен- |
|
леотиди, які включаються в тканинний обмін. |
ня (молоко, масло, риб’ячий жир), інші містяться |
|
|
|
|
|
|
|
|
|
|
|
|
|
у рослинах (фолієва кислота). Отже, вітаміни — |
|
|
|
|
|
|
|
|
|
|
|
|
|
це харчові речовини, наявні в невеликих кілько- |
|
|
|
|
|
|
|
|
|
|
|
|
|
стях у їжі, вони забезпечують нормальний пе- |
|
16.3. ВІТАМІНИ ЯК КОМПОНЕНТИ |
ребіг біохімічних і фізіологічних процесів шляхом |
|
участі в регуляції обміну цілісного організму. |
|
ХАРЧУВАННЯ: ЕКЗОГЕННІ |
|
|
|
Незамінні амінокислоти, деякі рослинні ненаси- |
|
ТА ЕНДОГЕННІ ГІПОВІТАМІНОЗИ. |
|
чені жирні кислоти (лінолева, ліноленова й ін.) |
|
ВОДОРОЗЧИННІ (КОФЕРМЕНТНІ) |
також є незамінними для людини, оскільки вони |
|
ВІТАМІНИ |
|
|
|
|
|
|
не синтезуються в організмі. Однак в останньо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
му випадку згадані речовини не належать до |
|
|
|
|
|
|
|
|
|
|
|
|
|
вітамінів, оскільки вітаміни відрізняються від |
|
У 1880 р. російський учений М. І. Лунін про- |
інших органічних речовин двома характерними |
|
вів експериментальні дослідження на двох групах |
ознаками: не включаються в структуру тканин; |
|
мишей. Одна група одержувала штучно виго- |
не використовуються організмом як джерело |
|
товлене молоко з білків (казеїну), жирів, молоч- |
енергії. |
|
ного цукру, солей і води. Друга група мишей |
При недостатньому надходженні в організм |
|
одержувала свіже молоко. Перша група тварин |
вітамінів, їх повній відсутності у споживаній їжі |
|
загинула, а друга залишилася здоровою і нор- |
або порушенні їхнього всмоктування, транспор- |
|
мально розвивалася. На підставі цих досліджень |
ту тощо розвиваються ті чи інші захворювання. |
|
учений дійшов висновку, що, крім білків, жирів, |
Хвороби, що виникають при повній відсутності |
|
молочного цукру, солей і води, тварини мають |
в їжі або повному порушенні засвоєння якого- |
|
потребу в якихось ще невідомих речовинах, не- |
небудь вітаміну, називаються авітамінозами. |
|
обхідних для життя. |
|
|
|
|
|
|
Хвороби, що виникають через недостатнє над- |
|
У 1886 р. голландський лікар Х. Ейкман, який |
ходження вітамінів з їжею або погане їх засвоєн- |
|
працював в’язничним лікарем на о. Ява, де ос- |
ня, називаються гіповітамінозами. Гіпо- й авіта- |
|
новним продуктом харчування людей був полі- |
мінози можуть бути первинними (екзогенними) й |
|
рований (очищений) рис, помітив, що у курчат, |
вторинними (ендогенними). Первинні гіпо- й аві- |
|
які одержували полірований рис, виникло захво- |
тамінози виникають при недостатній або повній |