Материал: Біохімічна відповідь олігодендроцитів до ішемічного стану
Розуміння механізмів ішемічного ушкодження в природних умовах в моделі ішемії є необхідним кроком на шляху до розробки терапевтичних втручань. У фокальній ішемії людини, інфаркти часто пов'язані з ураженням білої речовини, і ретельне вивчення клітинного пошкодження в білій речовині має вирішальне значення в моделях інсульту тварин. Попередні дослідження вивчали відносну зміні експресії олігодендроцит- і мієліноспецифічних маркерів, але ці епітопи можуть бути тимчасово втрачені, або замасковані при патологічних станах. Навіть у здорової тканини, візуалізація антитіл до цих антигенів, як правило, обмежена або в тілі клітини або товстим шаром мієліну, і може не показувати всіх змін у морфології олігодендроцитів, які відбуваються у відповідь на пошкодження. Трансгенні миші, які продукують олігодендроцитарні клони клітин з конкретними флуоресцентними мітками, дозволяють повністю візуалізувати морфологію олігодендроцитів, і надають розуміння ішемічного ушкодження цих клітин. Тим не менш, в лініях трансгенних тварин, отриманих нині, візуалізація флуоресцентних міток може бути вираженою в клітинах-попередниках, а не лише зрілих олігодендроцитах. Крім того, високі рівні експресії в трактах білої речовини ускладнюють розмежування окремих процесів мієліногенезу, і, отже, обмежують вимірювання аналізів, які нечутливі до тонких змін у морфології [50].
Мало що відомо про часову залежність дегенеративних змін або регенеративного потенціалу білої речовини від тривалості дії фактору індукції ішемічного ураження. У цьому дослідженні вчені використовували лентивірусний вектор спеціально для зрілої мієлінпродукуючої популяції олігодендроцитів щурів в білій речовині. Направляючи LV-MBP-EGFP ін'єкцією у бічне мозолисте тіло, дослідники отримали зону поширення проліферуючих клітин при реперфузії. Конфокальна мікроскопія застосовувалася для того, щоб більш точно дослідити часовий хід відновлення білої речовини після MCAO. Використання трифеніл тетразоліум хлориду (TTC) та фарбування барвником LFB підтвердили, що ця модель ішемії провокує виникнення інфарктів, пов'язаних з ушкодженням білої речовини, як повідомлялося раніше. TTC-забарвлені тканини використовували для документування загальної площі інфаркту, а потім згодом обробляли для візуалізації травми білої речовини на клітинному рівні. Це важливо, оскільки MCAO може індукувати появу різних за розміром інфарктів, навіть якщо вимірювання потоку крові головного мозку послідовно знижується під час оклюзії. Тут використання ТТС дозволяє вченим стверджувати, що зменшення кількості GFP(+)-олігодендроцитів в бічному мозолистому тілі починається вже з 24-48 годин реперфузії після інсульту. Щодо розподілу GFP(+)-олігодендроцитів, які спостерігаються в білій речовини, дослідники також спостерігали залежне від часу зменшення числа тих клітин, що уздовж медіально-бічної зони мозолистого тіла, при майже повній відсутності в зовнішній зоні через 48 годин після ішемії [48].
Малоймовірно, що зниження експресії GFP відбувалося через неактивність промотору MBP, оскільки рівень транскрипції MBP збільшується після розвитку ішемії. GFP(+)-олігодендроцити, що вижили, були виявлені в регіонах ішемічної загибелі клітин, які мали у своєму складі маркер TUNEL (трансфераза термінального приєднання дезоксиуридинтрифосфату). Враховуючи ці дані, то малоймовірно, що зниження GFP(+)-клітин пригнічується активністю промотору MBP.
Широкий некроз в смугастому тілі (corpus striatum) і корі є визначальною рисою серцевини інфаркту в цій моделі ішемії, тому цілком імовірно, що GFP(+)-олігодендроцити піддаються клітинній загибелі, що призводить до втрати або деградації GFP. Тут вчені прагнули вивчити олігодендроцити ближче до межі ішемізованої зони, де може бути більший потенціал клітин для відновлення. Тому що варіабельність в розмірах інфаркту є основною рисою цієї експериментальної моделі, дослідники не могли виключити можливість того, що деякі клітини, проаналізовані в даному дослідженні, загинули саме в центральній зоні (ядрі) інфаркту [48].(+)-олігодедроцити, що вижили, характеризувалися зниженням мієліноутворюючого потенціалу. При цьому були виявлені значні зони фрагментації мієлінових мембран на 24- і 48-у години після реперфузії. Живі GFP(+)-олігодедроцити характеризувалися також TUNEL(-)-показником та не мали пікнотичних ядер. Ці результати показують, що дегенерація процесів мієлінізації (мієліногенезу) може передувати загибелі олігодендроцитів [48]. Це переконливі перспективи у світлі доказів того, що на цей процес індукують високі концентрації глутамату. Показано, що за умов ішемії експресія субодиниць глутаматних рецепторів спостерігається саме в зонах демієлінізації [51].
Збереження морфології тіла клітини під час мієлінової дегенерації представляє інтригуючу можливість того, що ремієлінізація відбувається завдяки структурному відновленню раніше пошкоджених олигодендроцитів. На перший тиждень реперфузії після осередкової ішемії, спостерігалося відновлення інтактних процесів мієлінізації і кількості GFP(+)-олігодендроцитів в ішемізованій області білої речовини. Проте, як було зазначено раніше, порушення мієліногенезу спостерігалося через 24-48 годин після ішемії. На додаток до відновлення структури олігодендроцитів спостерігалося і відновлення GFP(+)-клітин після ішемії білої речовини мозолистого тіла (corpus callosum). Репопуляціі GFP(+)-олігодендроцитів, візуалізовані в цьому дослідженні, швидше за все, походять від клітин-резидентів вже в білій речовині, а не клітин, що мігрують в районах з сірою речовиною.
Використання бромодеоксиуридинової
реєстрації (BrdU-реєстрації) дозволило відстежити реакцію проліферуючих клітин
протягом одного тижня після реперфузії, щоб визначити, диференціюються вони в
GFP(+)-олігодендроцити, чи ні. Вчені знайшли численні BrdU-клітини в тій же
області ішемічного ураження білої речовини, де були знайдені регіони збільшених
популяцій GFP(+)-олігодендроцитів [50]. Навіть одного імпульсу BrdU, враховуючи
24 годин після травматизації спинного мозку, було достатньо, щоб відстежувати
новостворені олігодендроцити через тиждень [50, 53]. В даний час широко
визнається, що дорослі OPCs несуть відповідальність за ремієлінізацію аксонів
після ішемічного ушкодження. У моделях демієлінізації було добре показано, що
OPCs реагують на втрату олігодендроцитів проліферацією і диференціацією в
мієілноутворюючі олігодендроцити (рис. 1.4) [48].
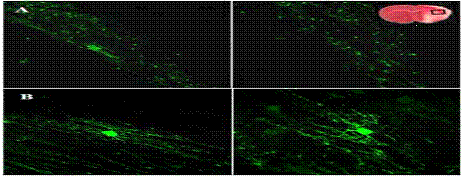
Рис. 1.4 Стан олігодендроглії в ішемізованій зоні мозку: А - на 24 год після розвитку ішемії, В - через 1 тиждень після ішемії (клітина-попередник OPC дає початок зрілому олігодендроциту). На рис. зверху справа показано уражену ішемією ділянку мозку
Команда МакАйвер та інші дослідники
наводять докази, що підтверджують здатність до регенерації білої речовини, яке
залежить від кількості відновлених клітин і збереження процесів мієліногенезу.
Лентівірусні вектори не тільки підвищують візуалізацію морфологічних змін
олігодендроцитів у відповідь на пошкодження, а й забезпечують ефективний метод
для оцінки потенційних захисних ефектів нової трансгенної експресії. Це може
бути корисним підходом для діагностики багатьох захворювань, при яких активація
процесів ремієлінізації ушкоджених після травми ділянок мозку є терапевтичною
метою [48].
1.3.5 Енергетичний дефіцит олігодендроцитів за умов ішемії
Різні форми церебральної ішемії корелюють з фазними змінами вмісту ATФ <#"867912.files/image006.gif">
Рис. 3.1 Вміст основного білка
мієліну в різних відділах головного мозку 1- та 3-місячних щурів: n
= 6; *р<0,05 відносно 1-місячних тварин
У всіх вищевказаних відділах мозку новонароджених (1-денних) тварин наявні лише слідові концентрації досліджуваного білок, оскільки процеси мієлінізації нервових волокон розпочинаються лише після народження. Тому рівень ОБМ у цей період дуже низький (див. рис. 3. 1).
Експериментальні дані, отримані для 1- та 3-місячних щурів, наступні: у тварин 2-ї групи - 0,630±0,100 мкг/100 мг тканини (гіпокамп), 2,00±0,40 мкг/100 мг тканини (таламус) та 4,550±0,300 мкг/100 мг тканини (мозочок). Тварини 3-ї групи мали наступний розподіл білка у мозку: 2,31±0,70 мкг/100 мг тканини (гіпокамп), 2,09±0,60 мкг/100 мг тканини (таламус) та 3,08±0,60 мкг/100 мг тканини (мозочок) відповідно.
Згідно з отриманими результатами, концентрація ОБМ у гіпокампі та таламусі 1-місячних тварин є нижчою, ніж у 3-місячних. Інакше кажучи, рівень ОБМ у гіпокампі 3-місячних збільшується у 3-4 рази. Таке нерівномірне збільшення рівня досліджуваного протеїну пояснюється процесами швидкої мієлінізації нервових волокон у гіпокампу. За літературними даними, у мозку 1-місячних щурів спостерігається підвищена синтетична активність олігодендроцитів [24]. Специфічні фактори транскрипції підвищують експресію генів основного білка мієліну [22, 25].
У таламусі не спостерігається достовірних змін концентрації білка. У таламусі процеси мієлінізації відбуваються повільно. Загальний пул ОБМ у мембранній фракції мало змінюється. Порівнюючи з гіпокампом, слід відзначити, що найінтенсивніше процеси мієлінізації відбуваються у гіпокампі, якщо порівнювати з іншими відділами головного мозку щурів (див. рис. 3.1).
3.2
Загальний протеїн протягом раннього постнатального
розвитку
Отримані експериментальні вказують
на тенденцію до збільшення вмісту загального протеїну (ЗП) у мембранній фракції
мозочка зі збільшенням віку тварин (рис. 3.2).
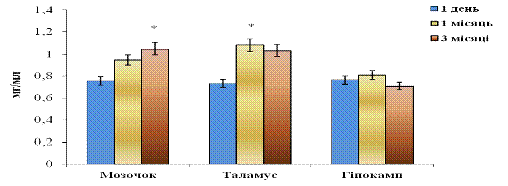
Рис. 3.2 Вміст загального протеїну (ЗП) у різних відділах головного мозку 1-денних, 1- та 3-місячних щурів: n = 6; *р<0,05 відносно 1-денних тварин
Дослідження загального пулу мембранних протеїнів у мозку тварин визначило тенденцію для всіх відділів мозку. Концентрація загального протеїну у мозочку складає: для одноденних тварин - 0,76±0,04 мг/мл, 1-місячних - 0,95±0,14 мг/мл та 3-місячних - 1,05±0,12 мг/мл відповідно. Звідси бачимо, що вміст білка підвищився у другій групі тварин у 1,3 рази (на 25,7%) при порівнянні з одноденними тваринами; у 3-групі спостерігається максимальний вміст протеїну (підвищується на 10,4% у порівнянні з 1-місячними).
Подібне підвищення білкової експресії свідчить про те, що у мозочку починається розвиток складних міжнейронних зв’язків, які відповідають за рухову діяльність тварин, тобто регулюють координацію рухів, орієнтацію у просторі, вивчення і закріплення тваринами складних рухових механізмів протягом розвитку. При цьому активно йдуть процеси синапто- та нейрогенезу, наслідком яких є підвищення синаптичної пластичності моторних сигнальних шляхів.
Для таламусу концентрація ЗП наступна: одноденні тварини - 0,73±0,06 мг/мл, 1-місячні - 1,08±0,11 мг/мл, 3-місячні - 1,03±0,09 мг/мл відповідно. На основі цих даних бачимо, що в другій групі ЗП зростає у 1,5 рази (на 47,1%), що свідчить про високу інтенсивність нейрогенезу. Це найвищий показник ЗП у порівнянні з іншими відділами головному мозку. Фактично процеси нейрогенезу у таламусі тривають протягом усього життя тварин.
На момент досягнення тваринами 3-місячного віку концентрація ЗП дещо знижується на 4-5%. При цьому вміст білків коливався у межах нормальної варіації. Такі дані не вказують на достовірні зміни ЗП у таламусі головного мозку щурів 3-ї групи, оскільки це - результат нормальних вікових змін. При цьому не спостерігається яких-небудь порушень зі сторони сприйняття тваринами як зорових, слухових чи тактильних подразників. Концентрація ЗП та пов'язаний з ним розвиток ЦНС в таламусі зберігає відносну стабільність, оскільки постійно відбувається сприйняття дії подразників та формування відповідних реакцій на них [15].
Для мембранних фракцій, отриманих з гіпокампу кори великих півкуль мозку, вміст ЗП розподілений таким чином: одноденні тварини - 0,76±0,16 мг/мл, 1-місячні - 0,81±0,05 мг/мл та 3-місячні - 0,71±0,07 мг/мл відповідно. Згідно з отриманими результатами, вміст загального протеїну у гіпокампі новонароджених щурів є меншим, ніж у 1-місячних, тобто концентрація ЗП за місяць зросла на 6,2%. В останніх концентрація ЗП у гіпокампі у порівнянні з 3-місячними щурами переважає майже на 12,5%. Спостерігається незначне падіння експресії білка. При цьому коливання концентрації ЗП у мозку не завжди супроводжуються помітним погіршенням соматичного стану тварин, але одночасно можуть виникати різноманітні порушення інтегративної функції мозку, залежно від ступеня коливання вмісту білків.
Синаптична пластичність гіпокампу з цього часу трохи знижується. Це, у свою чергу, може впливати на розвиток лімбічної системи мозку, однак при цьому зміцнюються процеси консолідації пам'яті завдяки елімінації старих між нейронних зв’язків та утворенні нових. Тому експресія білка після 3-місячного віку знову зростає.
Важливе значення для формування синаптичної пластичності у ході функціонування нервової системи мають нервовоспецифічні інтегральні білки мембран нейронів та компоненти міжклітинного матриксу (зокрема, його глікозаміноглікан-зв’язуючі компоненти). Ці білки, як правило, є трансмембранними і складаються з трьох областей: внутрішньоклітинного домену, який взаємодіє з цитоскелетом, трансмембранного домену та позаклітинний домену, який взаємодіє з іншою молекулою клітинної адгезії. Вони приймають участь в розпізнаванні і зв'язуванні різних позаклітинних лігандів [61].
Завдяки взаємодії з компонентами
міжклітинного матриксу мембранні білки впливають на організацію клітини та її
поведінку [62]. Сьогодні велика увага приділяється не тільки вивченню здатності
нейроспецифічних білків регулювати міжклітинні взаємодії, а також їх впливу на
структурну організацію нейронів та гліальний елементів.
3.3
Загальний протеїн за умов ішемії
Церебральна ішемія є однією з найрозповсюдженіших патологій головного мозку. Проблема гострої та хронічної ішемії мозку має надзвичайно важливу медико-соціальну значимість. Ріст розповсюдженості судинних захворювань, зафіксований протягом останніх років, зумовив збільшення частоти гострих порушень мозкового кровообігу [63].
Найбільш грізним ускладненням церебральної ішемії є розвиток ішемічних інсультів, які складають 80-85% від загальної кількості інсультів [64]. Значна розповсюдженість - з одного боку, та той факт, що саме гострі порушення мозкового кровообігу за ішемічним типом найкраще піддаються терапії за умов своєчасно розпочатого лікування - з іншого [65], робить поглиблене дослідження патогенетичних ланок ішемічних ушкоджень мозку актуальним і перспективним щодо розробки та удосконалення патогенетичних засобів їх корекції.
Крім численних морфологічних, біохімічних та електрофізіологічних змін у тканині самого мозку, церебральна ішемія викликає загальну нейрогормональну відповідь, яка є компонентом реакції єдиної нейроімуноендокринної системи та впливає на різні біохімічні показники ЦНС, зокрема, на розподіл рівня загального протеїну у головному мозку ссавців. Саме ця реакція забезпечує метаболічну основу компенсаторно-пристосувальних змін, від яких багато в чому залежить перебіг ішемічних ушкоджень нервової тканини [66]. Вираженість стресорних білково-нейрогормональних перебудов відображає тяжкість ішемії, впливає на перебіг патологічного процесу та має прогностичне значення [67]. Це виступає показником важкості ішемії, в той же час впливає на перебіг патологічного процесу та разом із іншими чинниками визначає його наслідки.
Однак зусилля більшості дослідників проблеми ішемії зосереджені на вивченні місцевих, церебральних її проявів, і лише поодинокі роботи присвячені вивченню білкового обміну за цих умов. Зокрема, незважаючи на досить давно встановлений факт впливу катехоламінів на перебіг та наслідки ішемічного ушкодження мозку, конкретні патогенетичні ланки, на рівні яких ці ефекти реалізуються, не вивчені, а існуючі дані, сповнені протиріч. Тому питання про білковий обмін при церебральній ішемії залишається відкритим, що свідчить про актуальність нашого дослідження.