Материал: Біохімічна відповідь олігодендроцитів до ішемічного стану
Біохімічна відповідь олігодендроцитів до ішемічного стану
Міністерство освіти і науки україни
Дніпропетровський національний університет імені Олеся Гончара
Факультет біології, екології та медицини
Кафедра
біофізики та біохімії
ДИПЛОМНА РОБОТА МАГІСТРА
на тему: «БІОХІМІЧНА ВІДПОВІДЬ ОЛІГОДЕНДРОЦИТІВ ДО ІШЕМІЧНОГО СТАНУ»
Виконав: студент VI курсу, групи БХ-14м
спеціальності 8.04010205 «Біохімія»
Жданкін А.Є.
Керівник д.б.н., проф. Ушакова Г. О.
Рецензент к.б.н., проф. Мурзін
О. Б.
Дніпропетровськ 2016
РЕФЕРАТ
Біохімічна відповідь олігодендроцитів до ішемічного стану
Дипломна робота магістра містить: 62 ст., 17 рис., 74 джерела.
Об'єкт дослідження: головний мозок білих щурів лінії Вістар. Предмет дослідження - cтан мієлінової оболонки головного мозку гризунів.
Мета роботи: вивчити стан мієлінової оболонки в головному мозку ссавців на початкових етапах постнатального розвитку; оцінити біохімічну відповідь олігодендроглії до ішемічного стану мозку.
Методи: гомогенізація різних відділів головного мозку; отримання мембранної та цитозольної фракцій шляхом диференціального центрифугування гомогенатів мозку; визначення вмісту основного білка мієліну за допомогою непрямого імуноферментного аналізу; визначення вмісту загального протеїну за методом Бредфорд; статистичні методи обробки даних.
Одержані результати та їх новизна. Вперше досліджено вплив глобальної ішемії на розподіл основного білка мієліну у різних відділах головного мозку. Оцінено вплив ізадрину та пітуїтрину на вміст загального протеїну у цитозольних фракціях мозку. Вивчено розподіл основного білка мієліну протягом раннього постнатального розвитку.
Встановлено, що за умов глобальної ішемії у всіх відділах головного мозку, окрім кори великих півкуль, спостерігається тенденція до зниження вмісту загального протеїну та основного білка мієліну, що свідчить про демієлінізацію нервових волокон та зниження функціональної активності олігодендроглії. Нейропротекторні препарати Корвітин та альфа-кетоглутарат не повністю відновлюють уражені ішемією ділянки мозку. Результати дослідження можуть бути застосовані при терапії ішемічних уражень мозку різної етіології.
Ключові слова: основний білок мієліну, загальний протеїн, олігодендроцити, ішемія, ранній постнатальний розвиток.
RESUME
' biochemical response to the
ischemic condition's work contains 62 p., 17 fig. and 74 sources.of study:
Wistar rat brain.
The subject of study is a state of the myelin sheath in the rodent brain.of the
work: to study stage of myelin sheath in the mammal brain during the early
stages of postnatal development; to evaluate
a biochemical response of oligodendroglia to the ischemic brain condition.:
brain homogenization; membrane and cytosolic fractions' receiving by
differential centrifugation of brain homogenates; MBP- determining using
indirect ELISA; determination of total protein by the Bradford method;
statistical methods of data processing.results and their novelty. At first time
the impact of global ischemia on myelin basic protein distribution in different
parts of the brain was studied. The effects of Isadrinum and Pituitrinum on
total protein content in brain cytosolic fractions were evaluated. The
distribution of myelin basic protein during the early postnatal development was
indicated.tendency to reduction of total protein and myelin basic protein under
global ischemia conditions was established in the different parts of brain,
besides the cerebral cortex. It suggests the demyelination of nerve fibers and
reduction of oligodendroglial functional activity. Neuroprotective drugs,
Corvitin and 2-oxoglutarate
don't fully restore the affected brain parts after the
ischemia. Results of the study can be applied in the treatment of ischemic
brain lesions of various etiologies.words: myelin basic protein, total protein,
oligodendrocytes, ischemia, early postnatal development.
ВСТУП
Мієлінова оболонка - це комплекс ліпідних та білкових компонентів, утворений мембранами гліальних клітин, сконцентрованих навколо аксонів нейронів. Відкриття мієліну приписують видатному вченому німецькому Рудольфу Вірхову (1854 р.), який використовував методи світлової мікроскопії для вивчення структури тваринних тканин. Детальне вивчення мієлінової оболонки аксонів дозволило з'ясувати механізми процесу передачі нервових імпульсів. Функціями мієлінової оболонки є: прискорене проведення нервового збудження, побудова опорного молекулярного матриксу аксонів та забезпечення процесів їх трофічного росту, а також підтримка сталості систем міжклітинної комунікації [1]. Різні патологічні стани нервової системи або усього організму в цілому можуть суттєво порушувати структуру мієлінової оболонки.
Мета дипломної роботи магістра - вивчити стан мієлінової оболонки у головному мозку ссавців на початкових етапах постнатального розвитку; оцінити біохімічну відповідь олігодендроглії до ішемічного стану мозку. Об'єктом дослідження був головний мозок щурів. Предмет дослідження: стан мієлінової оболонки головного мозку гризунів.
Згідно з поданою метою поставлено
такі завдання: проаналізувати літературні дані, в яких розглядається біохімічна
відповідь олігодендроцитів за умов ішемічного ушкодження мозку гризунів;
визначити кількісні показники основного білка мієліну та загального протеїну у
різних відділах головного мозку щурів на ранніх етапах постнатального розвитку;
оцінити рівень загального протеїну та основного білка мієліну за ішемічного
стану мозку гризунів та при введенні терапевтичних препаратів - Корвітину та
альфа-кетоглутарату.
1. ОГЛЯД ЛІТЕРАТУРИ
1.1
Структура та функції мієліну
Мієлінізація нервових волокон ЦНС - динамічний процес, в основі якого лежить багаторівнева координація проліферації і диференціації клітин-попередників (OPCs) в зрілі олігодендроцити. Ці процеси необхідні для побудови мієлінових оболонок навколо аксонів нейронів, що, в свою чергу, служить умовою для забезпечення швидкої стрибкоподібної нервової провідності. Розкриття механізмів і молекулярних посередників мієлінізації служить важливою ланкою для розуміння біології нейро-гліальних взаємодій і має важливе практичне значення при лікуванні демієлінізуючих розладів ЦНС [2].
Рентгеноструктурний аналіз та електронна мікроскопія внесли свій внесок у вивчення структури мієлінових оболонок (мієліну). Виняткова властивість цих мембран полягає в тому, що їх формування здійснюється шляхом спірального обвиття відростків олігодендроглії в ЦНС і шванноцитів у ПНС навколо аксонів нервових клітин. За даними електронної мікроскопії у структурі мієліну виділяють суцільні концентрично розташовані темні лінії, відокремлені одна від одної світлими проміжками. Подвійна мембрана клітини декілька разів спірально закручується навколо аксона. Темні лінії утворюються при злитті внутрішніх листків клітинної мембрани, а світлі - зовнішніх. Внутрішні листки складаються з ліпідів, а зовнішні - з білків.
Ліпіди мієліну представлені фосфоліпідами, гліколіпідами і холестеролом. Вони побудовані за єдиним планом, мають гідрофобний компонент («хвіст») і гідрофільну групу («голівку»). На частку холестеролу відводиться близько 28%, 43% - на фосфоліпіди і 29% становлять гліколіпіди (галактоліпіди).
За допомогою рентгеноструктурного
аналізу тканин головного мозку щурів досліджено білкові компоненти мієліну (29
білків). Докладно вичені основний білок мієліну (myelin
basic protein
або MBP),
протеоліпідний білок, мієлін-асоційований глікопротеїн (рис. 1. 1), конексин 32
та периферичний мієліновий білок [3].
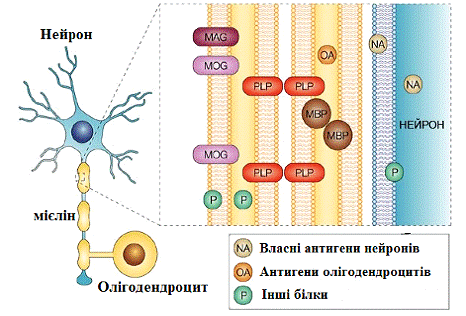
Рис. 1.1 Білки мієліну: MAG
- мієлін-асоційований глікопротеїн; MOG мієлін-олігодендроцитарний
глікопротеїн; PLP
- протеоліпідний білок (ліпофілін); MBP
- основний білок мієліну (ОБМ)
Процеси утворення мієлінової
оболонки у центральній та периферичній нервовій системі мають певні
відмінності. При формуванні мієліну ЦНС один олігодендрогліоцит має зв'язки з
декількома сегментами мієліну кількох аксонів; при цьому до аксона приєднується
відросток олігодендрогліоциту, розташованого на деякій відстані від аксона, а
зовнішня поверхня мієліну контактує з позаклітинним простором. Шванівська
клітина при утворенні мієліну ПНС формує спіральні пластинки мієліну та
відповідає лише за окрему ділянку оболонки між перехватами
<#"867912.files/image002.gif">
Рис. 1.2 Загальна схема HIF-1α-опосередкованої
демієлінізації: 1 - гіпоксія-індукований фактор; 2 - зв'язування HIF-1α
з рецептором і транспорт у цитоплазму; 3 - транспорт до ядра; 4 - транскрипція
мРНК мієлінових протеїназ; 5 - трансляція; 6 - дозрівання ферменту; 7 -
екзоцитоз ферменту з клітини з наступним руйнуванням мієліну
Загибель олігодендроцитів за умов
ішемії також може відбуватися за рядом механізмів, серед яких порушення іонного
гомеостазу, приток кальцію у внутрішньоклітинний простір,
мітохондріально-опосередкована ініціація клітинної загибелі та зниження
аксонального транспорту. Внаслідок цього демієлінізацію можна розглядати як
патологічну реакцію у нервовій системі на рівні «глія-мієлін-нейрональний
комплекс» у відповідь на вплив ішемії чи інших ендо- та екзогенних ушкоджуючих
факторів [11].
1.3.3 Вплив ішемії мозку на експресію основного білка мієліну
Основний білок мієліну (ОБМ) - структурно-функціональний маркер мієлінової оболонки (мієліну) ЦНС. ОБМ входить до складу серозної (білкової) лінії мієліну, утворюючи при цьому тісні інтегративні комплекси зі сфінголіпідами та стабілізує аксони нервових клітин [11]. Протеїн визначає специфічність нервової тканини [40], оскільки зниження його експресії індукує порушення перебігу мієлінізуючих процесів у мозку [12]. Коливання концентрації ОБМ в різних відділах головного мозку - важливий діагностичний показник багатьох патологічних станів ЦНС, зокрема церебральної ішемії.
Експерименти, проведені з використанням головного мозку молодих (3-місячних) щурів, показують, що експресія гену ОБМ у різних відділах мозку неоднакова і має хвилеподібний характер. Максимальний вміст матричної РНК (мРНК) білка виявлено у гіпокампі, таламусі та корі великих півкуль, в той час як мінімум експресії характерний для довгастого мозку й мозочка [14].
Дослідженнями [35] та [41] вперше продемонстровано різке зниження рівня ОБМ та білкової мРНК, характерне для початкових етапів ішемічного ушкодження мозку мишей (церебральної ішемії), викликаного високими концентраціями адреналіну (при підшкірному або внутрішньочеревному введенні) чи механічним шляхом (при оклюзії серединної мозкової артерії). Ішемічно-гіпоксичний стан мозку індукує загибель олігодендрогліальних клітин з наступною демієлінізацією аксонів. При цьому порушується структура гемато-енцефалічного бар'єру, що, у свою чергу, призводить до вивільнення ОБМ у кров [42].
Мінімальні показники протеїну
виявлені на першу-другу ішемічну добу впродовж терміну ішемічної експозиції.
Так, показано, що експресія ОБМ мРНК та самого білка суттєво зменшується на
23-24-ту годину церебрального ішемічного ушкодження в ішемізованих ділянках,
проте підсилюється в периішемічних зонах (зонах, розташованих поряд з
ішемізованою ділянкою) [43]. На 7-му добу спостерігається стійке підвищення
вмісту ОБМ практично у всіх відділах мозку, що свідчить про поступову
регенерацію мієлінових оболонок. Доведено, що підвищення експресії протеїну
можна викликати штучним шляхом - введенням речовин-нейропротекторів -
доксицикліну, Корвітину (рис. 1. 3), енцефаболу [44], α-кетоглутарату
та пікрозиду II
[45, 46].
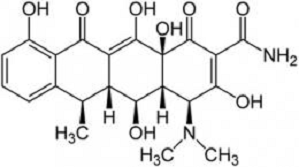
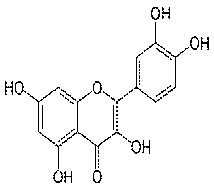
Рис. 1.3 Нейропротекторні препарати:
А - доксициклін; Б - Корвітин (кверцетин)
.3.4 Дегенерація олігодендроцитів та їх відновлення після фокальної ішемії мозку
Вперше вивченням проблеми загибелі олігодендроглії за умов фокальної ішемії та розробкою методів відновлення її клітин зайнялися команда американських дослідників з Washington University School of Medicine, очолювана професором Саллі МайАйвер (Sally R. McIver). Дослідження проводилися з використанням дорослих щурів-самців лінії Sprague Dawley вагою 200-250 г (Charles Rivers Laboratories, Wilmington, Massachusetts) [48].
Вченими показано, що вразливість олігодендроцитів за умов церебральної ішемії сприяє втраті функціонально повноцінних мієлінових оболонок. Це може призводити до руйнування білої речовини мозку. Сучасні іммуноцитохімічні методи виявлення ушкоджень олігодендроцитів в експериментальних моделях базуються на використанні антитіл до специфічних епітопів, наявних у структурі ОБМ. При цьому ці методи не дискримінують структурних змін в олігодендроцитарній морфології [48].
У дослідженні вченими використано лентивірусний вектор LV-MBP-еGFP («лентівірус-основний білок мієліну-зелений флуоресцентний білок») для визначення олігодендроцитів у білій речовині головного мозку щурів за умов перехідної фокальної церебральної ішемії та встановлено ступінь ушкодження олігодендроглії через 24 годин, 48 годин і один тиждень після реперфузії шляхом оцінки кількісного виживання клітин і аналізу процесів мієлінізації. Вірусний вектор LV проникав у клітини олігодендроглії та вбудовувався в їх геном. При цьому, як було зазначено вище, вектор містив у своєму складі сенсибілізований еGFP та ген ОБМ [48].
В загиблих у результаті церебральної ішемії олігодендроцитах спостерігається невисока реплікативна активність вірусу, причому було відмічено прогресуючу втрату GFP(+)-клітин через 24 та 48 годин після індукції ішемічного ураження мозку. GFP(+)-клітини, які вижили, мали змінену морфологію ядра, яка нагадувала аналогічну морфологію пікнотичного ядра при некрозі. Проте їх ядро не піддавалося некротичним ураженням. Такі клітини не мали у своєму складі ферменту TUNEL, тобто були TUNEL-негативними. У таких клітин показано порушення процесів мієлінізації, в результаті чого фрагментована мієлінова оболонка на початку 24-ї години після ішемії не відновлювалася.
Через тиждень після ішемії, дослідники спостерігали відновлення популяцій GFP(+)-олігодендроцитів, що було добрим прогностичним показником при відновленні мієліногенезу. Проте, за допомогою BrdU- включень показано, що проліферуючі клітини-попередники олігодендроглії не були основним джерелом GFP(+)-олігодендроцитів. Ці спостереження ідентифікували наявність нових перехідних клітинних форм між попередниками і зрілими олігодендроцитами. Подальше вивчення таких нових попередників дозволить відкрити нез'ясовані механізми структурних змін мієліну при ішемічній патології мозку [48]. Виживання і збереження цілісності мієлінопродукуючих олігодендроцитів має вирішальне значення для нормальної функції аксонів білої речовини мозку. Існує все більше доказів на моделях хвороби і в трансгенних нокаут-мишей, позбавлених експресії білків мієліну, що первинна дисфункція в олігодендроцитах може призвести до вторинного пошкодження аксонів. Це спостерігається при різноманітних неврологічних порушеннях, зокрема розсіяному склерозі, інсульті, перинатальній травмі головного мозку тощо [49].
Уразливість олігодендроцитів за умов ішемічної пошкодження мозку продемонстрована в численних моделях в пробірці і опосередковується як окисними, так і ексайтотоксичними механізмами. При гострій ішемії, яка розвинулася в результаті травматизації головного чи спинного мозку продемонстровано втрату імунореактивності до олігодендроцит-специфічних маркерів і появу у клітинах пікнотичних ядер. Олігодендроцит-специфічна експресія флуоресцентних маркерів в умовах ішемічного інсульту демонструє зниження інтенсивності флуоресценції в мієліновій оболонці [50].
Зміна перебігу процесів ремієлінізації може сприяти функціональному відновленню при демієлінізуючих захворювань і може бути залученою в початкове відновлення функції клітин в моделі пошкодження спинного мозку. Як стверджують деякі дослідники, цього можна досягти, якщо замість ушкоджених клітин трансплантаційним шляхом ввести нові, генномодифіковані попередники олігодендроглії. Тим не менш, не цілком сформований потенціал для подібної заміни олігодендроцитів при ішемії білої речовини мозку, особливо якщо це стосується дорослого організму [48].
У мозку новонароджених тварин є запас недиференційованих клітин, які за умов травматизації мозку під дією ендогенних сигнальних молекул можуть утворювати різні класи клітин нервової системи. Так може утворюватися клас специфічних «білих» олігодендроцитів, які є достатньо стійкими при різних патологічних станах мозку. Проте для дорослого мозку така кількість клітин є набагато меншою, тому питання про формування «особливих» резистентних олігодендроцитів залишається відкритим. Визначення долі «білих» олігодендроцитів речовини після осередкової ішемії в довгострокових дослідженнях може дати уявлення про передбачувані ендогенні механізми репарації мієліну, такі як ті, що описані при у моделях травматичного пошкодження спинного мозку.