Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО
тема 19. сПиРти і феноли
Гліцерол — безбарвна сиропоподібна, дуже в’язка рідина, не отруйна. Температура плавлення +18,2 °С, температура кипіння +290 °С, густина 1,26 г/мл. Із водою змішується в будь-яких співвідношеннях, дуже гігроскопічна. За рахунок своєї гігроскопічності використовується для пом’якшення шкіри в шкіряній промисловості та фармації.
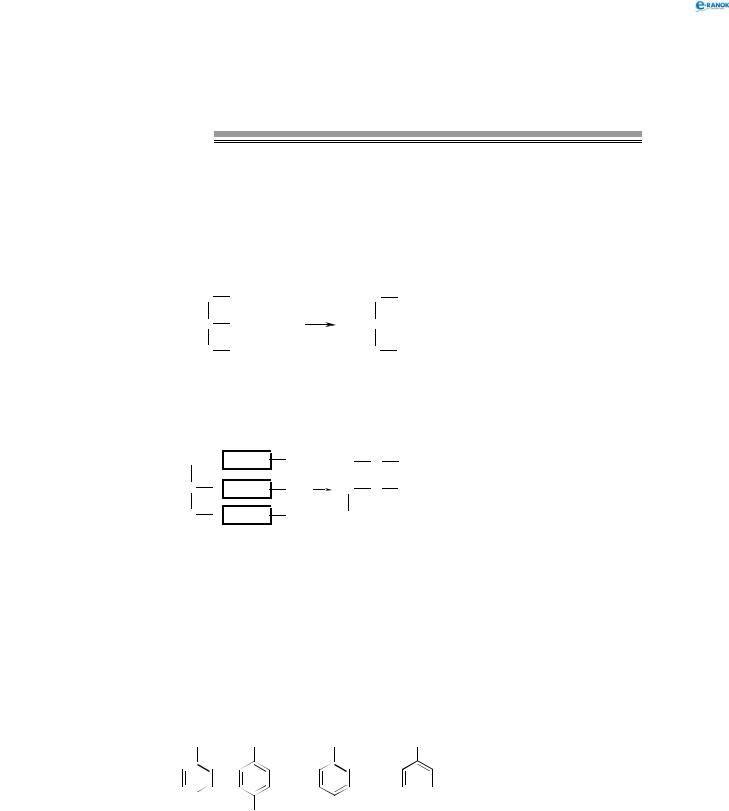
Багатоатомні спирти також здатні взаємодіяти з активними металами, зокрема з натрієм. Реакція відбувається аналогічно до одноатомних спиртів.
H2C |
OH |
H2C |
ONa |
|
2 HC |
OH |
+ 6Na |
2 HC |
ONa + 3 H2 |
H2C |
OH |
|
H2C |
ONa |
Взаємодія з натрієм відбувається дуже бурхливо з виділенням великої кількості теплоти, унаслідок чого водень, який виділяється, може самозайматися.
Взаємодія багатоатомних спиртів з мінеральними кислотами.
H2C OH HO NO2 H2C O NO2
HC OH + HO |
NO |
2 |
HC O |
NO |
2 |
+ 3H O |
|
|
|
|
2 |
H2C OH HO NO2 H2C O NO2
Взаємодією з нітратною кислотою добувають динітроетиленгліколь і тринітрогліцерол.
Якісна реакція на багатоатомні спирти. Якісною реакцією на багатоатомні спирти є взаємодія їх зі свіжоосадженим купрум(ІІ) гідроксидом. У результаті реакції при додаванні до блакитного осаду купрум(ІІ) гідроксиду розчину багатоатомного спирту утворюється темно-синій розчин комплексної сполуки Купруму із двома молекулами спирту:
Поняття про феноли
Феноли — це клас ароматичних гідроксилвмісних сполук, в яких гідроксильна група з’єднана безпосередньо з бензеновим ядром.
OH |
OH |
OH |
OH |
|
|
|
OH |
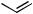
 OH
OH
OH
Фенол Гідрохінон Пірокатехін Резорцин
фізичні властивості фенолу
Фенол являє собою безбарвні кристали (в ідеалі), при зберіганні набуває рожевуватого за - барвлення внаслідок часткового окиснення. Має специфічний стійкий запах (так званий «запах карболки»). Отруйний! При потраплянні на шкіру викликає хімічні опіки. Температура плавлен - ня +42 °С. Фенол дуже погано розчиняється в холодній воді, але дуже добре розчиняється в га - рячій воді.
135
www.e-ranok.com.ua
тема 19. сПиРти і феноли
Добування фенолів
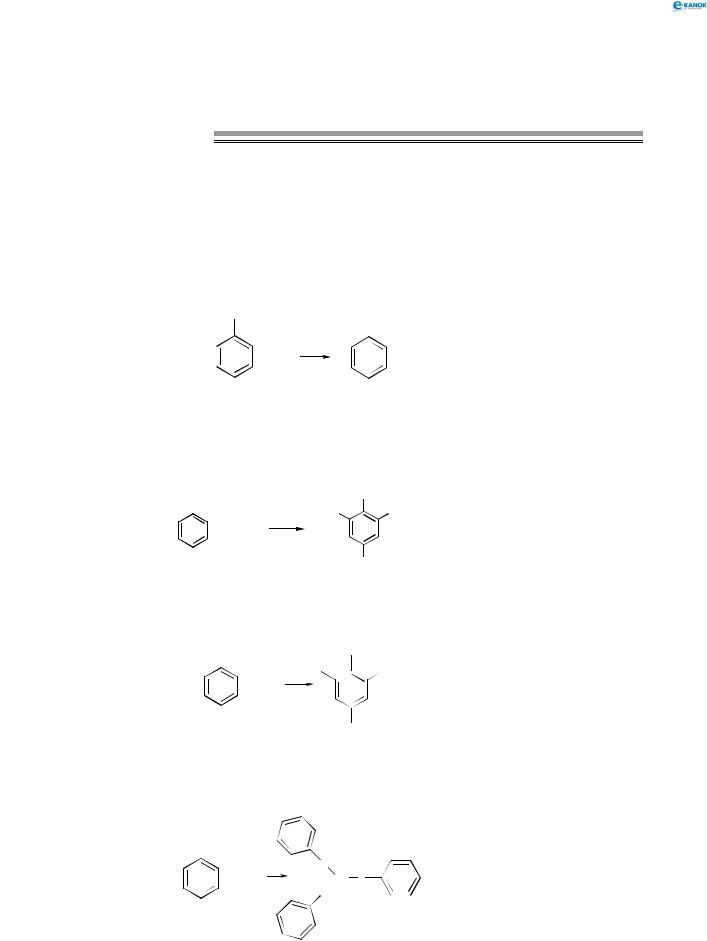
Джерелом добування фенолу є насамперед коксохімічне виробництво. Вихідною речовиною для синтезу фенолу є бензен:
C6H6 → C6H5Cl → C6H5OH.
хімічні властивості фенолів
1. Взаємодія фенолів з натрієм. Ця реакція доводить подібність фенолів до спиртів:
|
OH |
|
ONa |
|
2 |
+ 2Na |
2 |
+ |
H |
|
|
|
2 |
2. Взаємодіяфенолівзлугами.Феноли не випадково виділені із класу спиртів, вони мають особливі властивості. На відміну від спиртів, феноли здатні реагувати з лугами як звичайні кислоти:
C6H5OH + NaOH → C6H5ONa + H2O. 3. Взаємодія фенолу з мінеральними кислотами:
OH |
|
OH |
|
O2N |
NO2 |
+3HNO |
H2SO4 |
+3 H O |
3 |
2 |
|
NO2
4. Бромування фенолу також відбувається значно легше, ніж для бензолу. Реакція протікає так легко, що фенол реагує навіть із бромною водою (розчином брому у воді) з утворенням трибромфенолу, що випадає в осад:
OH |
OH |
Br |
Br |
+ 3Br2 |
+ 3HBr |
Br
5. Якісна реакція на феноли. Якісною реакцією на фенол є його кольорова реакція із ферум(ІІІ) хлоридом:безбарвнийрозчинфенолуреагуєзісвітло-жовтимферум(ІІІ)хлоридомзутвореннямтемно- синього ферум феноляту:
OH
|
O |
|
+ FeCl3 |
Fe O |
+HCl |
|
O |
|
136
www.e-ranok.com.ua

тема 19. сПиРти і феноли
Застосування фенолу
Колись фенол уважали одним з найважливіших антисептиків і широко використовували для дезінфекції приміщень, меблів, хірургічних інструментів. Дотепер збереглася тривіальна назва фенолу — карболова кислота. Зараз фенол рідко виступає в ролі антисептика, його замінили інші речовини. З фенолу добувають капролактам, який застосовують для виробництва пластмас та синтетичного капронового волокна, разом з формаліном із нього добувають феноло-формальдегідні смоли:
На основі фенолу добувають вибухові речовини, наприклад пікринову кислоту:
Окрім того, деякі феноли — гідрохінон, пірокатехін та пірогалол — застосовують у виробництві хімреактивів для фотографічних процесів.
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 38 (контрольний)
1. Дією яких реагентів можна відрізнити багатоатомні спирти від одноатомних?
А Na |
В NaOH |
Б HCl |
Г Cu(OH)2 |
2. Укажіть формулу двохатомного спирту.
АH2COH – CH2OH
БH3C – CH3 - OH
В H3C – OH
Г H3C – CH2 – CH2OH
3.Укажіть речовину, яка утворюється при бромуванні фенолу надлишком брому.
А2-бромфенол
Б2, 3 - дибромфенол
В 2, 4 - дибромфенол
Г2, 4, 6 - трибромфенол
4.Установіть відповідність між реагентами та продуктами реакції.
А C6H5Cl + NaOH |
1 |
C6H5ONa + H2 |
Б C6H5OH + Br2 |
2 |
C6H5ONa + H2O |
В C6H5OH + Na |
3 |
C6H5OH + NaCl |
Г C6H5OH + NaOH |
4 |
C6H2Br3OH + HBr |
5. Установіть генетичний ланцюг утворення етилового спирту. |
В CH4 |
|
А H3C – CH2OH |
||
Б H2C = CH2 |
Г CH ≡ CH |
|
6. При нагріванні насиченого одноатомного спирту масою 18,5 г із концентрованою сульфатною кислотою утворився алкен масою 12,6 г. Вихід продукту становить 90%. Визначте формулу вихідного спирту і у відповіді вкажіть суму індексів у спирті.
137
www.e-ranok.com.ua

тема 20. альдегіди, каРбонові кислоти
Тема 20. Альдегіди, Карбонові кислоти
Перевірте свої знання
Виконайте тест 39. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
тест 39 (вступний)
1. Позначте загальну формулу насичених одноосновних карбонових кислот.
А CnH2n+1COOH
Б CnH2nCOOH
В CnH2n+1COOCH3
Г CnH2n+1CHO
2. Найсильнішою кислотою з наведених сполук є:
А Cl – CH2 – CH2 – OH
Б Cl – CH2COOH
В CH3 – COOH
Г CHCl2 – COOH
3. Укажіть речовину, із якою реагує оцтова кислота. А метан
Б натрій гідроксид В мідь
Гнатрій хлорид
4.Установіть відповідність між реагентами та продуктами реакцій.
А CH3COOH + Cu(OH)2 |
1 |
(CH3COO)2Mg + H2 |
Б CH3COOH + Mg |
2 |
CH3COOH + CuOH + H2O |
В CH3CHO + Cu(OH)2 |
3 |
(CH3COO)2Mg + H2O |
Г CH3COOH + MgO |
4 |
(CH3COO)2Cu + H2O |
5. Розташуйте речовини в ряд за збільшенням кислотних властивостей.
А CH3COOH
Б C2H5COOH В HCOOH
ГC15H31COOH
6.У розчин оцтової кислоти масою 300 г помістили надлишок питної соди. У результаті реакції виділиться газ об’ємом 18 л (н. у.). Розрахуйте масову частку кислоти (%) у вихідному розчині.
138
www.e-ranok.com.ua

тема 20. альдегіди, каРбонові кислоти
теоретична частина
Альдегіди
Поняття про альдегіди
До альдегідів належать сполуки, які у своєму складі містять альдегідну групу. Альдегідна група є функціональною групою альдегідів:
O
 C
C
H
Скорочено альдегідну групу записують: . Найпростішим альдегідом є мурашиний альдегід, у молекулі якого до альдегідної групи приєднаний атом Гідрогену, його молекулярна формула — CH2O.
Зв’язки атома Карбону в альдегідній групі аналогічні до зв’язків у ненасичених вуглеводнях: три його валентні електронні хмари в стані sp2-гібридизації утворюють зв’язки із двома атомами Гідрогену (в інших альдегідах — з атомами Гідрогену й Карбону) і з атомом Оксигену.
З’єднані подвійним зв’язком атоми Оксигену й Карбону мають різну електронегативність. Унаслідок цього область перекривання електронів (область найбільшої електронної густини) зміщена до атома Оксигену. Таким чином, подвійний зв’язок C = O поляризований:
δ−
 O
O
δ+ C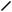
H
Назви альдегідів
формула
HCHO
CH3CHO
C2H5CHO C3H7CHO C4H9CHO
Назва IUPAC |
Тривіальна назва |
|
Метаналь |
Формальдегід, |
|
мурашиний альдегід |
||
|
||
Етаналь |
Ацетальдегід, |
|
оцтовий альдегід |
||
|
||
Пропаналь |
Пропіоновий альдегід |
|
Бутаналь |
Масляний альдегід |
|
Пентаналь |
Валеріановий альдегід |
Загальна формула насичених альдегідів CnH2nO.
Альдегіди — безбарвні речовини, з характерним запахом. Перший член гомологічного ряду альдегідів — формальдегід — при звичайних умовах є газоподібною речовиною (на відміну від спиртів).
хімічні властивості альдегідів
1. Горіння.
CH2O + O2 → CO2 + H2O .
139
www.e-ranok.com.ua