Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО

тема 18. аРоматичні вуглеводні. бенЗин
Іншимнапрямкомвикористаннякам’яноговугілляєпереробкайогонарідкеігазоподібнепаливо. Заслуговує на увагу і газифікація вугілля, тобто добування з вугілля не рідкого, а газоподібного палива.
У деяких країнах бензин для двигунів внутрішнього згорання замінюють на етанол, а також створюють автомобілі з двигунами, що працюють на метані або водні.
Найважливішими завданнями світової енергетики: обмеження витрат органічного палива, заміна його на інші енергоносії, тобто використання енергії сонця, вітру, річок, морів, океанів, атомного ядра, біологічних решток, вивільнення значної частини палива для використання у хімічній промисловості, пошук альтернативних джерел енергії.
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 36 (контрольний)
1. Бензен можна отримати
А тримеризацією ацетилену Б гідруванням гексану В тримеризацією етилену
Гкрекінгом метану
2.Укажіть умови, за яких із бензену утворюється нітробензен.
Апри дії KNO2 Б при дії KNO3 В при дії HNO2
Г при дії суміші HNO3 та H2SO4
3.Укажіть процеси, які проходять із руйнуванням ароматичної системи бензину.
Ахлорування при світлі
Б бромування в присутності FeBr3 В нітрування
Гхлорування в присутностіAlCl3
4.Установіть відповідність між реагентами та продуктами реакцій.
А C6H6 |
+ Br2 |
→t FeBr3 |
1 |
С6Н12 |
|
|
|||||||
Б C6H6 |
+ O2 |
→ |
2 |
С6Н5Br + HBr |
|||||||||
В C |
H |
6 |
+ Cl |
|
→УФ |
3 C |
6 |
H |
6 |
Cl |
6 |
|
|
6 |
|
2 |
|
4 |
|
|
|
O |
|||||
Г C |
H |
|
+ H |
→tkat |
CO |
+ H |
|||||||
6 |
6 |
2 |
|
|
|
|
|
2 |
|
|
2 |
|
|
5. Установіть генетичний ланцюг добування гексахлорану з метану. |
|
|
|
|
|
|
|||||||
А C2H2 |
|
|
|
В C6H6 |
|
|
|||||||
Б CH4 |
|
|
|
|
Г C6H6Cl6 |
|
|||||||
6. У бензині масова частка гептанових ізомерів становить 80%, а октанових — 20%. Який об’єм кисню (м3) (н. у.) потрібний для спалювання такого бензину масою 30 кг?
130
www.e-ranok.com.ua

тема 19. сПиРти і феноли
Тема 19. Спирти і феноли
Перевірте свої знання
Виконайте тест 37. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
тест 37 (вступний)
1.Укажіть назву органічної сполуки, яка належить до трьохатомних спиртів:
АМетанол
Б етиленгліколь В гліцерол Г етанол
2. Укажіть формулу фенолу.
А C6H5CH3
Б С6H5OH
В C6H5NH2
Г C6H5Cl
3. Феноли відрізняються від одноатомних насичених спиртів здатністю: А реагувати з активними металами Б реагувати з лугами В реагувати в галогеноводнями Г утворювати естери
4. |
Установіть відповідність між реагентами та продуктами реакцій. |
|
|
|
|
||||
|
А CH3OH + Na |
1 |
HCHO + H2O |
|
|||||
|
Б CH3OH + HBr |
2 |
CH3ONa + H2 |
|
|||||
|
В CH3OH + [O] |
3 |
CH3Br + H2O |
O |
|||||
|
Г CH |
CH |
OH →H2SO4 |
4 |
CH |
2 |
= CH |
+ H |
|
|
3 |
2 |
|
|
|
2 |
2 |
|
|
5. |
Розташуйте речовини в ряд за посиленням кислотних властивостей. |
|
|
|
|
||||
|
А CH3OH |
|
В C6H5OH |
|
|
||||
|
Б C2H5OH |
Г HOH |
|
|
|||||
6. Бромна вода, що містила 43,2 г брому, повністю прореагувала з фенолом, що міститься у 15 г водного розчину. Розрахуйте масову частку фенолу у водному розчині (%).
131
www.e-ranok.com.ua

тема 19. сПиРти і феноли
теоретична частина
Спирти й феноли
Спирти—оксигеновмісніорганічніречовини,молекулиякихмістятьоднуабокількагідроксильних груп OH, приєднаних до карбонового радикала. Групу OH називають функціональною групою, оскільки вона відповідає за всі функціональні особливості спиртів, за якими спирти відрізняються від вуглеводнів та які обумовлюють їхні фізичні й хімічні властивості.
За числом гідроксильних груп у молекулах спирти поділяють на одноатомні (одна гідроксильна група), двохатомні (дві гідроксильні групи) тощо.
Загальна формула одноатомних спиртів:
CnH2n+1OH (R − OH) або CnH2n + 2O.
За типом атома Карбону, до якого приєднана гідроксильна група, спирти поділяють на первинні, вторинні й третинні.
CH3 CH2 CH2 |
OH |
CH3 CH CH3 |
|
|
OH |
первинний спирт |
вторинний спирт |
|
|
CH3 |
|
CH3 |
C |
CH3 |
OH
третинний спирт
Спирти також мають загальну назву — алканоли та алкоголі.
Правила складання назви спиртів ґрунтуються на правилах для алканів з деякими доповненнями:
1.Назва спиртів походить від назви відповідного алкану зміною суфікса -ан на -ол.
2.ОскількиіснуютьспиртизоднаковоюкількістюатомівКарбонувмолекулі,вякихOH-групапри- єднана до різних атомів Карбону, то слід також указувати положення гідроксильної групи (пропанол-1, пропанол-2, гексанол-3 тощо).
3.При складанні назв спиртів розгалуженої будови нумерацію карбонових атомів починають із того кінця, ближче до якого гідроксильна група, у назві спершу позначають місця відгалужень, а потім положення гідроксильної групи (2-метилпропанол-1, 3-метилбутанол-1 тощо). Таким чином, тут зберігається той самий принцип, що й у ненасичених сполуках.
У ряді насичених одноатомних спиртів, на відміну від насичених і ненасичених вуглеводнів, немає газоподібних речовин, хоча перші члени ряду мало відрізняються від них за молекулярною масою. Це пояснюється утворенням водневого зв’язку між молекулами спиртів.
За рахунок нього молекули спиртів, так само, як і води, асоційовані, між ними існує додаткова сила міжмолекулярної взаємодії.
Сутність водневого зв’язку полягає в тому, що гідроксильний атом Гідрогену внаслідок зсуву електронної густини до Оксигену має частковий позитивний заряд. Атом Оксигену через наявність у ньо-
132
www.e-ranok.com.ua

тема 19. сПиРти і феноли
го неподілених електронних пар і зміщеної до нього електронної густини зв’язків O − H має негативний заряд.
H H
δ− δ+
H C
C C
C O
O H
H
H H
Таким чином встановлюється електростатична взаємодія між атомами Гідрогену й Оксигену різних молекул спирту.
методи добування спиртів
1. Гідратація алкенів. При взаємодії алкенів з водою в присутності мінеральних кислот (сульфатної, фосфатної) утворюються спирти. Мінеральні кислоти виконують роль каталізаторів і є джерелом протонів:
H2C CH + H O H
CH + H O H
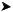 CH3 CH2 OH
CH3 CH2 OH
2. Гідроліз галогенопохідних алканів водним розчином лугів:
CH3 CH2 C l + K O H |
CH3 CH2 OH |
||
|
|
|
–K C l |
|
(водн. розчин) |
|
|
3. Відновлення альдегідів у присутності каталізаторів:
O
CH3 C |
+ 2[H] |
CH3 CH2 OH |
H
4. Етиловий спирт можна добувати спиртовим бродінням вуглеводів (глюкози) під впливом ферменту зимази спиртових дріжджів:
C6H12O6 → 2C2H5OH + 2CO2 ↑.
хімічні властивості спиртів
1. Горіння. При збільшенні кількості атомів Карбону в молекулі спиртів поряд з реакцією повного згорання спиртів може відбуватися реакція неповного згорання з виділенням сажі (вуглецю), що призводить до збільшення світління полум’я. Виділення різних продуктів (CO2 та C) пояснює явище яскравого полум’я, що коптить.
Повне згорання (достатня кількість кисню):
C2H5OH +3O2 →2CO2 +3H2O.
Неповне згорання з виділенням чадного газу (нестача кисню):
C4H9OH + 4O2 → 4CO +5H2O.
Неповне згорання з виділенням сажі (нестача кисню):
C6H13OH +3O2 →6C +7H2O.
2. Взаємодія спиртів з лужними металами. Атоми активних металів витісняють атоми Гідрогену гідроксильної групи з утворенням алкоголятів та газоподібного водню:
133
www.e-ranok.com.ua
тема 19. сПиРти і феноли
2C2H5OH +2Na →2C2H5ONa+ H2 ↑.
етилат
натрію
3. Взаємодія спиртів з галогеноводнями:
C2H5OH + HBr → C2H5Br + H2O.
4. Дегідратація. Процес дегідратації може відбуватися двома різними способами: за участю однієї молекули спирту та двох молекул спирту.
4.1. Внутрішньомолекулярна дегідратація:
H H |
|
H H |
H C C H |
H2SO4 |
H C C H + H2O |
|
HOH
4.2.Міжмолекулярна дегідратація:
H |
H |
H |
H |
H C |
C OH + HO |
C |
H2SO4 |
C H |
|||
H |
H |
H |
H |
H |
H |
H |
H |
H C C O C C H + H2O |
|||
H |
H |
H |
H |
Застосування спиртів
Спирти використовують як органічні розчинники, як паливо для двигунів (добавка метилового й етилового спиртів сприяє повноті згорання й запобігає забрудненню атмосфери).
Їх використовують також для виробництва бутадієну, з якого в подальшому виготовляють синтетичний каучук, для добування низки фармацевтичних препаратів (медичного етеру, хлоретану тощо), а ще для добування оцтової кислоти та «фруктових есенцій» (естерів).
Метиловий спирт використовують для добування формальдегіду, потрібного для виробництва пластмас та феноло-формальдегідних смол і деяких етерів (за аналогією до етилового спирту).
Багатоатомні спирти
Загальна формула багатоатомних спиртів:
|
|
|
CnH2n+ 2− m (OH)m. |
|
CH2 |
CH2 |
— етандіол, або етиленгліколь |
|
OH |
OH |
|
CH2 |
CH |
CH2 |
— пропантріол-1,2,3, або гліцерол |
OH |
OH |
OH |
|
Етиленгліколь — це безбарвна сиропоподібна рідина, солодкувата на смак, добре розчиняється у воді й спирті, не розчиняється у вуглеводнях та етерах. Температура кипіння +197,9 °С, температура плавлення –12,6 °С, густина 1,12 г/мл. Надзвичайно отруйна!
134
www.e-ranok.com.ua