Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО

тема 18. аРоматичні вуглеводні. бенЗин
Тема 18. Ароматичні вуглеводні. Бензин. Природні джерела вуглеводнів та їхня переробка
Перевірте свої знання
Виконайте тест 35. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
|
тест 35 (вступний) |
1. Укажіть молекулярну формулу ароматичного вуглеводню. |
|
А С6Н6 |
В С6Н14 |
Б С6Н12 |
Г С6Н10 |
2.Укажіть невідому речовину «Х» у схемі перетворень: ацетилен → Х → гексахлоран.
Аетилен
Б етан В бензен
Гметан
3.Назвати основний компонент природного газу.
А метан Б ацетилен В пропан
Гбутан
4.Укажіть відповідність фракції нафти і температури збирання фракції.
А газолінова |
1 |
>275 |
0 |
|
|
|
|
Б лігроїнова |
2 |
180 |
0–3000 |
В гасова |
|
|
3 1500–2500 |
Г газойль |
4 |
40 |
0–2000 |
5. Установіть генетичний ланцюг добування хлорбензену з метану.
А С6Н5Cl |
В СН4 |
Б С2Н2 |
Г С6Н6 |
6. Яку масу бензену (г) можна синтезувати з ацетилену об’ємом 4 л, якщо масова частка виходу бензену становить 46% теоретично можливого?
125
www.e-ranok.com.ua
тема 18. аРоматичні вуглеводні. бенЗин
теоретична частина
Ароматичні вуглеводні (Арени)
Ароматичними вуглеводнями (аренами) називають речовини, в молекулах яких міститься одне або кілька бензенових кілець — циклічних груп атомів Карбону з особливим характером зв’язків. Найпростішим представником ароматичних сполук є бензен. Першу структуру бензену запропонував у 1865 р. німецький учений А. Кекуле:
H |
|
H |
H |
|
або просто |
H |
H |
H |
, |
Згідно із сучасними уявленнями, шість атомів Карбону в молекулі бензену перебувають у sp2- гібридному стані. Кожен атом Карбону утворює σ -зв’язки із двома іншими атомами Карбону та одним атомом Гідрогену, що лежать в одній площині. Кути між трьома σ -зв’язками дорівнюють 120°. Таким чином, усі атоми Карбону лежать в одній площині, утворюючи правильний шестикутник.
Кожен атом Карбону має одну негібридну p-орбіталь. Шість таких орбіталей розташовуються перпендикулярно до площини циклу з атомів Карбону й паралельно один до одного:
Усі шість p-електронів взаємодіють між собою, утворюючи π -зв’язки, не локалізовані в пари, як при утворенні звичайних подвійних зв’язків, а такі, що утворюють єдину π -електронну хмару. Таким чином, у молекулі бензену здійснюється кругове зв’язування. Найбільша π -електронна густина у цій зв’язаній системі розташовується над і під площиною карбонового ланцюга:
H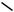 H
H
H


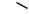
 H
H
HH
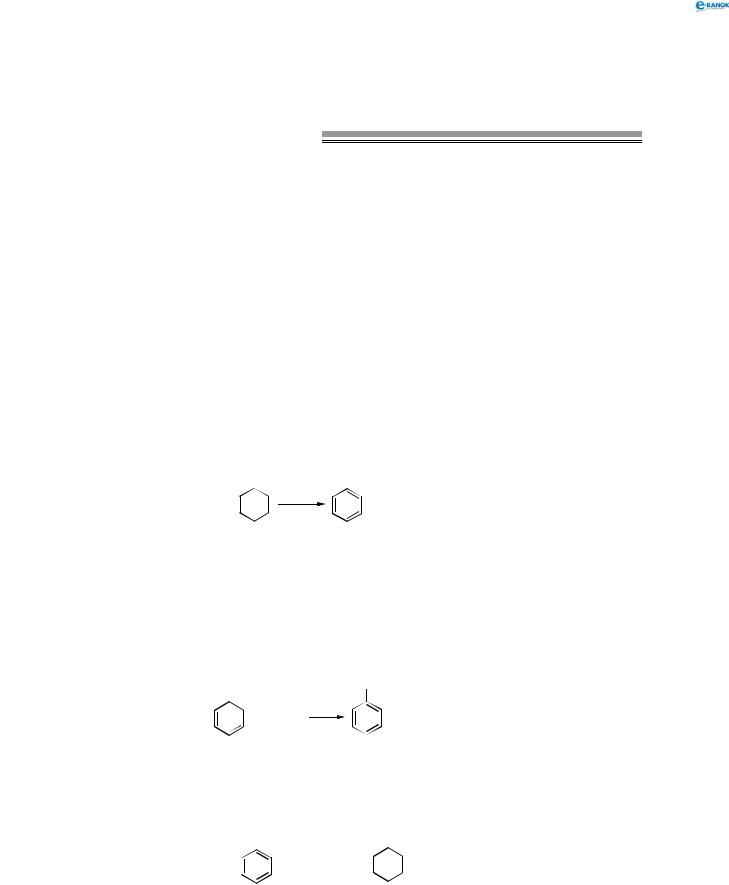
Як наслідок, усі зв’язки між атомами Карбону в бензені вирівняні й мають довжину 0,139 нм. Ця величина є проміжною між довжиною одинарного зв’язку в алканах (0,154 нм) і довжиною подвійного зв’язку в алкенах (0,133 нм). Рівноцінність зв’язків заведено позначати кружечком усередині циклу:
126
www.e-ranok.com.ua
тема 18. аРоматичні вуглеводні. бенЗин
Кругове зв’язування дає виграш в енергії 150 кДж/моль. Ця величина становить енергію зв’язування — кількість енергії, яку необхідно затратити, щоб порушити ароматичну систему бензолу. Така електронна будова пояснює всі особливості бензену. Зокрема, зрозуміло, чому бензен важко вступає в реакції приєднання — це призводить до порушення зв’язування. Такі реакції можливі тільки в дуже жорстких умовах. Сукупність властивостей бензену заведено називати проявом ароматичного характеру, або ароматичністю.
До одноядерних аренів належать бензен та його похідні, загальна формула вуглеводнів ряду бензену: CnH2n- 6. Відповідно, першим членом гомологічного ряду одноядерних аренів є вуглеводень із шістьма атомами Карбону, тобто C6H6 — бензен.
Перші члени гомологічного ряду бензену — безбарвні рідини зі специфічним запахом. Вони легші за воду й у ній не розчиняються. Добре розчиняються в органічних розчинниках і самі є гарними розчинниками для багатьох органічних речовин. Бензен має характерний, досить приємний запах, але при цьому є дуже токсичним.
Добування аренів
1. Дегідрування циклоалканів також призводить до ароматичних вуглеводнів. Реакція відбувається при пропусканні парів циклогексану або його гомологів над нагрітою платиною:
Pt |
+3H2 |
|
2. Бензен можна добувати при тримеризації ацетилену. Реакція відбувається при пропусканні ацетилену над активованим вугіллям при температурі +600 °С:
3CH ≡ CH → C6H6 .
хімічні властивості аренів
1. Галогенування. Бензен та його гомологи взаємодіють із хлором або бромом у присутності каталізаторів — безводних AlCl3, FeBr3 або AlBr3:
AlCl3
+ Cl2
Cl
+ HCl
2. Нітрування:
C6H6 + HNO3 H2SO4→C6H5 − NO2 + H2O.
3. Гідрування бензену йде при нагріванні й високому тиску в присутності металічних каталізаторів (Ni, Pt, Pd). Бензен перетворюється в циклогексан:
Ni
+ 3H2
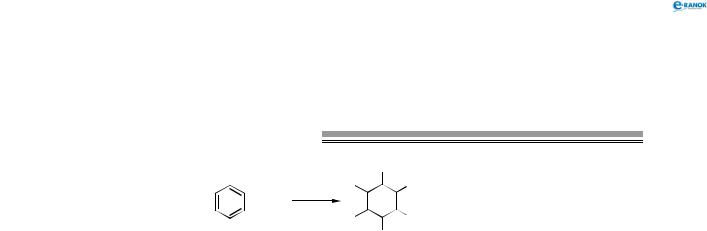
4. Радикальне галогенування бензену відбувається при взаємодії його парів із хлором тільки під впливомжорсткогоультрафіолетовоговипромінювання.Прицьомубензенприєднуєтримолекулихлору й утворюється твердий продукт — гексахлорциклогексан (гексахлоран):
127
www.e-ranok.com.ua
тема 18. аРоматичні вуглеводні. бенЗин
|
|
|
|
Cl |
|
|
hν |
Cl |
Cl |
|
|
|
|
|
+ |
3Cl2 |
|
|
|
|
|
|
||
|
|
|
Cl |
Cl |
Cl
(атоми Гідрогену в молекулі C6H6Cl6 не зазначені). 5. Повне окиснення (горіння)
2C6H6 + 15O2 → 12CO2 + 6H2O
Природні джерела вуглеводнів та їхня переробка
Природний газ
Основним компонентом природного газу є метан. Середній вміст метану за об’ємом становить 80–97%. Крім метану у природному газі є його гомологи (2-3%) – етан, пропан, бутан та невелика кількість домішок – сірководню, азоту, оксиду карбону (IV) і водяної пари.
Природний газ – цінне паливо. Він є важливою сировиною для хімічної промисловості. З нього добувають сажу, водень, ацетилен, синтез – газ тощо.
Супутній нафтовий газ
Супутній нафтовий газ за своїм походженням також є природним газом. Такий газ відрізняється від природного за складом: у нього міститься менше метану (30–50% за об’ємом), але більше етану, пропану, бутану, пентану (7–20% за об’ємом), ніж і природному газі. Його вловлюють і використовують як паливо і як дешеву сировину.
Під час хімічної переробки попутного газу виділяють індивідуальні вуглеводні: етан, пропан, бутан тощо. З них добувають ненасичені вуглеводні, з яких далі синтезують пластмаси, каучуку.
Склад нафти
За хімічним складом нафта – це природна суміш великої кількості органічних речовин, близько 90% яких становлять різні вуглеводні: насичені, циклопарафіни, ароматичні тощо. Співвідношення цих вуглеводнів у нафтах різних родовищ коливається. Крім вуглеводнів нафта містить також оксигено-, сульфурота нітрогеновмістні органічні сполуки.
Нафтопродукти та їх властивості
Розрізняють дві групи нафтопродуктів: світла та темні.
До світлих нафтопродуктів належать: бензин, що містить вуглеводні складу С5 – С11 з температу- |
|||||||
рою кипіння від 40 до 200 0С, лігроїн, що містить вуглеводні складу С |
8 |
– С |
14 |
з температурою кипін- |
|||
ня від 150 до 250 0С, гас, який складається з вуглеводнів складу С |
12 |
– С |
18 |
з температурою кипіння від |
|||
180-300 0С, газойль С15 – С20 з температурою кипіння понад 300 0С.
До темних нафтопродуктів належать: мазут, з якого виробляють мастила (веретенне, машинне, тощо ), вазелін, парафін, гудрон.
Переробка нафти
Первинна переробка нафти полягає в її перегонці, тобто розділенні на фракції: світлі та темні нафтопродукти.
128
www.e-ranok.com.ua

тема 18. аРоматичні вуглеводні. бенЗин
Вторинна переробка нафти включає методи переробки на бензин важких нафтових фракцій (гас, солярові масла, мазут).
У промисловості застосовують термічний і каталітичний крекінг.
Термічний крекінг проводять під час нагрівання мазуту до температури 450–550 0С з тиском 2,2–7,7 МПА. У процесі термічного крекінгу молекули вуглеводнів з молекулярною масою (великою кількістю атомів Карбону) розщеплюються на молекули насичених і ненасичених вуглеводнів з меншою молекулярною масою. Наприклад:
С16Н34 → C18H18 + C8H16.
Гексадекан Октан Октен
Процес розщеплення вуглеводнів нафти на речовини з меншою молекулярною масою і з нижчою температурою кипіння називається крекінгом ( англ. сrack - розколюватися, тріскатися)
Термічний крекінг відкрив у 1891р. російський інженер В.Г. Шухов.
Каталітичних крекінг проводять за наявності каталізаторів (переважно алюмосилікатів) при 450 0С й атмосферному тиску. Таким способом добувають авіаційний бензин.
Однією з найважніших характеристик усякого бензину є його детонаційна стійкість. Вибухове згорання бензину має назву детонації.
Найменш стійки до детонації — парафін нормальної будови. Вуглеводні розгалужені, ненасичені, ароматичні стійкі.
Для кількісної характеристики детонаційної стійкості бензинів вироблено октанову шкалу. Кожний вуглеводень і кожний сорт бензину характеризується певним октановим числом. Бензин має октанове число 80, то це означає, що він допускає таке саме стискання в циліндрі без детонації, як суміш з 80% ізооктану і 20% пентану.
Під час каталітичного крекінгу одночасно з реакціями розщеплення вуглеводнів відбувається також реакції ізомеризації, внаслідок перебігу яких утворюється вуглеводнів з розгалуженим карбоновим ланцюгом. Наявність останніх поліпшує якість бензину.
Важливим каталітичним процесом є ароматизація вуглеводнів, які входять до складу нафти, тобто перетворення насичених вуглеводнів і циклопарафінів на ароматичні вуглеводні, зокрема бензол, толуол тощо.
Під час перебігу крекінг – процесів утворюється велика кількість газоподібних органічних сполук (гази крекінгу), які містять здебільшого газоподібні насичені і ненасичені вуглеводні, зокрема метан, етан, етилен тощо. Ці гази використовують як сировину у хімічній промисловості.
Коксохімічне виробництво
Основний метод переробки кам’яного вугілля – коксування (піроліз)
Піролізом називається процес розкладання органічних речовин без доступу повітря за високої температури.
Під час коксування вугілля нагрівають без доступу повітря до температури 1000-1200 0С. Внаслідок його піролізу добувають чотири основних продукти: кокс, кам’яновугільну смолу, аміачну воду і коксовий газ. Нині відомо кілька способів переробки кам’яного вугілля на рідке паливо:
1)синтез, що ґрунтується на перетворення вугілля під тиском на суміш горючих речовин з використанням водяної пари, повітря, кисню;
2)гідрування – спосіб, що ґрунтується на насиченні вугілля воднем: взаємодія вугілля за високих температури і тиску з гідрогеновмістними речовинами.
129
www.e-ranok.com.ua