Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО
тема 20. альдегіди, каРбонові кислоти
2. Гідрування. Гідрування альдегідів проходить у присутності каталізаторів (Ni, Pt, Pd тощо).
H |
|
|
|
|
H |
|
|
|
|
|
|
H C |
H |
|
|
H |
C H |
|
|
|
|
||
C |
|
+ |
H |
|
або CH3 CH2 OH |
H |
O |
H |
H |
CH |
|
|
|
|
|
O H |
3. Окиснення альдегідів (реакція «срібного дзеркала»).
+1 |
O |
|
t0 |
|
O |
|
|
|
+3 |
|
|||
H3C C |
+ Ag |
O |
+ 2Ag |
|||
|
H C C |
|||||
|
2 |
|
|
3 |
|
|
|
H |
|
|
|
OH |
Аналогічно до аргентум оксиду купрум(ІІ) гідроксид здатний окиснювати альдегіди. При цьому утворюється жовтий осад одновалентного купрум(І) гідроксиду:
O |
O |
t0 |
+ 2CuOH + H2O |
H3C — C + 2Cu(OH)2 → H3C — C |
|
H |
CH |
При подальшому нагріванні відбувається розклад купрум(І) гідроксиду й утворення червоного осаду одновалентного купрум(І) оксиду:
|
|
|
t0 |
|
+ H2O. |
|
|
|
|
|
2CuOH → Cu2O |
|
|
||
4. |
Поліконденсація. |
|
|
|
|
|
|
|
H |
H |
H |
H |
H |
H |
|
|
OH |
C |
OH |
C |
OH |
C |
OH |
|
H |
O H |
H |
O H |
H O H |
|
|
|
OH |
OH |
OH |
OH |
|
|
|
|
|
CH |
CH |
|
CH |
CH2 |
|
|
|
2 |
2 |
2 |
|
|
|
|
–H2O |
|
|
|
|
|
|
Добування альдегідів |
|
|
|
|
|
|
|
1. |
Окиснення спиртів. |
|
|
|
|
|
|
|
CH3 − CH2 − OH + CuO → CH3 − CHO + H2O + Cu. |
|
|||||
2. |
Окиснення метану. |
|
|
|
|
|
|
Методдобуванняформальдегідузметанускладається,восновному,зкількохстадій:1)шляхомвзаємодії метану з водною парою добувають водний газ (суміш водню й карбон(ІІ) оксиду CO); 2) із нього синтезують метиловий спирт; 3) потім спирт окиснюють у мурашиний альдегід:
CH4 + H2O 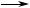 CO + H2
CO + H2 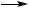 CH3OH
CH3OH 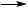 CH2O
CH2O
3. Реакція Кучерова.
CH ≡ CH + H2O → CH2 = CH − OH → CH3 − CHO.
140
www.e-ranok.com.ua

тема 20. альдегіди, каРбонові кислоти
4. Окиснення етилену киснем.
2CH2 = CH2 + O2 → 2CH3 − CHO.
Застосування альдегідів
Формальдегід. Застосовують у виробництві термореактивних пластмас, феноло-формальдегідних та сечовино-формальдегідних смол.
Формальдегід є біологічно активною речовиною: під його впливом відбувається згортання (денатурація) білка. На цьому ґрунтується його (точніше його водного розчину — формаліну) застосування як засобу для дезінфекції, як дубильного засобу та консерванта для анатомічних препаратів. Формаліном називають 37—40% водний розчин формальдегіду, до якого як інгібітор полімеризації додають 6—15% метанолу. У медицині також використовують похідні формальдегіду — гексаметилентетрамін (уротропін).
Ацетальдегід. Найважливіші застосування оцтового альдегіду ґрунтуються на використанні його реакцій окиснення та відновлення. За допомогою першої з них добувають оцтову кислоту, за допомогою другої у деяких країнах — етиловий спирт. Основне застосування оцтового альдегіду — добування оцтової кислоти.
Карбонові кислоти
Карбонові кислоти належать до оксигеновмісних органічних сполук і мають у своєму складі функціональну групу, що визначає їхню приналежність до кислот.
O
функціональна група |
C |
OH
У кислот функціональна група поєднує в собі карбонільну та гідроксильну групи — COOH. Цю групу називають карбоксильною групою.
Класифікація карбонових кислот
Класифікація за вмістом Оксигену: оскільки до складу функціональної групи кислот входять атоми Оксигену, то всі карбонові кислоти належать до оксигеновмісних кислот.
Класифікація за силою кислот: усі карбонові кислоти є слабкими кислотами.
Класифікація за основністю кислот: так само, як неорганічні кислоти, органічні поділяють за основністю.Причомуосновністькислотвизначаєтьсякількістюкарбоксильнихгруп.
Одноосновні кислоти
O |
O |
H C C |
H3C CH2 C |
3 |
OH |
OH |
оцтова |
|
пропіонова |
|
||
Двохосновні кислоти |
|
|
|
|
|
O |
O |
O |
|
O |
|
C |
CH CH C |
|
|||
C (CH2)6 C |
|
OH |
|||
OH |
HO |
OH OH |
|||
HO |
|||||
|
|
||||
коркова |
|
|
винна |
|
|
141
www.e-ranok.com.ua

тема 20. альдегіди, каРбонові кислоти
Класифікація за вуглеводневим радикалом: карбонові кислоти можна класифікувати за вуглеводневим радикалом — насичені, ненасичені (акрилова) та ароматичні (бензойна, фталева, корична, саліцилова).
Назва карбонових кислот та їхніх солей
формула |
Тривіальна назва |
Назва солей |
Назва IUPAC |
|
|
HCOOH |
Мурашина |
Форміат (метаноат) |
Метанова |
|
|
CH3COOH |
Оцтова |
Ацетат (етаноат) |
Етанова |
|
|
CH3CH2COOH |
Пропіонова |
Пропіонат (пропаноат) |
Пропанова |
|
|
CH3 (CH2 )2 COOH |
Масляна |
Бутират (бутаноат) |
Бутанова |
|
|
CH3 (CH2 ) COOH
Пентанова 3
CH3 (CH2 ) COOH
Гексанова 4
CH3 (CH2 )14 COOH
Гексадеканова
CH3 (CH2 )16 COOH
Октадеканова
Валеріанова Валерат (пентаноат)
Капронова Капронат (гексаноат)
Пальмітинова Пальмітат
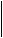 Стеаринова
Стеаринова 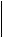 Стеарат
Стеарат
CH3 (CH2 )7 − CH = CH − (CH2 )7 COOH Олеїнова |
Олеат |
Октадеценова |
|
Загальна формула гомологічного ряду одноосновних насичених карбонових кислот:
(CnH2n + 1COOH або CnH2nO2).
Ізомерія кислот зумовлена будовою радикала.
хімічні властивості карбонових кислот
1. Вплив кислот на індикатори за рахунок дисоціації на йони:
CH3COOH CH3COO− +H+.
2. Взаємодія з металами:
Zn + 2CH3COOH → Zn(CH3COO)2 + H2. 3. Взаємодія з оксидами металів:
MgO + 2CH3COOH → Mg(CH3COO)2 + H2O.
4. Взаємодія з лугами:
CH3COOH + NaOH → CH3COONa + H2O.
5. Горіння:
Як і більшість органічних сполук, карбонові кислоти дуже добре горять, причому чим більшим є вуглеводневий радикал, тим більша ймовірність протікання реакції горіння з виділенням сажі (вільного вуглецю):
CH3COOH +2O2 →2CO2 + H2O , C17H35COOH + 8O2 →17C +18H2O.
142
www.e-ranok.com.ua
тема 20. альдегіди, каРбонові кислоти
6. Реакція естерифікації.
Карбонові кислоти здатні взаємодіяти зі спиртами з утворенням естерів:
|
|
O |
|
|
|
H3C |
C |
|
|
|
|
|
|
OH + H |
O |
CH2 |
CH3 |
|
|
O |
|
|
|
|
H C |
C |
|
+ H2O |
|
|
3 |
|
|
|
|
|
|
O |
CH2 |
CH3 |
|
7. Взаємодія з хлором. |
|
|
|
|
|
H |
|
O |
|
H |
O |
|
|
|
|
||
H C |
C |
+ Cl2 |
H |
C |
C + HCl |
H |
|
OH |
|
Cl |
OH |
|
|
|
|
||
Застосування мурашиної кислоти.
Оскільки при нагріванні мурашиної кислоти з оцтовою виділяється чадний газ, то її часто використовують у лабораторії для добування чистого чадного газу.
Мурашину кислоту широко використовують в органічному синтезі, як протраву при фарбуванні текстилю, у бджільництві проти вароатозу, для добування пестицидів тощо. У медицині мурашину кислоту застосовують у вигляді 1% спиртового розчину (мурашиний спирт) як розтирку при невралгіях, міозитах та інших захворюваннях.
Застосування оцтової кислоти.
Реакцією плюмбум(ІІ) оксиду з оцтовою кислотою добувають плюмбум(ІІ) ацетат Pb(CH3COO)2 (його також називають свинцевим цукром, унаслідок солодкого смаку), розчин якого застосовують у медицині (свинцева примочка).
Взаємодією ферум(ІІІ) гідроксиду з кислотою добувають ферум(ІІІ) ацетат Fe(CH3COO)3 , відомий як протрава при фарбуванні: нанесений на тканину, він, з одного боку, міцно втримується волокнами, з іншого боку, добре втримує барвник.
На мову хімії можна перекласти й використання оцтової кислоти для добування естерів, наприклад етилового естеру та інших естерів, які через їхній приємний запах використовують в парфумерній та харчовій промисловості.
У сільському господарстві та харчовій промисловості оцтову кислоту, а також її найближчі гомологи — мурашину й пропіонову — використовують як консерванти, що запобігають гнильним процесам і зберігають високу поживність кормів.
Добування кислот
1. Окиснення метану:
2СН4 + 3О2 →t0 2НСООН + 2Н2О
2. З чадного газу:
СО + NaOH → HCOONa, HCOONa + HCl → HCOOH + NaCl
143
www.e-ranok.com.ua

тема 20. альдегіди, каРбонові кислоти
3. Окиснення бутану:
2C4H10 + 5O2 → 4CH3COOH + 2H2O
4. Окиснення етанолу:
C2H5OH + O2 → CH3COOH + H2O
5. Окиснення етаналю:
CH3COH +Ag2O → CH3COOH + 2Ag
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 40 (контрольний)
1. |
Укажіть речовину, яка утворюється при окисненні альдегіду. |
||
|
А спирт |
В естери |
|
|
Б карбонова кислота |
Г вуглеводень |
|
2. |
Укажіть речовину, для якої відбувається реакція «срібного дзеркала». |
||
|
А метаналь |
|
В оцтова кислота |
|
Б етанол |
Г фенол |
|
3.Укажіть назву функціональної групи, наявної у карбонових кислот.
Агідроксильна
Б карбонільна В карбоксильна
Гальдегідна
4.Установіть відповідність між реагентами та продуктами реакцій.
А HCHO + H2 → |
1 |
CO2 + H2O +Ag |
Б HCHO + Cu(OH)2 → |
2 |
HCOOH + CuOH + H2O |
В HCHO +Ag2O → |
3 |
CH3OH |
Г HCOOH +Ag2O → |
4 |
HCOOH +Ag |
5. Установіть генетичний ланцюг утворення натрій етаноату. |
||
А C2H5OH |
В C2H4 |
|
Б CH3COOH |
Г C2H6 |
|
6.Визначити масу етаналю (т), яку можна добути з 2 т технічного кальцій карбіду, масова частка домішок у якому 15%.
144
www.e-ranok.com.ua