Материал: А27483 Красникова ЛВ Кострова ИЕ Машкин ДВ Микробиология производства хлеба кондит и макарон изделий
L. fermentum. Палочки короткие размером (2–3)(0,5–1,0) мкм; располагаются одиночно. При сбраживании углеводов образует DL-изомеры молочной кислоты. Как и L. brevis, является специфичным для заквасок.
L. buchneri. Палочки мелкие с закругленными концами размером (2–4)(0,7–1,0) мкм; располагаются одиночно, попарно или в виде цепочек. Вызывает гетероферментативное молочнокислое брожение, образуя DL-изомеры молочной кислоты. В заквасках встречается довольно редко.
L. sanfrancisсo. Ранее этот вид считался подвидом L. brevis. Палочки очень мелкие с закругленными концами размером (0,7–4) (0,30–0,35) мкм. При сбраживании углеводов по гетероферментативному пути образует DL-молочную кислоту. Впервые выделен из сырого теста в 1984 г. в г. Сан-Франциско, откуда и получил свое название.
Молочнокислые бактерии играют существенную роль в формировании вкуса и аромата хлеба, особенно ржаного. В результате сбраживания сахаров в тесте молочнокислые бактерии образуют молочную, уксусную, пропионовую, муравьиную кислоты, спирт и диоксид углерода. Молочная кислота придает ржаному хлебу приятный кисловатый вкус, а летучие кислоты – специфический аромат. Большое значение в образовании ароматического комплекса хлеба играют вторичные продукты метаболизма молочнокислых бактерий: альдегиды, ацетоин, диацетил, оксиметилфурфурол, фурфурол, диоксиацетон. Диоксид углерода способствует разрыхлению теста. Образуемые молочнокислыми бактериями кислоты не влияют на жизнедеятельность дрожжей и в то же время подавляют рост гнилостных, маслянокислых, уксуснокислых бактерий, представителей бактерий группы кишечной палочки. Гомо- и гетероферментативные лактобациллы осуществляют также протеолиз белков пшеничной и ржаной муки, способствуя накоплению в тесте азотосодержащих и водорастворимых соединений.
1.2.2. Гомоферментативное молочнокислое брожение
Гомоферментативное молочнокислое брожение является единственным способом получения энергии группой молочнокислых бактерий, которые при сбраживании глюкозы образуют от 85 до 90 % молочной кислоты. Такой тип брожения вызывают молочнокислые бактерии подродов Thermobacterium и Streptobacterium. Суммарно процесс брожения можно выразить в виде следующего уравнения:
С6Н12О6 + 2 Фн + 2 АДФ → 2 С3Н6О3 + 2 АТФ
глюкоза лактат
Гомоферментативное молочнокислое брожение, так же как и спиртовое, протекает по фруктозодифосфатному пути до пирувата, который принимает на себя водород окисляемого субстрата и под действием фермента НАД-зависимой лактатдегидрогеназы превращается в молочную кислоту:
С6Н12О6
→
2 СН3–СО–СООН
![]() 2 CH3–CHOH–COOH
2 CH3–CHOH–COOH
глюкоза пируват лактатдегидрогеназа лактат
В процессе как спиртового, так и гомоферментативного молочнокислого брожения можно выделить три типа биохимических реакций:
– перестройку углеводного скелета (расщепление 6-углеродного соединения до двух 3-углеродных);
– окислительно-восстановительные превращения;
– образование АТФ.
Как видно из суммарного уравнения, с точки зрения энергетического выхода процессы спиртового и гомоферментативного молочнокислого брожения одинаковы.
1.2.3. Гетероферментативное молочнокислое брожение
Гетероферментативное молочнокислое брожение протекает по окислительному пентозофосфатному пути (рис. 1.7). При гетероферментативном молочнокислом брожении образуются органические кислоты (молочная и уксусная), этанол, СО2, глицерин и др. Особенностями этого брожения являются участие в процессе НАДФ+ в качестве акцептора водорода и окислительное декарбоксилирование 6-фосфоглюконовой кислоты, что приводит к образованию пентоз (рибулозо-5-фосфата и ксилулозо-5-фосфата). Образовавшиеся при расщеплении пентоз С3- и С2-фрагменты фосфокетолазной реакции претерпевают дальнейшие преобразования. 3-фосфоглицериновый альдегид в ходе ферментативных реакций, идентичных гликолитическому пути, превращается в молочную кислоту – лактат. Двухуглеродный фрагмент (ацетилфосфат) либо двухступенчато восстанавливается до этанола, либо окисляется до уксусной кислоты.
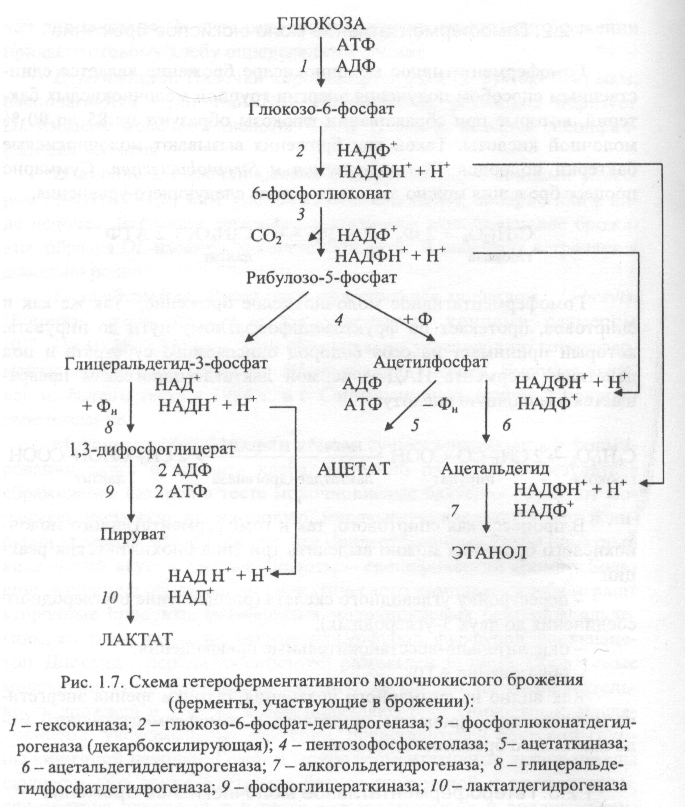
Преобладание в среде ферментации того или иного продукта зависит от вида культуры, условий культивирования, фазы развития. Гетероферментативные молочнокислые бактерии вида Leuconostoc mesenteroides сбраживают глюкозу с накоплением эквимолярных количеств лактата, этанола и диоксида углерода:
С6Н12О6 → CH3–CHOH–COOH + CH3–CH2OH + СО2
глюкоза лактат этанол
У других гетероферментативных молочнокислых бактерий, главным образом из подрода бетабактерий, которые используются в хлебопечении, в значительно больших количествах накапливается уксусная кислота.
1.3. Пропионовокислые бактерии
В 1962 г. К.Е. Бартенева предложила использовать для подавления картофельной болезни хлеба пропионовокислые бактерии, являющиеся сильными антагонистами картофельной палочки.
Пропионовокислые бактерии объединены в семейство Propioni-bacteriaceae, род Propionibacterium. Типовым представителем рода является вид Propionibacterium freudenreichii (назван по имени швейцарского бактериолога Эдварда Фрейденрайха). В группу классических пропионовокислых бактерий входят также виды P. jensenii, P. thoenii, P. acidipropionici.
Пропионовокислые бактерии представляют собой мелкие полиморфные палочки размером (1,0–5,0)(0,5–0,8) мкм. Форма клеток бывает кокковидной, булавовидной, разветвленной. Клетки располагаются чаще всего одиночно, иногда парами, в виде китайских иероглифов или букв V или Y. Пропионовокислые бактерии грамположительны, неподвижны, не образуют спор и капсул. Некоторые штаммы могут образовывать внеклеточную слизь, однако она не формируется в виде четкой капсулы.
Большинство пропионовокислых бактерий являются аэротолерантными анаэробами, получающими энергию в процессе брожения. Аэротолерантность этих бактерий обусловлена наличием у них ферментов, защищающих клетку от токсических форм кислорода: каталазы, пероксидазы и супероксиддисмутазы. Пропионовокислые бактерии могут синтезировать гемсодержащие белки, в их клетках обнаружены цитохромы. Важную роль в метаболизме пропионовокислых бактерий играет так называемое «флавиновое дыхание», в процессе которого происходит перенос двух электронов с флавопротеидов на молекулярный кислород, сопровождающийся образованием пероксида водорода. Однако энергетическая эффективность окислительного фосфорилирования у этих бактерий крайне низка, и основным способом получения энергии у них является пропионовокислое брожение.
Пропионовокислые бактерии обитают в кишечном тракте жвачных животных, встречаются в молоке, твердых сырах, силосе, забродивших маслинах.
Пропионовокислые бактерии расщепляют глюкозу по гликолитическому пути до пирувата с последующим образованием пропионовой и уксусной кислот и диоксида углерода согласно суммарному уравнению
3 С6Н12О6
4 СН3
–СН2–СООН
+ 2 СН3–СООН
+ 2 СО2 +
2 Н2О
С6Н12О6
4 СН3
–СН2–СООН
+ 2 СН3–СООН
+ 2 СО2 +
2 Н2О
глюкоза пропионовая уксусная кислота кислота
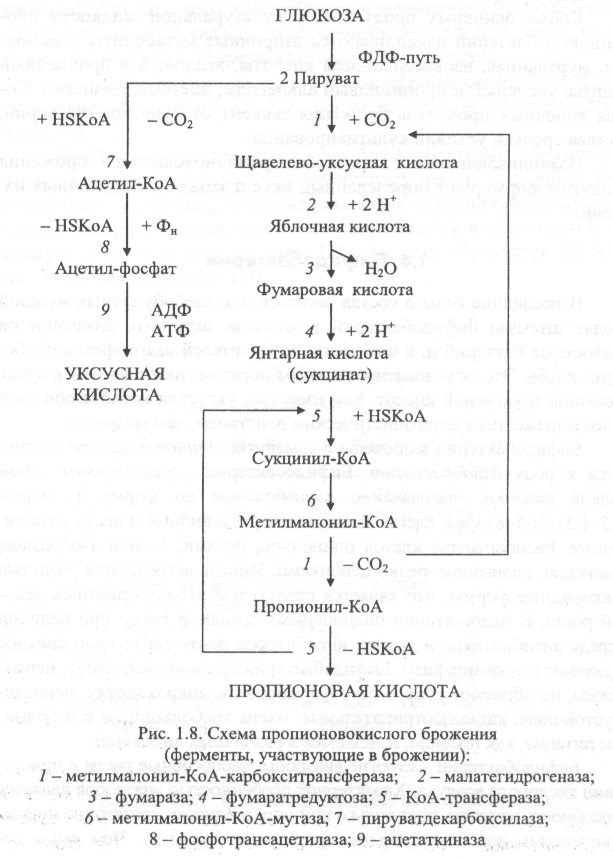
Особенностью пропионовокислого брожения является реакция присоединения к молекуле пирувата диоксида углерода, что приводит к образованию 4-углеродного соединения, т. е. С3 + С1 = С4. В реакции карбоксилирования пирувата участвует биотинзависимый фермент, у которого биотин выполняет функцию переносчика СО2 (рис. 1.8).
Последовательность реакций, показанных на рис. 1.8, приводит к образованию пропионовой кислоты. Однако пропионовокислое брожение – процесс более сложный, так как, помимо пропионовой кислоты, продуктами брожения являются уксусная, янтарная кислоты и диоксид углерода. Из схемы брожения видно, что янтарная кислота является промежуточным продуктом, но она может накапливаться в среде и как конечный продукт.
Кроме основных продуктов, в культуральной жидкости пропионовых бактерий накапливаются вторичные метаболиты – молочная, муравьиная, изовалериановая кислоты, этиловый и пропиловый спирты, уксусный и пропионовый альдегиды, ацетоин, диацетил. Состав конечных продуктов брожения зависит от культуры бактерий, состава среды и условий культивирования.
Накапливающиеся в процессе пропионовокислого брожения продукты формируют определенный вкус и запах хлебобулочных изделий.
1.4. Бифидобактерии
В последние годы в состав заквасок для хлебобулочных изделий вводят штаммы бифидобактерий в качестве активных антагонистов гнилостных бактерий и, в частности, возбудителей картофельной болезни хлеба. Это обусловлено, главным образом, накоплением в среде молочной и уксусной кислот. Как известно, уксусная кислота обладает более выраженным антагонистическим действием, чем молочная.
Бифидобактерии включены в семейство Actinomycetaceae и относятся к роду Bifidobacterium. Бифидобактерии представляют собой мелкие палочки, чрезвычайно вариабельные по форме, размером (0,5–1,3)(1,5–8) мкм, слегка изогнутые, булавовидные и часто разветвленные. Расположение клеток одиночное, парами, V- или Y-об-разное, розетками, палисадом, редко цепочками. Иногда встречаются раздутые кокковидные формы, что является следствием неблагоприятных условий роста. В недостаточно полноценных средах, а также при наличии в среде антибиотиков и других ингибиторов роста характерно сильное ветвление и полиморфизм. Бифидобактерии грамположительны, неподвижны, не образуют спор, могут формировать микрокапсулу, некислотоустойчивы; каталазоотрицательные; очень требовательны к источникам питания; как правило, нуждаются в различных витаминах.
Бифидобактерии – строгие анаэробы, неспособные расти в присутствии кислорода воздуха. Характерной особенностью анаэробов является способность начинать рост только при определенном, достаточно низком окислительно-восстановительном потенциале среды Eh. Чем выше содержание О2 в среде, тем выше Eh. Рост бифидобактерий при наличии в среде растворенного кислорода возможен лишь при добавлении в среду редуцирующих веществ (например, 0,05 % цистеина; 0,2 % аскорбиновой кислоты). В связи с этим бифидобактерии выращивают на среде Блаурока, основой которой является отвар печени, богатый цистеином, или на гидролизатно-молочной среде, в которую вносят цистеин.
Оптимальная температура роста бифидобактерий 37–41 °С, оптимальное значение рН 6,0–7,0; они не растут при рН ниже 4,5 или выше 8,5.
На плотных питательных средах бифидобактерии образуют колонии в виде «гвоздиков» или гречишных зерен. Бифидобактерии сбраживают углеводы по так называемому фосфокетолазному пути, в ходе которого 2 моля глюкозы превращаются в молочную и уксусную кислоты в соотношении 2:3, при этом образуется 2,5 АТФ на 1 моль глюкозы (рис. 1.9).
2 Глюкоза






 Фруктозо-6-фосфат
Фруктозо-6-фосфат
Фруктозо-6-фосфат
Фруктозо-6-фосфат




 Эритрозо-4-фосфат
+ Ацетил-фосфат
Эритрозо-4-фосфат
+ Ацетил-фосфат

 Рибозо-5-фосфат
+ Ксилулозо-5-фосфат
Рибозо-5-фосфат
+ Ксилулозо-5-фосфат




2 Глицеральдегид-3-фосфат 2 Ацетилфосфат


2 СН3–СНОН–СООН 2 СН3–СООН СН3–СООН
2 Лактат 2 Ацетат Ацетат
Рис. 1.9. Схема сбраживания углеводов бифидобактериями