Материал: А27483 Красникова ЛВ Кострова ИЕ Машкин ДВ Микробиология производства хлеба кондит и макарон изделий
1.1.2. Классификация дрожжей
Дрожжи относятся к царству грибов Mycetaliа. Их классификация основана на морфологических признаках, системе физиологических тестов, деталях полового и вегетативного размножения. На основании наличия и характера полового процесса дрожжи относят к трем классам грибов: аскомицетам (Askomycetes), базидиомицетам (Basidiomycetes) и дейтеромицетам несовершенным (Deuteromy-cetes) – рис. 1.2.
Царство Mycetalia → Подцарство Mycobionta →
→ Отдел Eumycota → Подотдел Eumycotina →
→ Классы




-
Аскомицеты (Askomycetes)
Базидиомицеты (Basidiomycetes)
Дейтеромицеты (Deuteromycetes)
Подкласс
Подкласс
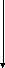
Hemiaskomycetidia
Heterobasidiomycetes
Порядок
Порядки
Endomycetales

Ustilaginalеs Tremellales Tilletiales
С
 емейства
емействаFilobasidiales
Семейства

Saccharomycetaceae Schizosaccharomycetaceae Endomycetaceae и др.
Сandidaceae
Cryptococcaceae
Sporobolomycetaceae
Рис. 1.2. Классификация дрожжей
Дрожжи классифицируют в первую очередь по способу полового размножения, т. е. споруляции. Споры аскомицетных дрожжей образуются посредством конъюгации клеток противоположных типов спаривания, мейотического деления ядра диплоидной клетки и формирования аска. В базидиомицетных дрожжах сложный половой цикл заканчивается образованием базидиоспор, которые принимают форму почкующихся дрожжей. Споруляция редко встречается среди базидиомицетных дрожжей. Более того, почти для половины описанных дрожжей ничего не известно о половых процессах, которые протекают в анаморфном (незаконченном или несовершенном) состоянии в противоположность телеоморфным (законченным или совершенным) состояниям полового размножения.
Несовершенные дрожжи – это либо анаморфы известных аскомицетовых или базидиомицетовых дрожжей, либо виды, у которых отсутствует или не обнаружена половая стадия размножения. Их аффинитет может быть установлен по ряду признаков, которые позволяют судить о филогенетических связях этих дрожжей с аскомицетами или базидиомицетами. На этом основании выделены семейство Candidaceae с признаками аскомицетового аффинитета и два семейства с признаками базидиомицетового аффинитета: Cryptococcaceae (не образуют баллистоспор) и Sporobolomycetaceae (образуют баллистоспоры)
В хлебопечении используют дрожжи видов Saccharomyces cerevisiae и Saccharomyces minor, относящиеся к роду Saccharomyces семейства Saccharomycetaceae. Все остальные виды дрожжей являются посторонними, контаминирующими биотехнологический процесс на разных его стадиях.
1.1.3. Размножение дрожжей
Дрожжи семейства Saccharomycetaceae размножаются почкованием, семейства Schizosaccharomycetaceae – делением, а дрожжи семейства Saccharomycodaceae размножаются почкованием, завершающимся делением.
Почкование - это вегетативный способ размножения дрожжей. Различают следующие способы вегетативного размножения дрожжей:
– мультилатеральное почкование (как у Saccharomyces), почка образуется на различных участках поверхности дрожжевой клетки;
– биполярное почкование (как у Наnseniaspora), почкование происходит последовательно от каждого полюса клетки поочередно;
– бинарное деление (как у Schizosaccharomyces), материнская клетка удлиняется, ядро делится, новые ядра перемещаются к полюсам клетки, эти две почки разделяются перегородкой с последующим формированием стенок и разделением их на две самостоятельные клетки (рис. 1.3).
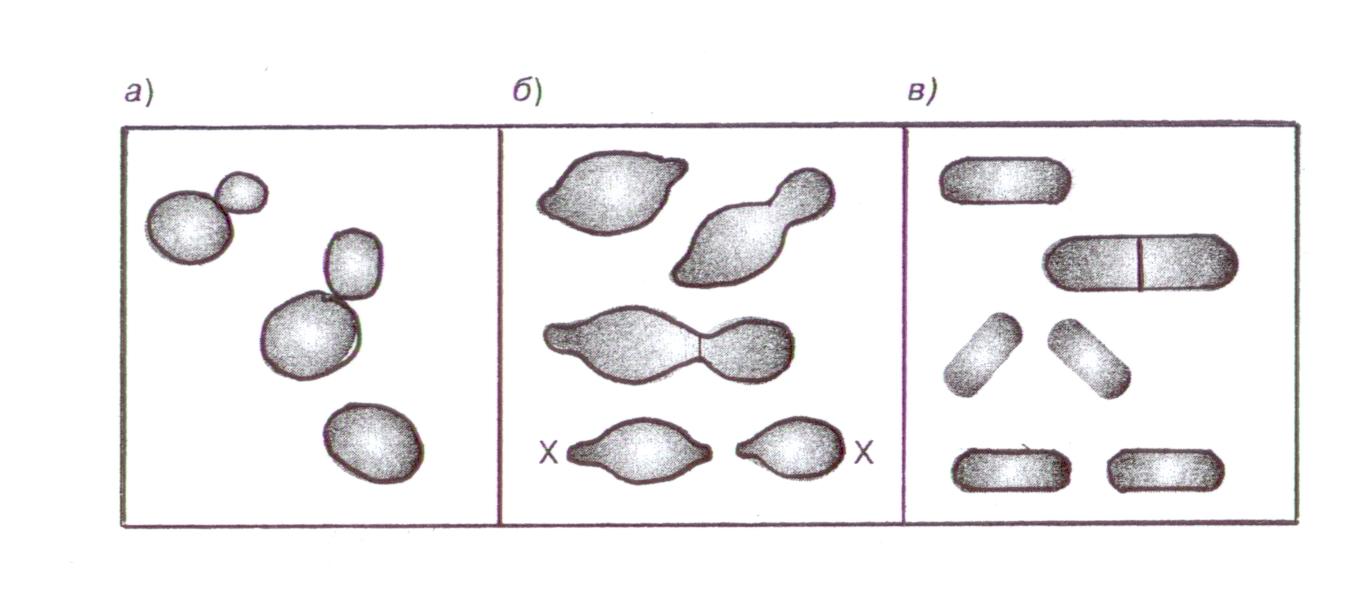
а б в
Рис. 1.3. Вегетативное размножение дрожжей:
а – мультилатеральное почкование; б – биполярное почкование; в – бинарное деление
Время, за которое клетка образует себе подобную, называется клеточным циклом. Он включает в себя четыре основные стадии, длительность которых примерно одинакова:
G1 - предсинтетическая фаза. Она начинается с синтеза ферментов, необходимых для синтеза почки и дубликации ДНК. Образованию почки предшествуют сложные внутриклеточные процессы: гидролиз полисахаридов клеточной стенки и ее размягчение, активация фермента хитинсинтетазы и биосинтез хитина, который входит в состав почечной перегородки. Фаза заканчивается наклевыванием почки;
S - синтетическая фаза. Там, где почка соединена с клеткой, постепенно образуется сужение – перетяжка. По достижении размера почки примерно 1/3 размера материнской клетки ядро перемещается в перетяжку;
____________
Микробиология пива /Ф. Дж. Прист, И. Кэмпелл: Пер. с англ.; Под общ. ред. Т.В. Мелединой и Тыну Сойдла. – СПб.: Профессия, 2005. – 368 с.
G2 - постсинтетическая фаза. В течение этой фазы происходит дальнейшее увеличение размера почки. Идет распределение ядерного материала между материнской и дочерней клетками;
М - митоз. Ядро делится; одно из ядер остается в материнской клетке, другое переходит в почку;
(С) - цитокинез. Перетяжка постепенно сужается, заканчивается образование хитинового слоя, и примерно через 2 ч молодая дочерняя клетка отделяется от материнской. Отделение дочерней клетки происходит лишь тогда, когда разделяются слои перегородки, оставляя на материнской клетке почковый рубец.
Дочерние клетки не всегда отделяются от материнских, они также размножаются почкованием, в результате образуются скопления из многих клеток.
Деление дрожжевой клетки происходит аналогично делению бактерий: после деления ядра появляется поперечная перегородка, что приводит к образованию двух дочерних клеток, идентичных материнской.
Saccharomyces cerevisiae обладает хорошо охарактеризованным жизненным циклом, в гаплоидной и диплоидной фазах которого клетки могут размножаться почкованием (рис. 1.4). Штаммы, у которых гаплоидная фаза стабильна и может поддерживаться в течение длительных генераций, получили название гетероталлических.
Вегетативные клетки противоположных типов спаривания (a и a) сливаются, в них происходят последовательные процессы плазмогамии (слияние цитоплазм двух клеток) и кариогамии (слияние ядер). В результате образуется зигота – диплоидная клетка с двойным набором хромосом. В благоприятных условиях диплоидные клетки стабильны и могут неограниченное время размножаться почкованием. Они крупнее и активнее гаплоидных. В случае голодания или других неблагоприятных условий клетка приступает к спорообразованию. Диплоидное ядро делится путем мейоза на четыре–восемь частей, после чего формируются аскоспоры. Процесс образования и созревания аско-спор длится 15–48 ч. Клеточная стенка дрожжей изменяется, и клетка превращается в аск (сумку). Обычно в аске содержатся четыре аско-споры, однако встречаются также аски с двумя и тремя спорами. Споры дрожжей имеют более толстую и прочную оболочку, чем вегетативные клетки. Они довольно устойчивы к неблагоприятным внешним факторам (температуре, высушиванию, рН и др.), но менее термостабильны по сравнению с бактериальными спорами и погибают при температуре 80 °С.
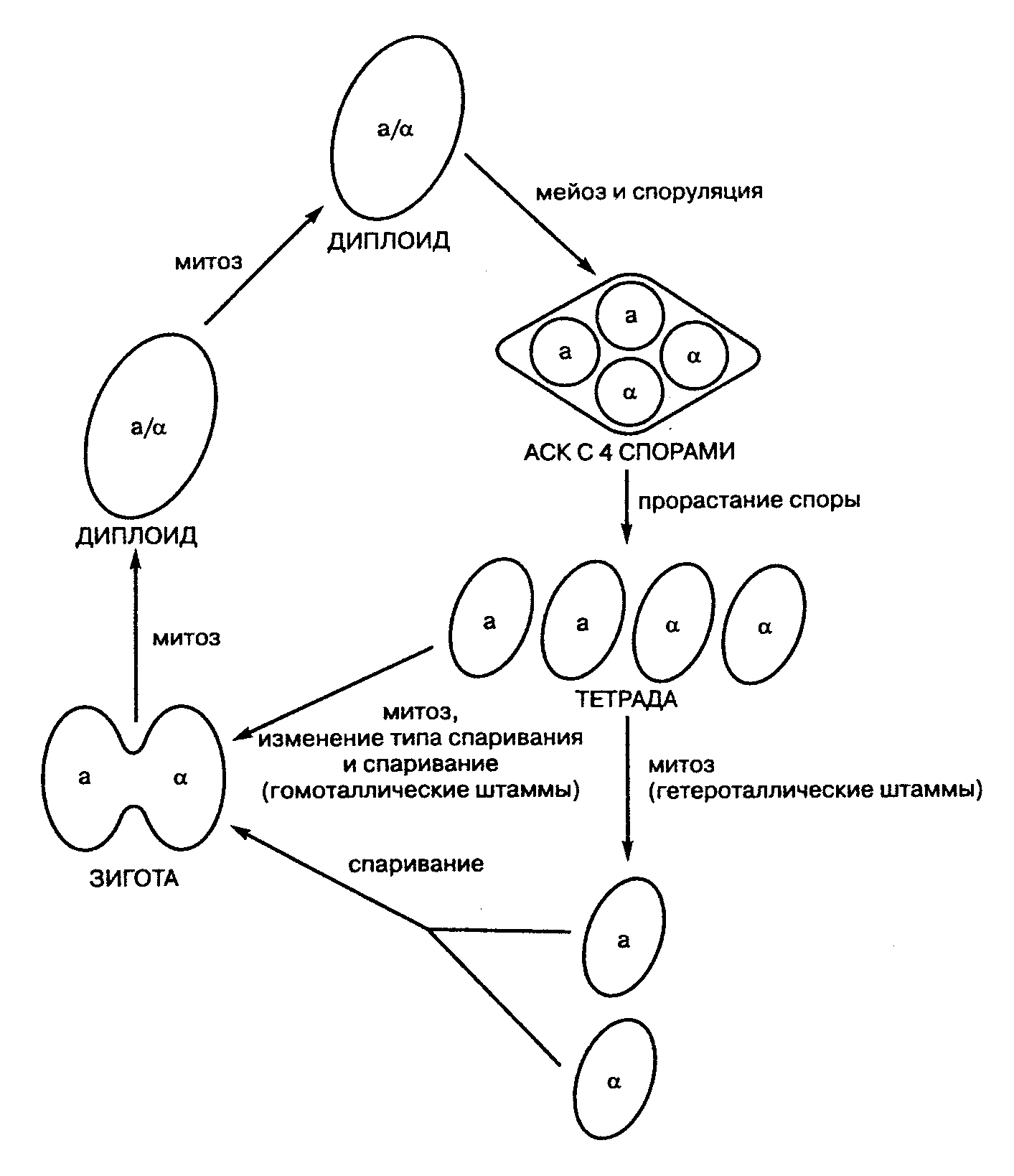
Рис. 1.4. Жизненный цикл развития дрожжей сахаромицетов
В благоприятных условиях аскоспоры прорастают в гаплоидные клетки, которые далее размножаются почкованием. Быстрое прорастание аскоспор наблюдается только в среде, содержащей легко доступные источники углерода, такие, как глюкоза или фруктоза.
У культурных дрожжей, развитие которых происходит на богатых углеводами средах, способность к спорообразованию значительно ослаблена или полностью утрачена. Восстановить способность дрожжей образовывать споры можно принудительным путем, культивируя их на обедненных питательными веществами средах.
__________________
Микробиология пива /Ф. Дж. Прист, И. Кэмпелл: Пер. с англ.; Под общ. ред. Т.В. Мелединой и Тыну Сойдла. – СПб.: Профессия, 2005. – 368 с.
1.1.4. Характеристика дрожжей, используемых в хлебопекарном производстве
Дрожжи хлебопекарные представляют собой технически чистую культуру Sacсharomyces cerevisiae, используемую в изготовлении изделий из пшеничной и ржаной муки. Дрожжи вида Saccha-romyces minor участвуют только в брожении теста из ржаной муки.
Вид Saccharomyces cerevisiae
Морфологические признаки. Клетки дрожжей данного вида имеют овальную, округлую, яйцевидную или слегка удлиненную форму размером (5–6)(10–14) мкм. Молодые активные клетки при микроскопировании имеют тонкую прозрачную оболочку и гомогенную, без видимых включений, цитоплазму, небольшую вакуоль. Иногда в цитоплазме встречаются зерна полифосфатов. В более зрелых клетках оболочка утолщается, цитоплазма становится зернистой, число и размеры вакуолей увеличиваются. При старении культуры в цитоплазме клеток появляются капли жира в виде круглых, резко преломляющих свет блестящих включений.
Культуральные признаки. Колонии на сусле-агаре белые, круглой формы с ровными краями и выпуклым центром, с гладкой тускло-блестящей поверхностью, диаметром 0,5–1,0 см. Иногда встречаются колонии со складчато-шероховатой поверхностью, бугристые. Культуры дрожжей, образующие шероховатые колонии, характеризуются пониженной бродильной активностью.
При росте на жидком солодовом сусле дрожжи этого вида образуют небольшой осадок желтовато-белого цвета.
Физиологические признаки. Дрожжи данного вида сбраживают глюкозу, галактозу, сахарозу, мальтозу, частично раффинозу и простые декстрины солодового сусла; не сбраживают лактозу, ксилозу, арабинозу, крахмал и клетчатку. Оптимальная температура развития - около 30 °С; оптимальное значение рН находится в диапазоне 4,6–5,0. Концентрации сахара свыше 15 %, хлорида натрия свыше 1,5 %, этилового спирта свыше 5 % угнетают жизнедеятельность дрожжей. При содержании в среде спирта 12–14 % брожение практически прекращается.
Вид Saccharomyces minor
Морфологические признаки. Клетки мелкие, круглые, диаметром 1,5–3,0 мкм с характерным почкованием: почки располагаются на одном из концов клетки. При выращивании дрожжей в жидкой среде почки образуются на обоих концах клеток или по две почки на одном конце.
Культуральные признаки. На сусле-агаре образуют мелкие серовато-белые колонии с ровными краями и приподнятым цент-ром, диаметром 0,4–0,8 см. Поверхность колоний гладкая, блестящая. В солодовом сусле образуют небольшой осадок серовато-белого цвета, который при взбалтывании легко взмучивается.
Физиологические признаки. Сбраживают и усваивают глюкозу, галактозу, сахарозу, раффинозу; не сбраживают лактозу, ксилозу, арабинозу, крахмал, клетчатку. Характерной особенностью дрожжей данного вида является отсутствие у них способности сбраживать мальтозу и простые декстрины. Тем не менее, они хорошо размножаются в ржаных заквасках, что объясняется наличием в ржаной муке свободных сахаров, а также обеспечением доступных углеводов в результате действия ферментов муки и молочнокислых бактерий.
Оптимальная температура роста 25–28 °С. При повышенных температурах (32–35 °С) скорость размножения этих дрожжей снижается.
По бродильной активности дрожжи S. minor уступают виду S. cerevisiae, но они менее требовательны к источникам азотного и витаминного питания, более кислотоустойчивы и способны размножаться в среде с рН 3,0–3,5.
В хлебопекарном производстве используют разные штаммы дрожжей вида S. сerevisiae. Штаммами (или расами) называют микроорганизмы одного вида, выделенные из разных источников или из одного источника, но в разное время, различающиеся между собой по некоторым признакам, ценным для данного производства.
Технологические свойства дрожжей оцениваются на основании их ферментативной активности по следующим показателям:
– количеству выделенного диоксида углерода (манометрический метод);
– скорости сбраживания сахаров;
– кислотности, стойкости, осмочувствительности, активности протеиназ, содержанию трегалозы, эргостерина.
Наиболее важными производственными свойствами дрожжей являются подъемная сила, мальтазная и зимазная активность, осмочувствительность.
П о д ъ е м н о й с и л о й называют время, необходимое для подъема стандартного теста на высоту 70 мм от дна стандартной формочки. Подъемная сила дрожжей удовлетворительного качества не должна превышать 70 мин. Этот показатель характеризует способность сбраживания собственных сахаров муки, что является следствием активности только зимазного комплекса ферментов дрожжей. Однако при определении подъемной силы не учитывается активность фермента ά-глюкозидазы, который индуцируется дрожжами при дефиците глюкозы и сахарозы и наличии мальтозы в среде.
З и м а з н о й и м а л ь т а з н о й а к т и в н о с т ь ю называют продолжительность выделения 10 см3 диоксида углерода при сбраживании дрожжами 5 %-го раствора глюкозы и мальтозы соответственно.
Показатели как зимазной активности, так и подъемной силы характеризуют практически один и тот же процесс – сбраживание глюкозы зимазным комплексом дрожжей без учета сбраживания мальтозы.
Прессованные дрожжи по показателю мальтазной активности оцениваются согласно данным табл. 1.1.
Таблица 1.1