Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Глава 7. ОБЛАСТИ ПРИМЕНЕНИЯ ПОЛИОКСИАЛКАНОАТОВ
Полиоксиалканоаты, как уже было отмечено, по ряду физикохимических свойств сходны с синтетическими полимерами (полипропиленом, полиэтиленом). Помимо термопластичности, полиоксиалканоаты обладают оптической активностью, антиоксидантными свойствами, пьезоэлектрическим эффектом и, что самое главное, биоразрушаемостью и биосовместимостью. Полиоксиалканоаты чрезвычайно различаются между собой по структуре и свойствам (гибкости, кристалличности, температуре плавления и др.) в зависимости от таксономического положения и физиолого-биохимических свойств микроорганизмов-продуцентов, условий биосинтеза и типа углеродного субстрата. Более того, недавно продемонстрированные возможности получения на основе ПОА композитов с различными природными и синтетическими материалами, позволяющие направленно изменять их структуру, состав и, следовательно, базовые свойства материала – пластичность, механическую прочность, температурные и другие характеристики, еще более усиливают привлекательность ПОА и расширяют возможные сферы применения.
Линейная структура молекул ПОА придает им свойство термопластичности и изменения прочности (возрастание по направлению растяжения). При нагревании молекулярные цепи в ПОА легко сдвигаются относительно друг друга, в результате этого материал размягчается и приобретает текучесть. Данное технологическое свойство имеет большую коммерческую ценность, так как позволяет с использованием различных методов (прессования, экструзии и др.) получать из ПОА разнообразные изделия и материалы. Гомогенный полиоксибутират по механическим свойствам сходен с полипропиленом и полистерином, однако обладает лучшими газобарьерными свойствами (например, по отношению к кислороду) и большей устойчивостью к ультрафиолету, характеризуется также хорошей водостойкостью и теплоустойчивостью, при этом проницаемость для водяного пара через него втрое ниже по сравнению с полипропиленом.
Из ПОА возможно получение гибких пленок различной толщины, в том числе полупроницаемых мембран, нитей, нетканых материалов, различных полых форм (бутыли, контейнеры, коробки и пр.), а также гелей и клеев. Совокупность характерных свойств делает их перспективными для применения в различных сферах, – медицине, фармакологии, пищевой и косметической промышленности, сельском и коммунальном хозяйстве, радиоэлектронике и других сферах (Abe, Doi, 1992; Brandle et al., 1990; Luzier, 1992; Muller, Seebach, 1993 et al.) (рис. 7.1).
245
Рис. 7.1. Продукция из Биопола
(Asrar and Grauys, 2002).
Масштабы применения полиоксиалканоатов в настоящее время сдерживаются достаточно высокой стоимостью (практически на порядок более высокой, по сравнению с полиолефинами). Однако возрастающие требования к охране окружающей среды, с одной стороны, и имеющиеся перспективы снижения стоимости биополимеров за счет повышения эффективности производства, с другой, делают полиоксиалканоаты одним из перспективных материалов XXI века.
Уже сейчас сферы применения полиоксиалканоатов – самые различные. Данные материалы активно исследуются с целью переработки в США, Скандинавии и Европе, особенно в Германии и Голландии. Совет объединенной Европы утвердил концепцию необходимости замены не разрушаемых синтетических пластиков биодеградируемыми полимерами, а с 1993 г санкционировано применение упаковочной продукции из ПОА в пищевой промышленности.
7.1. Использование полиоксиалканоатов в медицине
Развитие науки приводит к все более широкому внедрению в медицине высокомолекулярных соединений, в том числе синтезируемых живыми системами, то есть биополимеров (Amass et al., 1998; Angelova, Hunkeler, 1999). Разнообразие полимеров, варьирование в широких пределах их стереоконфигурации и молекулярной массы, возможность получения композитов в разнообразных сочетаниях с различными веществами, – все это является основой для получения широчайшего спектра новых материалов с новыми ценными свойствами (Gregor, 1975; Kronenthal et al., 1975; «Полимеры медицинского назначения», 1981;
Платэ, Васильев, 1985; Williams, 1987; Alper, 1991; Адамян, 1994; Amass et al., 1998; «Биосовместимость», 1999; Nasseri et al., 2001).
246
Среди применяемых и активно разрабатываемых в настоящее время биоматериалов – алифатические полиэфиры, полиамиды, сегментированные полиэфируретаны, полимеры молочной и гликолевой кислот (полилактиды и полигликолактиды), силикон, полиэтилентерефталат (ПЭТФ) и с недавних пор – полимеры оксипроизводных жирных кислот (полиоксиалканоаты, ПОА) (Amass et al., 1998; More and Sauders, 1998; Биосовместимость, 1999; Sudesh et al., 2000).
Сферы применения полиоксиалканоатов в медицине потенциально широки и могут включать сердечно-сосудистую хирургию, ортопедию, урологию, стоматологию и др. (Amass et al., 1998; Madison, Huisman, 1999; Williams et al., 1999; Sudech, Doi, 2000; Stock et al., 200l; Asrar and Gruys, 2002). Особенно перcпективным считается применение ПОА в клеточной и тканевой трансплантологии для реконструктивной хирургии тканей и создания биоискусственных орга-
нов (Williams and Martin, 2002):
Сформировавшееся в последние годы мультидисциплинарное направление биоматериаловедения и трансплантологии – тканевая инженерия, остро нуждается в специализированных биосовместимых материалах. Тканевая инженерия ориентирована на создание конструкций, обеспечивающих восстановление, укрепление и улучшение функций тканей (Mooney and Vacanti, 1993; Williams et al., 1999; Heath, 2000; Humacher, 2000; Sodian et al., 2000; Nasseri et al., 2001). Мате-
риалы, применяемые в тканевой инженерии, должны обладать спектром специальных свойств. Прежде всего, продукты деградации материала не должны быть токсичными, конструкция должна сохранять свою форму и обладать достаточной прочностью до тех пор, пока новая ткань организма-хозяина в месте имплантации полностью не восстановится; материал, применяемый для изготовления конструкции, не должен быть иммунногенным, он должен поддерживать рост клеток и организацию их в ткань, в свою очередь, сам имплантат должен беспрепятственно отводить продукты обмена клеток.
Техника получения биоактивных имплантатов и биоискусственных органов включает: 1) изготовление биосовместимых и биоабсорбируемых конструкций (инкубаторов) для культивирования аутологических клеток пациента или клеток, взятых из банка, 2) выращивание клеток и формирование тканей in vitro и 3) последующую имплантацию полученных конструкций пациенту (рис. 7.2).
Применение таких биоконструкций, дополнительно нагруженных лекарственными препаратами (антибиотиками, гормонами, витаминами, белковыми факторами и др.), является революционным направлением в реконструктивной и прецизионной хирургии и в трансплантологии и имеет огромные перспективы.
247
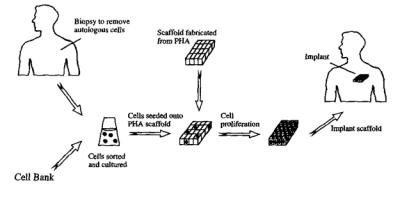
Рис. 7.2. Применение ПОА в тканевой инженерии (Williams et al., 1999).
Ключевой проблемой для успеха создания таких биоконструкций является наличие адекватного биодеградирующего и биосовместимого материала. В настоящее время ПОА рассматриваются в качестве особо перспективного материала для изготовления матриц при конструировании тканевых протезов и биоискусственных органов. Наиболее многообещающим представляется использование этих полимеров для регенерации поврежденных кожных покровов, изготовления имплантатов кровеносных сосудов и клапанов сердца, закрытия дефектов мягких и костных тканей.
7.1.1. Сердечно-сосудистая хирургия
В настоящее время основное биомедицинское применение ПОА ориентировано на конструкции для сердечно-сосудистой хирургии. Одним из наиболее разработанных направлений является использование полиоксибутирата (ПОБ) в качестве нетканых лоскутов для закрытия дефекта перикарда в постоперационном периоде для предотвращения спаечного процесса (Bowald and Johansson, 1990; Malm et al., 1992a, b).
Группа сотрудников Медицинского университета и отделения торакальной и сердечно-сосудистой хирургии госпиталя г. Ланда в Швеции под руководством профессора Малма исследовала возможность снижения осложнений, имеющих место после операций на открытом сердце, за счет имплантирования полимерных лоскутов из ПОБ в качестве временного перикарда (Malm et al., 1992a, b). Животных (были взяты овцы) наблюдали в течение 2.5 лет относительно контроля (у животных после иссечения участка перикарда перикардиальная полость была оставлена открытой). В ходе опыта у экспериментальных животных развития спаечного процесса между сердцем и грудиной не отмечено (рис. 7.3). Показано, что в ответе тканей на имплантацию ПОБ принимали участие многоядерные макрофаги. По мере формирования новой ткани на фоне деструкции полимерного лоскута в многоядерных макрофагах было отмечено наличие включений частичек ПОБ. С применением СЭМ выявлено, что на перикардиальной поверхности регенерированной ткани со стороны сердца сформировался мезотелеподобный слой, который полностью покрывал подлежащий слой коллагена.
248
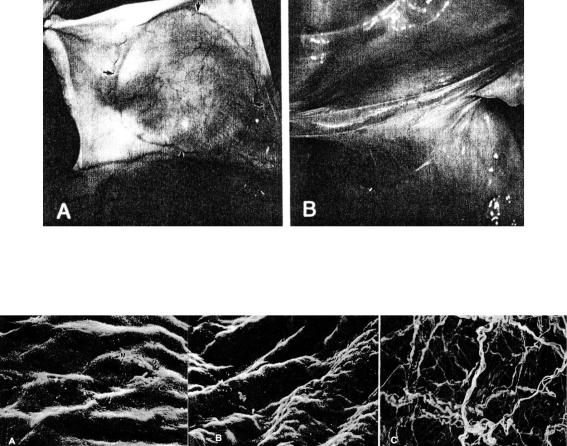
Рис. 7.3. Макроскопические снимки фрагментов тканей в месте имплантации: A – 12 месяцев после имплантации модельного перикарда из ПОВ, место регенерированных тканей отмечено стрелками; спаечный процесс отсутствует; B – развитие спаечного процесса через 12 месяцев после операции, перикард был оставлен открытым (Malm et al., 1992а).
Рис. 7.4. Электронные микрофотографии ткани перикарда после операции:
(A) – поверхностный слой регенерированной ткани из мезотелеобразующих клеток спустя 24 месяца после операции в месте имплантации лоскута из ПОБ; (В) – вид нормальной ткани нативного перикарда, (аналогичен А);
(C) – поверхность ткани перикарда в контрольной группе (слой мезотелия отсутствует)
(Malm et al., 1992а).
Морфология поверхности вновь сформированных тканей была сходной с нативным перикардом (рис.7.4).
В следующей работе авторов (Malm et al., 1994) биодеградируемые нетканые пленочные лоскуты из ПОБ были имплантированы в правый вентрикулярный тракт и легочную артерию овцам. В контрольной группе животным имплантированы лоскуты из дакрона. Животных наблюдали в течение 3–12 месяцев после операции. Регенерированный сосуд на основе ПОБ имел сходные структурные и биохимические показатели с нативными тканями.
Исследованы имплантаты – протезы легочной артерии и створок клапана легочной артерии, изготовленные из ПОА. Экспериментальным животным имплантировали полимерные трубочки, засеянные аутоклетками из сонной артерии, контрольным – полимерные трубочки без клеток. У контрольных животных произошла окклюзия имплантатов на разных постоперационных сроках. В опытных группах все имплантаты оставались функционирующими до конца наблюдения (рис. 7.5).
249