Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
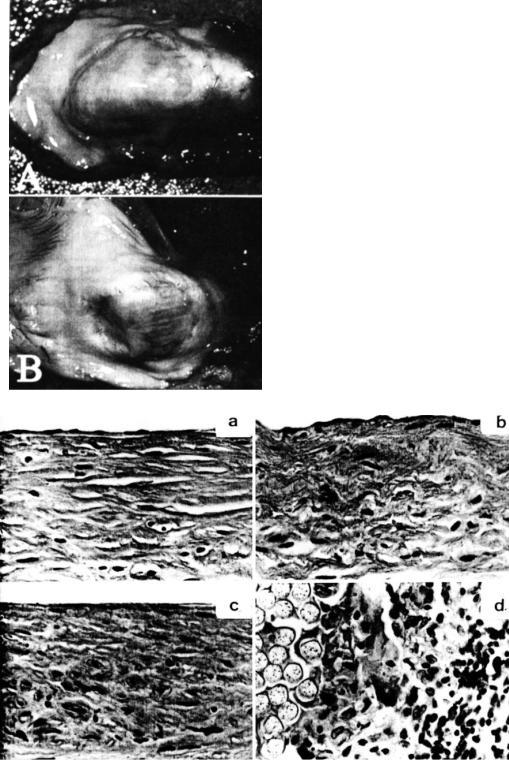
Рис. 7.5. Макроскопические фотографии тканей в месте имплантации:
А – спустя 12 месяцев после имплантации лоскута из ПОБ, отчетливо видна регенерированная ткань внутри тракта оттока, видны нормальные вновь сформированные ткани в месте имплантации; Б – спустя 12 месяцев после имплантации
лоскута из дакрона, виден тонкий слой неонтимы (Malm et al., 1994).
Рис. 7.6. Снимки срезов тканей в месте имплантации: а – регенерированная ткань спустя 9 месяцев после имплантации лоскута из ПОБ, видна единичные клетки;
b – срез нативной ткани легочной артерии, структура аналогична тканям на срезе (а); c – неонтима, сформированная спустя 12 месяцев в месте имплантации дакрона; d – регенерированные ткани в месте имплантации дакрона спустя 9 месяце, видна
выраженная клеточная инфильтрация в тканях, прилегающих в имплантату из дакрона. Окраска по Ван-Гизону. Увеличение 400 (Malm et al., 1994).
250
Гистологическими исследованиями зафиксировано образование в среднем слое эластиновых волокон и специфического эндотелиального фактора Виллибранта на поверхности пластин.
В работе (Nkere et al., 1998) проведены более сложные наблюдения в экспериментах на телятах, которые были подвергнуты шунтирующей операции на сердце. При этом ПОБ был использован в качестве перикардиального лоскута. Однако, в данной работе существенных отличий в постоперационном ответе тканей у экспериментальных животных в сравнении с контрольными (полимерный имплантат отсутствовал, перикардиальная полость была оставлена открытой) отмечено не было.
Сотрудниками отделения грудной и сердечно-сосудистой хирургии университетского госпиталя г. Упсалы (Швеция) исследованы экспериментальные образцы перикардов, изготовленные из ПОБ (Duvernoy et al., 1995). Группе пациентов из19 человек, подвергшимся операциям на открытом сердце, были имплантированы модельные перикарды, изготовленные из ПОБ. С помощью компьютерной томографии эти пациенты на сроке 6 и 24 месяца после операции были обследованы на наличие спаечного процесса в области опера-
ции (рис. 7.7).
У больных с ПОБ-имплантатом было отмечено достоверно низкое возникновение осложнений в виде спаечного процесса между лоскутом ПОБ и поверхностью сердца по сравнению с контрольной группой, представленной пациентами, которым лоскуты из ПОБ не имплантировали. В ходе наблюдений площадь модельных перикардов постепенно замещалась вновь образованными тканями по мере деструкции полимера. При этом в ходе наблюдения отмечено наличие жировой клетчатки между имплантатом и поверхностью сердца. У больных, которым после аналогичной операции полимерный перикард не имплантировали, были отмечены множественные спаечные осложнения (Duvernoy et al., 1995).
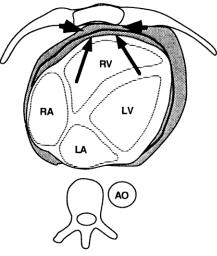
Рис. 7.7. Схематический показ проведения компьютерного сканирования сердца. Показано отсутствие/или наличие жировой ткани в загрудинной области (короткие стрелки) и жировая ткань в эпикардии (длинные стрелки). Правый желудочек (RV), левый желудочек (LV), левое предсердие (LA), нисходящая аорта (AO) (Duvernoy et al., 1995).
251
Нетканые лоскуты, изготовленные из полиоксибутирата, исследованы для ликвидации дефектов межпредсердной перегородки в эксперименте на телятах (Malm et al., 1992c). Зафиксировано образование сформированных эндотелиальных слоев со стороны правого и левого предсердий с субэндотелиальным слоем коллагена и гладкомышечными клетками. Как и в других работах, полимерные лоскуты постепенно деградировали с участием полинуклеарных фагоцитирующих макрофагов, в которых спустя 12 месяцев присутствовали фрагменты ПОБ. По мере биодеградации лоскута из ПОБ формировалась ткань, сходная с таковой у нативной межпредсерной перегородки, достаточно прочная для предотвращения развития шунта между предсердиями.
Как известно, применение металлических стентов в кардиохиругии сопряжено с возникновением осложнений в виде рестенозов вследствие разрастания сосудистой стенки. В этой связи ПОА исследуются в качестве потенциального материала для изготовления биоабсорбируемых стентов, в том числе в комбинации с системами доставки лекарственных средств (Peng et al., 1996). В работе (Van der Giessen et al.,1996) испытан cополимер оксибутирата и оксивалерата в виде полосок, нанесенных на поверхность витых металлических стентов, которые были имплантированы в коронарные артерии (диаметром 2.5–3.0 мм) свиней. В ходе опыта данные имплантаты сравнивали с другими абсорбируемыми полимерами, типа полилактидов и полигликолидов. Через 4 недели в месте имплантации сополимера ПОБ-со-ПОВ, аналогично другим биоматериалам, отмечена выраженная воспалительная реакция и фиброцеллюлярная пролиферация тканей. Следует отметить, что имплантаты не были простерилизованы перед операцией. Эти результаты отличаются от реакции клеток на данные материалы in vitro, вероятно, вследствие того, что in vivo на характер ответа тканей влияют многие дополнительные факторы, такие как форма имплантата, место имплантации, характер продуктов деструкции материала и др.
Изготовленные из полиоксибутирата сосудистые стенты (Schmitz and Behrend, 1997) теcтированы в эксперименте на кроликах (Underdorden et al., 1998). В последствие были изготовлены более эластичные стенты с использованием в качестве пластифицирующего агента триэтил цитрата; поверхность стентов была также обработана лазерной резкой (Behrend, 2000b). Стенты были имплантированы в артерии кроликам и вызывали незамедлительную реакцию сосудистой интимы. Отмечено, что материал стентов деградировал достаточно быстро. Однако в одной из последних работ в ходе сравнительного исследования ПОБ-стентов в сравнение с танталовыми конструкциями получены отрицательные результаты (Unverdorben et al., 2002). Так, при имплантации стентов, изготовленных из ПОБ, в
252
подвздошную артерию кроликам наблюдали выраженную воспалительную реакцию, повышенную продукцию коллагена, а также сужение и повреждение стенок сосудов.
Полиоксиалканоаты исследуются также в качестве материала для изготовления сосудистых протезов. Последние имплантируются для восстановления или пересадки поврежденных и подверженных риску сосудов. Протезы сосудов крупного диаметра предварительно пропитываются белками. Однако в ходе эксплуатации таких протезов возможно проявление и развитие нежелательных иммунологических реакций.
Следует отметить, что еще до планомерных медико-биологичес- ких исследований полиоксиалканоатов, которые были развернуты в конце 80-х – начале 90-х годов, в одной из первых работ (Baptist and Ziegler, 1965) была показана возможность использования 3-поли- оксибутирата для восстановления кровеносных сосудов.
В настоящее время с целью улучшения функциональных свойств применяемых сосудистых протезов, получаемых из синтетических материалов, предпринята попытка использования для их по-
крытия сополимера 3-ПОБ-со-4-ПОБ (Noisshiki and Komatsuzaki,
1995). Такие сосудистые протезы были имплантированы собакам и исследованы на сроке 2 и 10 недель. Отмечено, что деградация полимера началась уже на второй неделе. В работах (Marois et al, 1999с; 2000) оценен в качестве пропитывающего покрытия синтетических протезов эластичный сополимер оксигексаноата и оксиоктаноата (3-ПОГ-со-3-ПОО). В эксперименте на крысах проведено сравнение эффективности сосудов, пропитанных данным полиоксиалканоатом и белком, а также флюорополимером на сроке от 2 до 180 суток. Внутри сосудов, покрытых ПОА, не отмечено инфильтрации ткани. При этом обнаружено, что деградация полимера происходила очень медленно. Так, молекулярная масса полимера снизилась за 6 месяцев эксперимента всего на 30 %. Ответ тканей на имплантацию таких протезов был очень мягким. Имплантаты, изготовленные из данного сополимера, исследованы в качестве протеза легочной артерии и створок клапана легочной артерии в экспериментах на ягнятах (Shum-Tim et al., 1999). Экспериментальным животным в качестве протеза имплантировали полимерные трубочки (диаметр 7 мм), изготовленные из сетчатого полилактида, на поверхность которых был нанесен слой 3-ПООГ-со-3-ПОО. Имплантаты предварительно были засеяны аутоклетками из сонной артерии, и после подращивания клеток были имплантированы животным. Контрольной группе имплантировали полимерные трубочки без клеток. У контрольных животных в течение первых недель отмечено развитие аневризм и окклюзия имплантатов. В экспериментальной группе полимерные имплантаты, засеянные клетками, оставались функциональными в
253
течение всего периода наблюдения. Зафиксировано образование в среднем слое формирующейся ткани эластиновых волокон и специфического эндотелиального фактора Виллибранта. Осложнений в виде развития аневризм или стриктур не отмечено. Механическая прочность испытуемых протезов сосуда была сопоставима с нативными сосудами (Shum-Tim et al., 1999). Результаты данного опыта резко отличаются от аналогичных исследований модельных сосудистых протезов, изготовленных из композита синтетических полилак- тид-полигликолида. При использовании последних отмечена быстрая деструкция данного пористого композита и развитие аневризм в течение нескольких недель после операции.
Следует отметить, что самые удачные результаты применения ПОА в сердечно-сосудистой хирургии получены в ходе их исследования в качестве клапанов сердца, сконструированных по технологии клеточной и тканевой инженерии. Имеющиеся на сегодняшний день результаты тестирования ПОА позволяют надеяться, что применение полиоксиалканоатов в этой области позволит в ближайшее время снять проблему, существующую при использовании механических и животных клапанов. При применение последних необходимо применение антикоагулянтной терапии, возникает необходимость также в повторных операциях для замены отработанных клапанов и их замены, например, у растущих детей. Как установлено, тканно-инженерные конструкции полимерных клапанов в результате развития из засеянных клеток новых тканей и удлинения имплантанта по мере роста детей и увеличения массы сердца соответствуют данному процессу во времени, что исключает необходимость повторных имплантаций. Следует отметить также, что абсорбируемые жесткие синтетические материалы, такие, как полигликолактиды, пригодны только для изготовления двустворчатых клапанов и не пригодны для изготовления трехстворчатых клапанов, например, клапанов легочных артерий.
В работе (Stock et al., 2000) получены положительные результаты при сравнительном испытании на животных моделей легочных шунтов, изготовленных из полиоксиоктаноатa (ПОО), в сравнении с полилактидными имплантатами. Трехстворчатые полимерные трубочки, засеянные аутологическими срединными клетками эндотелия in vitro, после семидневного подращивания клеток были имплантированы овцам. В ходе постоперационного периода антикоагулянты прооперированным животным не вводили. Функцию клапанов оценивали в динамике в течение 24 недель с использованием эхокардиографии. Параллельно проводили гистологические и биохимические исследования. У опытных животных наблюдали формирование нормально организованной ткани. Образования тромбов в ходе всего эксперимента не отмечено. Молекулярная масса полимерного имплантата при этом
254