Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
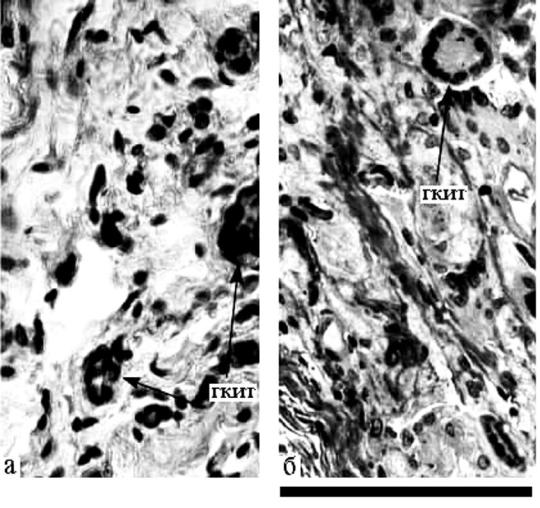
Рис.6.17. Гигантские многоядерные клетки инородных тел с упорядоченным кольцевидным расположением ядер (ГКИТ) в тканях, окружающих ПОБ-нити:
2 (а) и 16 (б) недель после имплантации. Полутонкий срез. Толуидиновый синий. Маркер 0,01 мм. (Шишацкая, 2003)
Через 8 недель гистологическая картина в зоне имплантации ПОБ
иПОБ-со-ПОВ практически не изменилась, равно как и толщина капсул
иих клеточный состав. Капсулы пронизаны сосудами микроциркуляторного русла (рис. 6.18); в них преобладали коллагеновые волокна зрелого типа (рис. 6.16). В зоне, примыкающей к ПОБ и ПО-со-ПОВ, попрежнему регистрировалось большое количество активных макрофагов. Их количество было сопоставимо с показателями активности КФ в сыворотке крови животных (рис. 6.12). Увеличение активности КФ свидетельствует об усиление фагоцитарной реакции макрофагов, являющихся, как установлено недавно, одним из активных агентов биодеструкции ПОА (Williams and Martin, 2002). В структуре ФК, окружающих имплантаты из ПОБ и ПОБ-со-ПОВ, идентифицированы активные фибробластические элементы и формирующиеся коллагеновые волокна.
240
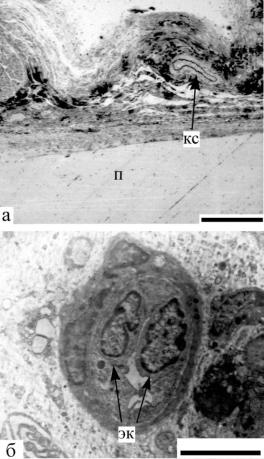
Рис. 6.18: а – полутонкий срез. Кровеносный сосуд (кс) во вновь образованной ткани вокруг ПОБ-нити (п) (4 недели после операции).
Маркер 0,01 мм.
б – формирующийся сосуд микроциркуляционного типа в фиброзной капсуле (8 недель после перации).
Обозначения: эк – эндотелиальные клетки. Маркер 5 мкм.
(Шишацкая, 2003).
Средняя толщина капсул (ТК) вокруг ПОБ и ПОБ-со-ПОВ составила на этом сроке, соответственно, 161.20 ± 5.93 и 158.08 ± 4.37 мкм; рядность фибробластов (РФ) – 9.50±0.57 и 10.57±0.67. Это было сопоставимо с ТК вокруг шелка на этом сроке (рис. 6.19б) (173.17±5.46 мкм), однако увеличения количества макрофагальных клеток вокруг шелка не отмечено. В тканях, окружающих кетгут, попрежнему отмечены лейкоцитарные клетки; толщина фиброзной капсулы составила 514.21±12.01 мкм (рис. 6.19А).
Спустя 16 недель после операции вокруг шовных нитей зафиксировано значительное истончение капсул (рис. 6.11), до 54.09 ± 3.28 и 43.71 ± 3.11 мкм вокруг ПОБ и ПОБ-со-ПОВ, соответственно, при снижении РФ в них до 4.64 ± 0.37 и 3.36 ± 0.37. Однако количество активных макрофагов в тканях, примыкающих к ПОА-имплантатам, по-прежнему высоко (табл. 6.10). Отмечены макрофаги непосредственно на полимерных нитях (рис. 6.16), появились ГКИТ с 10–12 ядрами (рис. 6.17). Среди фибробластических элементов преобладали зрелые клетки. В периферических частях капсул наблюдалось образование зрелой соединительной ткани в виде пучков коллагеновых волокон и прилегающих к ним цепочек фиброцитов. Здесь же определялись активные фагоцитирующие макрофаги и ГКИТ. Это позволяет предположить миграцию продуктов деструкции материала.
241
А |
Б |
В |
1
2
3
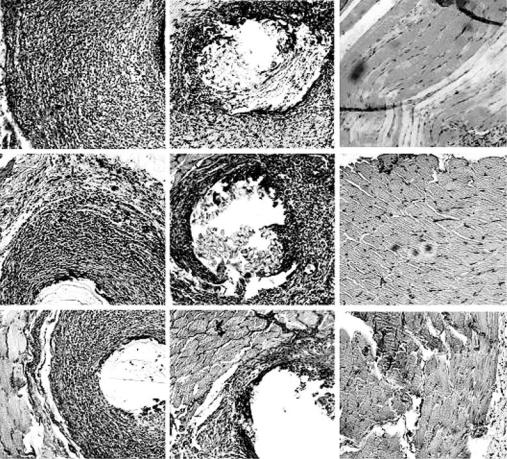
Рис. 6.19. Морфология тканей вокруг имплантатов из кетгута (А), шелка (Б) через 8, 16 и 24 недели после операции, соответственно, 1, 2 и 3 (обозначено слева).
Мышечная ткань у интактных животных на этих же сроках. Гематоксилин–эозин. Маркер – 0,01 мм
(из неопубликованных данных Шишацкой).
Через 24 недели после операции была отмечена дальнейшая инволюция фиброзных капсул вокруг имплантированных нитей из ПОБ и ПОБ-со-ПОВ (рис. 6.11); ТК уменьшились до 48.02 ± 5.25 и 33.73 ± 2.05 мкм, соответственно. В капсулах преобладали зрелые коллагеновые волокна, в них по-прежнему присутствовали активные фагоцитирующие макрофаги. Вокруг шелка значительного истончения фиброзных капсул не наблюдали; к концу эксперимента ТК составили 125–132 мкм. В месте имплантации кетгута, несмотря на активную деструкцию (к 4 мес. он не определялся в тканях), плотные капсулы сохранялись. Через 16 и 24 недели после имплантации ТК составили,
соответственно, 342,00 ± 9,68 и 272,14 ± 4,11 мкм (рис. 6.19). Пучки коллагеновых волокон в ФК вокруг кетгута были гораздо толще и занимали практически весь объем капсулы (рис. 6.20).
242
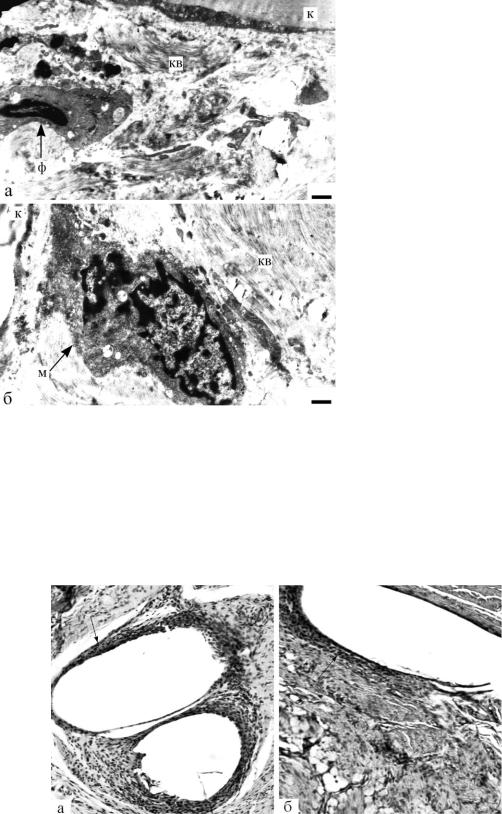
Рис. 6.20. Ультратонкий срез тканей вокруг кетгута: а и б – пучки коллагеновых волокон (кв) (8 и 16 недель после операции). Обозначения:
м – макрофаги, ф – фиброциты. Маркер – 1 мкм (Шишацкая, 2003)
Дальнейшее наблюдение за состоянием тканей у животных, которым были имплантированы нити из ПОБ и ПОБ-со-ПОВ, не выявило неблагоприятных явлений в прилегающих тканях. Спустя 36 недель ТК вокруг нитей из полиоксиалканоатов составляла 20–40 мкм. Имплантаты были окружены здоровыми тканями из вновь сформированных волокон, ориентированных вокруг нитей.
Через 48 недель толщина фиброзных капсул не превышала 5–10 мкм (рис. 6.21). В непосредственной близости с нитями – по-прежнему значительное количество моно- и полиядерных макрофагальных клеток.
Рис. 6.21. Морфология тканей вокруг ПОБ-со-ПОВ спустя 36 (а) и 48 (б) недель после имплантации. Гематоксилин – эозин. Маркер – 0,01 мм (Volova et al., 2003a).
243
Таким образом, установлено, что воспалительная и регенераторная реакции тканей животных на имплантаты из ПОА, на всем протяжении эксперимента, независимо от химического состава материала, была одинаковой. Присутствие оксивалерата в полимере не изменяло длительности и интенсивности воспаления, а также характера развития фиброзной капсулы вокруг нитей. В течение двенадцати месяцев наблюдения в месте имплантации ПОА обоих типов неблагоприятных проявлений в виде гнойного воспаления, некроза, кальцификации и малигнизации фиброзных капсул не отмечено.
В целом, выполненные комплексные исследования полиоксиалканаотов и изделий из них в условиях in vitro и in vivo свидетельствуют о высоких медико-биологических свойствах данного материала. Это позволяет рекомендовать данный класс биодеградируемых полимеров для создания био- и гемосовместимых изделий медицинского назначения, в том числе, и в качестве матриц в биоискусственных органах.
244