Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Для анализа биохимических перестроек, сопровождающих морфологические изменения в тканях после операции и имплантации нитей, исследованы в динамике активность фосфомоноэстераз, кислой (КФ) (рис. 6.12–6.13) и щелочной фосфатаз (ЩФ) (рис. 6.14– 6.15), которые наиболее ярко реагируют на повреждение тканей (Salthouse, 1976). ЩФ, присутствующая в основном в нейтрофилах, является показателем процессов воспаления, а также неоваскуляризации (Музыкант, Дудникова, 1975; Salthouse, Matlaga, 1975); КФ макрофагов и гигантских клеток инородных тел (ГКИТ) служит показателем интенсивности биодеструкции полимерных материалов
(Пхакадзе с соавт., 1982; Burpee et al., 1978).
Активность КФ в сыворотке крови у всех оперированных животных была выше по сравнению с интактным контролем (рис. 6.12). На всех сроках наблюдения активность КФ в III (кетгут), IV (ПОБ-со-ПОВ) и V группах (ПОБ) была выше, чем у животных II группы (шелк). Между экспериментальными (IV и V группами), начиная с 4 недели, различия активности КФ были достоверными; при этом активность фермента у животных, которым были имплантированы нити из ПОБ- со-ПОВ, была выше. Это согласуется с результатами по биодеградации ПОА в биологических средах, где ПОБ-со-ПОВ деградируют более активно по сравнению с ПОБ.
Активность ЩФ в первые две недели у всех оперированных животных была существенно (в 2.0–2.5 раза) выше относительно интактных животных (рис. 6.14). Внутри групп между оперированными животными самые высокие значения ЩФ, достоверно отличающиеся от положительного контроля (шелк) и экспериментальных групп, зафиксированы у животных, раны которых были ушиты кетгутом. Повышение активности ЩФ у этой группы животных наблюдали на более поздних сроках (до 8 недель), в то время, как у всех других оперированных животных значения ЩФ нормализовались к 4 неделе. Между IV и V экспериментальными группами по данному показателю достоверные отличия зафиксированы только на 2 неделю после операции.
Результаты биохимических и гистохимических исследований согласуются между собой (Рис. 6.12–6.15).
На 7 день после операции на фоне воспаления в области операции и имплантации нитей из обоих типов ПОА было отмечено значительное повышение уровня ЩФ в прилегающих тканях (рис. 6.15a). Аналогичная реакция отмечена вокруг шелка и существенно более выраженная – в месте имплантации кетгута. Активность КФ в этот период в тканях, прилегающих к имплантатам всех типов, в т. ч. из ПОБ-со-ПОВ, гистохимически существенно не проявлялась (рис. 6.13a). Это согласуются с невысоким уровнем макрофагов в тканях в этот период (2–3 п/зр) (таблица 6.10).
235
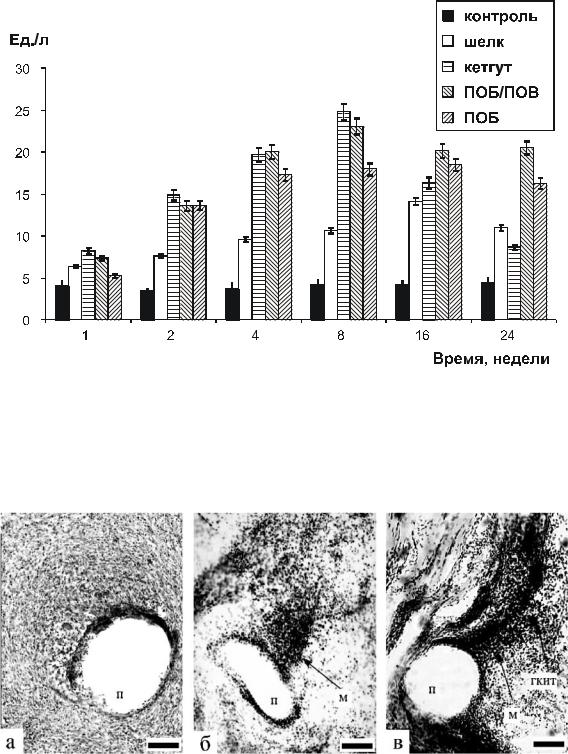
Рис. 6.12. Динамика активности кислой (КФ) фосфатазы сыворотки крови крыс в хроническом эксперименте (Шишацкая с соавт., 2002е).
Рис. 6.13. Гистохимическая реакция тканей на кислую фосфатазу (КФ) по Гомори: 1(а), 2(б) и 4(в) недели после имплантации ПОБ-нити. Маркер – 0,01 мм.
Обозначения: п – полимерная нить, м – макрофаги, ГКИТ – гигантские клетки инородных тел (Шишацкая с соавт., 2002 е).
236
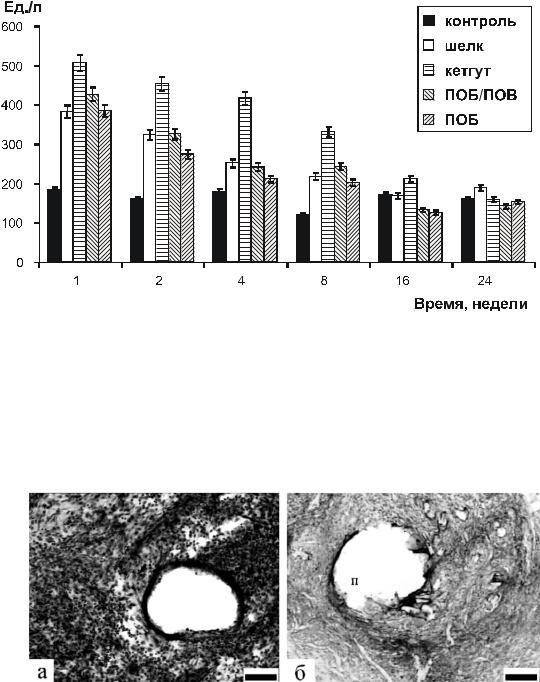
Рис. 6.14. Динамика активности щелочной фосфатазы (ЩФ) в сыворотке крови крыс в хроническом эксперименте (Шишацкая с соавт., 2002 е).
Рис. 6.15. Гистохимическая реакция тканей на щелочную фосфатазу (ЩФ) по Гомори: 1(а) и 4(б) недели после имплантации ПОБ-нити. Маркер – 0,01 мм.
Обозначения: п – полимерная нить (Шишацкая с соавт., 2002 е).
237
Микроскопическая картина в месте имплантации ПОБ и ПОБ-со- ПОВ на 7 сутки после операции характеризовалась незначительным отеком тканей вокруг имплантированных нитей и единичными тонкими зонами некроза (рис. 6.11). Шовные нити были окружены преимущественно макрофагами и лимфоцитами, а также нейтрофилами и фибробластами. Отмечено начало формирования вокруг имплантатов фиброзных капсул. Реакция тканей вокруг экспериментальных нитей из ПОА по силе воспаления была сопоставима с реакцией тканей на шелк и значительно менее выражена по сравнению с реакцией на кетгут.
Через 2 недели после операции признаки воспаления уменьшились, незначительная отечность тканей вокруг всех имплантатов сохранялась (рис. 6.16); в зоне воспаления по-прежнему встречались лейкоцитарные клетки. В сформировавшихся вокруг ПОБ и ПОБ-со-ПОВ капсулах отмечено увеличение количества зрелых макрофагов секреторно-фагоцитарного типа, в среднем, соответственно, до 6.36 ± 0.42 и 5.50 ± 0.40 в п/зр. Для них характерно смещение складчатого ядра к одному из полюсов клетки, развитый комплекс Гольджи, довольно много митохондрий овальной или вытянутой формы. Значительная часть цитоплазмы макрофагов занята лизосомами и фагосомами; внешняя клеточная мембрана образует толстые короткие и пальцевидные выпячивания. Макрофаги сгруппированы, как правило, на внутренней стороне капсул, примыкающих к нитям. Среди окружающих тканей отмечены единичные гигантские клетки инородных тел с 4–6 ядрами (рис. 6.17). Гистохимически зарегистрировано увеличение в цитоплазме макрофагов количества гранул кислой фосфатазы. Это коррелировало с ее активностью в сыворотке крови, увеличившейся на этом сроке до 13 ед./л (рис. 6.12). В капсуле вокруг кетгута, в отличие от шелка, также отмечено увеличение количества макрофагов (табл. 6.10).
Через 4 недели после операции толщина фиброзных капсул вокруг имплантатов из ПОБ и ПОБ-со-ПОВ увеличилась до 172.23 ± 13.64 и 169.67 ± 5.97 мкм. Это было сопоставимо с ТК вокруг шелка и в 2 раза меньше, чем ТК вокруг кетгута. Продолжало увеличиваться количество активных, с большим количеством выростов и клеточных лизосомальных структур макрофагов (до 11–12 в п/зр) и ГКИТ, а также активность КФ в них (рис. 6.13в).
Капсулы вокруг ПОА-имплантатов, в основном, были представлены фибробластами и коллагеновыми волокнами, которые начинали формироваться в пучки (рис. 6.11 и 6.16).
238
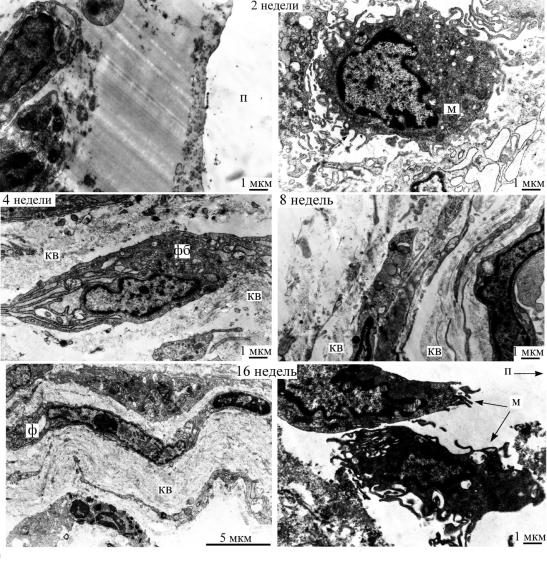
Рис. 6.16. Ультратонкие срезы участков фиброзных капсул, формирующихся вокруг имплантированных нитей из ПОА на разных сроках.
Обозначения: п – полимерная нить, м – макрофаги, я – ядро, аг – аппарат Гольджи, фб – фибробласты, ф – фиброциты, кв – коллагеновые волокна
(Volova et al., 2003a).
239