Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Таблица 6.7 Показатели общетоксического действия водных вытяжек ПОАв опыте на белых
мышах (М* ± m) (Севастьянов с соавт., 2001)
|
1 группа |
2 группа |
3 группа |
4 группа |
|
Показатель |
интактный |
положитель- |
|||
ПОБ |
ПОБ/ПОВ |
||||
|
контроль |
ный контроль |
|||
|
|
|
|||
Масса тела (г): |
|
|
|
|
|
исходная |
21.20 ± 0.14* |
22.24 ± 0.13 |
23.54 ± 0.20*** |
23.60 ± 0.19*** |
|
конец опыта |
24.10 ± 0.32 |
25.07 ± 0.45 |
26.33 ± 0.36 |
26.10 ± 0.39 |
|
Масса органов (г): |
|
|
|
|
|
печень |
1.19 ± 0.04 |
1.20 ± 0.03 |
1.24 ± 0.05 |
1.21 ± 0.04 |
|
селезенка |
0.15 ± 0.01 |
0.14 ± 0.01 |
0.15 ± 0.00 |
0.15 ± 0.01 |
|
почки |
0.33 ± 0.02 |
0.34 ± 0.01 |
0.34 ± 0.03 |
0.35 ± 0.02 |
|
легкие |
0.20 ± 0.02 |
0.20 ± 0.02 |
0.21 ± 0.02 |
0.21 ± 0.02 |
|
сердце |
0.15 ± 0.00 |
0.16 ± 0.01 |
0.14 ± 0.00 |
0.17 ± 0.01** |
*– достоверное отличие между 1 и 2 группами (0.99);
**– достоверное отличие между 3 и 4 группами;
***– достоверное отличие 3 и 4 групп от 2 группы.
Таблица 6.8 Морфология периферической крови мышей на 7 день после введения
вытяжек(М* ± m) (Севастьянов с соавт., 2001)
|
1 группа |
2 группа- |
3 группа |
4 группа |
|
Показатель |
(интактный |
(положитель- |
|||
ПОБ |
ПОБ-со-ПОВ |
||||
|
контроль) |
ный контроль) |
|||
|
|
|
|||
Эритроциты,109/мл |
8.05 ± 0.03 |
7.99 ± 0.04 |
8.00 ± 0.03 |
7.99 ± 0.04 |
|
Лейкоциты,109/мл: |
7.65 ± 0.06 |
7.57 ± 0.08 |
7.57 ± 0.06 |
7.67 ± 0.07 |
|
палочкоядерные, % |
2.50 ± 0.52 |
3.57 ± 0.48 |
4.00 ± 0.69** |
6.71 ± 0.58*** |
|
сегментоядерные, % |
48.00 ± 2.30 |
54.00 ± 2.14 |
46.71 ± 2.52 |
49.00 ± 2.28 |
|
лимфоциты, % |
40.50 ± 2.42 |
39.43 ± 1.95 |
41.43 ± 2.53 |
37.62 ± 2.34 |
|
моноциты, % |
9.00 ± 0.67 |
7.86 ± 0.80 |
7.86 ± 0.46 |
6.72 ± 0.71 |
|
|
|
|
|
|
** – достоверное отличие между 3 и 4 группами (0.99);
***-достоверное отличие 3 и 4 групп от 2 группы;
В конце эксперимента перед забоем животных определяли иммунотоксичность ПОА по фагоцитарной активности макрофагов перитонеальной жидкости испытуемых животных. Фагоцитарная активность макрофагов во всех экспериментальных группах была сопоставима с контролем. Результаты показали отсутствие иммунотоксического эффекта со стороны ПОБ и сополимеров ПОБ-со-ПОВ
Токсикологическое и биологическое действие ПОА (в виде моножильных шовных нитей) изучено в хроническом опыте длительностью 6 мес. на белых крысах линии Вистар (Шишацкая, 2003; Ши-
225

шацкая с соавт., 2003 а; г; Volova et al., 2003). Экспериментальные образцы шовных нитей, изготовленные Ю. П. Некрасовым по методике (Gordeev et al., 2001) из образцов ПОА, синтезированных в Институте биофизики СО РАН, имели следующие характеристики (таблица 6.10). Перед имплантацией нити автоклавировали.
Были взяты половозрелые самки с исходной массой 180–200 г, по 18 животных в каждой группе: I – отрицательный (интактный) контроль; II – положительный контроль (хирургический шелк), III – биодеградируемая нить сравнения (кетгут), IV – экспериментальная нить ПОБ-со-ПОВ (включение оксивалерата 15 мол. %), V – экспериментальная нить ПОБ. Животным под ингаляционным наркозом (диэтиловый эфир) в асептических условиях на наружной поверхности правого бедра делали линейный продольный разрез кожи и мышцы длиной 2 см. На мышцу накладывали три одиночных узловых шва из испытуемого материала (общая длина 3.0–3.5 см), кожную рану ушивали шелком (Шишацкая с соавт., 2002 а, б, г).
Таблица 6.9 Оптическая плотность раствора с лизированными перитониальными
макрофагами мышей в эксперименте (Dопыт) относительно контроля (Dконтр.) Севастьянов с соавт.., 2001)
Наименование образцов |
Dопыт/Dконтр |
|
|
ПОБ |
6.8 ± 1.1/7.1 ± 0.8 |
|
|
ПОБ-со-ПОВ |
|
(включение оксивалерата – 15 мол. %) |
6.9 ± 0.8/7.1 ± 0.7 |
|
|
Таблица 6.10 Характеристики экспериментальных образцов шовных нитей из ПОА ( М* ± м)
(Волова с соавт., 2003)
Показатель |
ПОБ |
ПОБ-со-/ПОВ |
||
|
|
|
||
Абсолютная разрывная нагрузка (Fр), Н |
7.10 ± 0.21 |
9.40 ± 0.19 |
||
|
|
|
||
Коэффициент вариации по нагрузке, % |
16.4 ± 1.82 |
3.00 ± 2.12 |
||
|
|
|
|
|
Прочность при разрыве, МПа |
205 |
± 31 |
274 |
± 27 |
|
|
|
|
|
Относительное разрывное удлинение, % |
27.80 |
± 1.02 |
37.70 |
± 1.74 |
|
|
|
||
Коэффициент вариации по удлинению, % |
12.1 ± 1.46 |
6.5 ± 0.81 |
||
|
|
|
||
Модуль упругости, ГПа |
3.75 |
3.13 |
||
|
|
|
|
|
*– среднее из 10 измерений |
|
|
|
|
226
Впериферической крови (забор из хвоста) с использованием общепринятых методов проводили развернутый анализ крови, определяли СОЭ, содержание гемоглобина и форменных элементов. В крови, забранной у наркотизированных животных из левого желудочка сердца, определяли биохимические показатели. С использованием серийных наборов реагентов для клинических исследований в сыворотке крови анализировали общее содержание и фракции белка, остаточный азот, мочевину, креатинин и активность ферментов: лактатдегидрогеназы (ЛДГ), кислой и щелочной фосфомоноэстераз (КФ, ЩФ), аланин- и аспартаттрансфераз (АЛТ и АСТ).
Исследование лимфоидной ткани («имплантационный тест») проводили патоморфологическим анализом отпечатков паховых лимфатических узлов животных (2 и 4 недели после имплантации); анализировали строение ЛУ и соотношение популяций иммунокомпетентных клеток. В середине (8 недель) и в конце эксперимента (24 недели) проводили макро- и микроскопические исследования внутренних органов (печени, почек, сердца, селезенки и легких). Оценивали общую гистоархитектонику внутренних органов (окраска гема- токсилин-эозином). Реакцию тканей на ПОА исследовали общепринятыми гистологическими методами; для этого спустя 1, 2, 4, 8, 16 и 24 недели после операции из бедренной мышцы животных иссекали фрагмент тканей с имплантатами. После фиксации в 10 % формалине материал заключали в парафин; из блоков готовили срезы толщиной 5–10 мкм. Анализировали общую реакцию ткани на имплантированные экспериментальные нити (окраска гематоксилинэозином) и процессов развития коллагеновых волокон (окраска пикрофуксином по Ван-Гизону) в сравнении с таковыми при имплантации шелковой нити и кетгута. С использованием Image Analysis System «Carl Zeiss Jena» проводили анализ изображений и морфометрические исследования срезов.
Втечение эксперимента все животные, которым были имплантированы нити из ПОБ и ПОБ-со-ПОВ, были здоровы и активны, равномерно прибавляли в весе. Достоверных изменений по сравнению с двумя контрольными группами обнаружено не было. Относительные массы внутренних органов у животных экспериментальных групп также не отличались от таковых в контроле. Макроскопические исследования внутренних органов у всех животных на всех сроках наблюдения отклонений не выявили (Шишацкая с соавт., 2002а; Шишацкая, 2003).
Анализ морфологического состава периферической крови в контрольных и опытных группах показал, что в основном эти показатели находились в пределах физиологической нормы и не отличались существенно у животных экспериментальных групп относительно контролей. Незначительное повышение количества лейкоцитов (от
10–11 до 12.5–13.0 109/л) и уровня СОЭ (до 3.0–3.5) отмечены на
227
седьмые сутки после оперативного вмешательства у всех оперированных животных относительно интактных. Лейкоцитоз на данном сроке у животных, раны которых были ушиты кетгутом, был достоверно (p = 0,05) выше относительно обеих экспериментальных групп и сохранялся на более поздних сроках (2 и 4 недели после операции). Достоверное повышение СОЭ отмечено только на первом наблюдаемом сроке и только у животных III и V групп относительно отрицательного контроля. Далее показатель был в границах физиологической нормы у всех животных. В лейкоцитарной формуле экспериментальных животных на всех сроках наблюдения достоверных систематических изменений не выявлено.
Биохимические исследования во всем комплексе показателей, не выявили между группами животных достоверных отклонений, выходящих за пределы физиологических величин (Шишацкая с соавт., 2002б). Анализ динамики содержания мочевины, креатинина и остаточного азота в сыворотке крови свидетельствуют об отсутствии негативного влияния имплантированных полимерных нитей на показатели азотного обмена и функцию почек животных. Содержание белка в сыворотке крови, а также его фракционный состав во всем массиве данных не выявили патологических изменений. Исключение составило достоверное падение величины «альбумины/глобулины» у всех оперированных животных (до 0.77 ± 0.02 – 0.81 ± 0.01) относительно интактных (0.89 ± 0.01 – 0.91 ± 0.02). Однако это изменение имело место только на первом сроке наблюдения (одна неделя после операции) и отражало наличие постоперационного воспаления; далее величина была сопоставима с контролем. Динамика активности АЛТ и АСТ как показателя дезинтоксикационной функции печени была в пределах физиологической нормы у всех животных в течение всего опыта
Выраженные изменения зарегистрированы у оперированных животных в показателях активности лактатдегидрогеназы в сыворотке крови. В течение первых двух недель у всех оперированных животных (2–5 группы) по сравнению с интактным контролем был повышен уровень лактатдегидрогеназы. В первую неделю после операции показатель у всех оперированных животных был выше более, чем в 3–4 раза по сравнению с интактной группой. Более выраженными изменения были у животных, раны которых были ушиты кетгутом. (рис. 6.8). На 14-е сутки после операции активность ЛДГ снизилась, а через 8 недель практически сравнялась с интактным контролем.
228
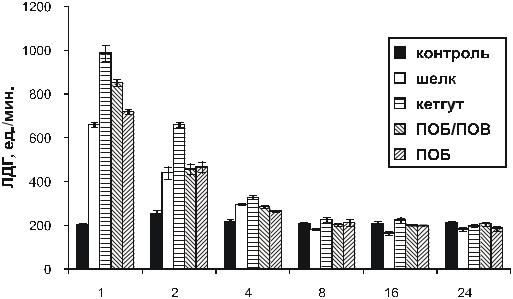
Рис. 6.8. Динамика активности лактатдегидрогеназы (ЛДГ)сыворотки крови крыс в хроническом эксперименте (Шишцкая с соавт., 2000 б).
Изменение активности ЛДГ отражает, как известно, биохимические изменения в тканях, имеющие место на стадии повреждения и связанные, наряду с высвобождением кислых липидов и их перекисным окислением, с активацией реакций гликолиза, которые сопровождаются накоплением в тканях молочной кислоты и ацидозом (Воспаление, 1981; Шехтер, Серов,1995).
Для определения степени влияния имплантированных полимерных нитей на органы иммунитета и выявления возможной сенсибилизации иммунокомпетентных систем животных исследована реакция лимфоидной ткани (Шишацкая с соавт., 2000б). Проанализированы макро- и микроскопические характеристики паховых правых (регионарных по месту имплантации) и левых (отдаленных) лимфоузлов (ЛУ). Во всех группах животных через 2 и 4 недели после начала эксперимента ЛУ имели плотно-эластическую консистенцию, бобовидную форму с гладкой поверхностью. Размеры ЛУ лежали в переделах 0.15 0.18 – 0.25 0.35 см. При микроскопии рисунок ЛУ сохранен; изменений средней площади лимфоидных узелков и в соотношении между корковым веществом и паракортикальной зоной не выявлено. Достоверных систематических изменений в соотношении клеточных популяций ЛУ (анализировали малые лимфоциты, бласты, плазматические, ретикулы, митозы) у экспериментальных групп относительно контролей не выявлено. В течение всего наблюдаемого периода доминирующей популяцией ЛУ были малые лимфоциты; соотношение зрелых клеток и делящихся также не изменилось. Это
229