Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
др. В отношении полиоксиалканоатов, вопрос о гемовосметимости должным образом в литературе не освещен.
В работе В. И. Севастьянова с сотрудниками (Севастьянов с соавт., 2001; Sevastianov et al., 2003) выполнено исследование возможности получения образцов ПОА, пригодных для контакта с кровью, и предпринята попытка идентификации примесей, способных активировать системы гемостаза (Sevastianov et al., 2002). Результаты исследования гемосовместимых свойств полимерных пленок, полученных из ПОБ и ПОБ-со-ПОВ, включающие определение относительного количества и морфологии адгезированных на поверхности полимерных пленок тромбоцитов, активации свертывающей системы крови и системы комплемента, представлена на рис. 6.3–6.7 и таблицах 6.3–6.6.
Количество и морфология тромбоцитов, адгезированных на поверхности пленок из ПОБ и ПОБ-со-ПОВ, изучена методом сканирующей электронной микроскопии. По степени морфологических изменений адгезированные тромбоциты были разбиты на четыре класса (рис. 6.3). Основными параметрами для характеристики процесса взаимодействия тромбоцитов с поверхностью материала служили:
1)общее количество тромбоцитов, адгезированных на поверхность исследуемого материала (относительно контрольного материала);
2)количество клеток каждого из указанных выше классов (относительно контрольного материала); 3) морфология одиночных клеток. Для каждого образца суммировали количество клеток по всем полям и вычисляли относительный показатель адгезированных тромбоцитов (ОПАТ) по формуле
ОПАТ = No6p/NКОНТР,
и N КОНТР. – количество клеток на образце и контроле (полиэтилене, ПЭ), соответственно. Значения ОПАТ вычисляют и для каждого класса тромбоцитов ОПАТi (i = 1, 2, 3, 4).
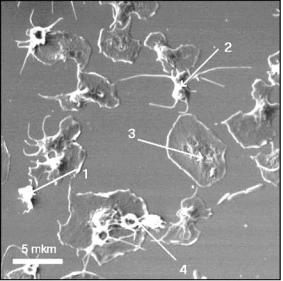
Рис. 6.3. СЕМ фотографии адгезированных клеток на пленках из полиэтилена низкого давление:
1 – неактивированные клетки (не деформированные) без признаков распластывания и псевдоподий; 2 – клетки с псевдоподиями
(активированные тромбоциты с явно выраженными псевдоподиями); 3 – полностью распластанные тромбоциты;
4 – агрегаты (Sevaianov, 2002).
215
Существенных различий в морфологии адгезированных тромбоцитов на поверхности пленок из образцов гомогенного ПОБ, а также из сополимеров оксибутирата с оксивалератом не обнаружено (рис. 6.4). Результаты количественного анализа адгезии тромбоцитов на поверхности полимерных пленок (вычисленные значения ОПАТi для каждого из полимеров) представлены на рис. 6.5.
Суммарное количество клеток, адгезированных на поверхности ПОБ, сопоставимо с контролем и несколько ниже на образцах ПОБ-со- ПОВ. В целом количество неактивированных тромбоцитов в 1.5–1.7 раза выше на пленках из ПОА обоих типов, по сравнению с контролем
– ПЕ (полиэтилен низкого давления). При этом доля распластанных клеток также существенно ниже на поверхности пленок ПОБ и ПОБ-со- ПОВ по сравнению с контрольным полиэтиленом. Количество агрегатов убывало с увеличением содержания гидроксивалерата в полимере.
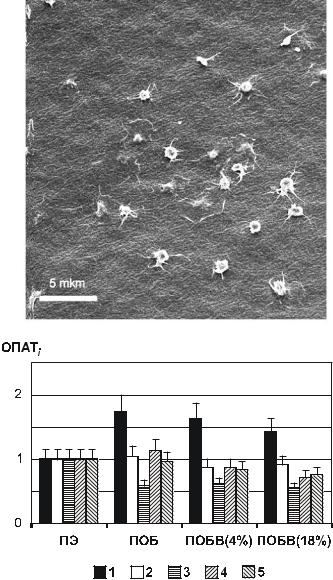
Рис. 6.4. Характерная картина тромбоцитов, адгезированных на поверхности пленок из ПОА
(Sevastianov et al., 2003).
Рис. 6.5. Значения ОПАТi для четырех классов тромбоцитов, адгезированных на поверхности полимерных пленок из ПОБ, ПОБВ и ПE (контроль):
1 – неактивированные клетки;
2 – клетки с псевдоподиями;
3 – полностью распластанные тромбоциты; 4 – агрегаты; 5 – сумма клеток
(Севастьянов с соавт., 2001).
216

Из полученных данных следует, что все исследуемые образцы ПОА обладают хорошей гемосовместимостью на стадии клеточного ответа (реакции тромбоцитов на чужеродную поверхность). По данному показателю сополимерный материал более пригоден для контакта с тромбоцитами. В целом, поверхность полимерных пленок из ПОА оказывала на тромбоциты меньшее активирующее воздействие, чем использованный в качестве контроля полиэтилен низкого давления.
Данные по активации свертывающей системы крови, индуцированной поверхностью ПОА-пленок (в значениях относительного времени рекальцификации плазмы) и системы комплемента (в значениях абсолютной (kинд)обр и относительной (Кинд) констант скоростей, суммированы в таблицах 6.3–6.4.
Для образцов из ПОБ-со-ПОВ время рекальцификации было сопоставимо с реакцией плазмы, однако для полиоксибутирата выявлено значительное превышение показателя, которое по величине сопоставимо с гепаринизированными материалами (Севастьянов с соавт., 1987). По-видимому, использованная технология очистки полимеров не исключает присутствие в образцах примеси биологически активные веществ, например липополисахаридов клеточных стенок грам-отрицательных бактерий (ЛПС), которые способны ингибировать каскадный путь активации свертывания крови.
Таблица 6.3 Абсолютные (ВРП) и относительные (ОВРП) значения времени
рекальцификации плазмы для образцов ПОА (Севастьянов с соавт., 2001)
Образец |
ВРП, с |
ОВРП |
||
|
|
|
|
|
Исходная плазма |
321 26 (n = 6) |
1.0 |
0.1 |
|
|
|
|
|
|
ПОБ |
919 100 (n = 4)* |
2.9 |
0.4 |
|
|
|
|
|
|
ПО-со-ПОВ |
296 4 (n = 4) |
0.90 |
0.07 |
|
(включение оксивалерата – 4 мол. %) |
||||
|
|
|
||
ПО-со-ПОВ |
359 29 (n = 4) |
1.1 |
0.1 |
|
(включение оксивалерата – 18 мол. %) |
||||
|
|
|
||
Таблица 6.4 Значения абсолютной (kинд)обр и относительной (Кинд) констант скоростей
активации системы комплемента, индуцированной поверхностью ПОА (Севастьянов с соавт., 2001)
Образец |
(kинд)обр см–2с–1 |
(Кинд) |
||
(n = 3) |
(n = 3) |
|||
|
||||
Купрофан (контроль 1) |
(1.7 0.1) 10–6 |
1.00 |
0.08 |
|
ПЭ (контроль 2) |
(1.3 0.1) 10–6 |
0.76 |
0.08 |
|
ПОБ |
(7.5 0.5) 10–6 |
4.4 |
0.4 |
|
ПО-со-ПОВ |
(5.3 0.4) 10–6 |
3.1 |
0.3 |
|
(включение валерата – 4 мол. %) |
|
|
|
|
ПОБ-со-ПОВ |
(4.3 0.2) 10–6 |
2.5 |
0.2 |
|
(включение валерата – 18 мол. %) |
|
|
|
|
217
Предположение о наличии в образцах ПОА биологически активных веществ за счет остаточных концентраций макромолекул бактериальных клеток подтвердилось обнаруженным комплементактивирующим действием полимеров (таблица 6.4). Все тестируемые образцы показали высокую активирующую способность относительно системы комплемента, существенно превышающую пороговое значение константы скорости активации системы комплемента (1.5). Наибольшее значение Кинд получено для ПОБ, наименьшее – для ПОБ-со-ПОВ с 18 мол. % оксивалерата.
Эти результаты свидетельствуют о негативном воздействии поверхности пленок из ПОА на ферментные системы крови. Возник вопрос, в результате какого фактора это происходит? Имеет ли место активация ферментных систем крови собственно полимерным материалом или нежелательные реакции есть следствие воздействия биологически активных веществ биомассы бактерий, присутствующих в образцах?
С целью поиска причины эффекта активации ферментных систем крови ПОА проведен детальный анализ химического состава образцов. В материале не обнаружено посторонних примесей белковой и углеводной природы, даже в следовых количествах. Учитывая это, а также принадлежность продуцента к грамотрицательным прокариотам, поиск был сосредоточен на компонентах мембран липидной природы. Известно, что образцы ПОА, синтезированные грам-отрицательными бактериями, после выделения из биомассы могут содержать в своем составе эндотоксины ЛПС, которые вызывают воспалительные, пирогенные и другие реакции (Martin and Williams, 2002). На примере двух продуцентов (природного штамма R. eutrophua и рекомбинантного штамма E. сoli) показано, что в зависимости от способа экстракции уровень эндотоксинов в полимере можно существенно снизить, до 20 U/g и менее. Это позволяет получать образцы материала, пригодные для медицинских приложений с допустимым уровнем эндотоксинов
(Lee at al., 1999).
Компонентом липидной составляющей ЛПС грам-отрицательных бактерий является липид А, в составе которого обнаружены -гидр- оксикислоты с длиной цепи от 12 до 18 атомов углерода, а также ряд насыщенных жирных кислот (ЖК) (Ritschel et al.,1988; Raitz et al.,
1991). В связи с тем, что спектр ЖК ЛПС достаточно специфичен для отдельных групп бактерий, воздействие эндотоксина на организм может быть различным. Поэтому была предпринята попытка обнаружения в исследуемых образцах полимеров эндотоксинов бактериального происхождения по составу жирных кислот.
В работе (Sevastianov et al., 2003) установлено, что жирнокислотный состав ЛПС исследуемого в данной работе продуцента ПОА
218

– бактерий R. eutropha B5786, характеризуется высоким содержани-
ем насыщенных С14:0 (более 20 мол. %), С16:0 (10 мол. %) и -гидр- оксикислот, представленных -ОН-С14:0 (> 50мол. %), -ОН-С12:0
(0.2 мол. %), -ОН-С16:0(0.2 мол. %), -ОН-С18:0 (0.5 мол. %).
Действительно, в тестируемых образцах ПОА методом хрома- то-масс-спектрометрии было выявлено присутствие длинноцепочечных ЖК. Суммарная концентрация жирных кислот в полимере составляла от десятых долей до единиц (2–3) мол. %. При
этом до 70 % этой величины приходилось на долю кислоты С16:0. Из длинноцепочечных гидроксикислот обнаружена только -ОН-С14:0,
доля которой не превышала 0.06 мол. % (рис. 6.6). Эти данные могут свидетельствовать о присутствии в образцах ПОА эндотоксинов клеточной стенки бактерий.
В этой связи используемая схема экстракции полимеров из бактериальной биомассы и очистки была модифицирована. В технологическую цепь включена дополнительная процедура перерастворения полимера в хлороформе с последующей экстракцией и дополнительной очисткой. Это позволило получить образцы полимеров, не содержащие длинноцепочечных ЖК (рис. 6.7).
Результаты последующего тестирования очищенных образцов полимеров (с 15 мол. % оксивалерата), не содержащих микропримесей насыщенных и длинноцепочечных гидроксикислот, представлены в таблицах 6.5–6.6.
Рис. 6.6. Хроматограмма образца ПОБ-со-ПОВ (соотношение мономеров С4:С5 = 79.19:18.12 мол. %) суммарное содержание примеси оксикислот С6–С18
2.67 мол. % (Sevastianov et al., 2003).
219