Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Таблица 6.2 Санитарно-химические исследования вытяжек шовных нитей из ПОА
при различных значения рН исходной воды (Севастьянов с соавт., 2001)
|
|
|
Исходное рН воды |
|
||
Показатель |
Образец |
|
|
|
|
|
4.5 |
|
7 |
|
10 |
||
|
|
|
|
|||
|
|
|
|
|
|
|
РН |
ПОБ |
+0.06/4.56 |
|
+0.10/7.10 |
|
–0.02/9.98 |
(ΔpH/pHконтр) |
ПОБ/ПОВ |
–0.01/4.49 |
|
+0.03/7.03 |
|
–0.10/9.90 |
Сдвиг оптической |
ПОБ |
0 |
|
0 |
|
+0.032 |
плотности (∆ D/Dконтр) |
ПОБ/ПОВ |
0 |
|
0 |
|
+0.28 |
Окисляемость |
ПОБ |
0 |
|
0 |
|
0 |
(мг О2/л) |
ПОБ/ПОВ |
0 |
|
0 |
|
0 |
Бромируемость |
ПОБ |
0 |
|
0 |
|
0 |
(мг Br2/л) |
ПОБ/ПОВ |
0 |
|
0 |
|
0 |
Свободные мономеры |
ПОБ |
0 |
|
0 |
|
0 |
β-оксикислот |
ПОБ/ПОВ |
0 |
|
0 |
|
0 |
В ходе культивирования фибробластов мыши линии NIH 3T3 на полимерных пленках, независимо от их состава, клетки сохраняли морфологию, характерную для нормальных клеток, выращиваемых в контроле на стекле. Оценка жизнеспособности клеток при помощи метода прижизненного окрашивания трипановым синим показала, что 99.8 ± 0.2 % клеток, культивируемых на полимерных пленках из ПОБ и ПОБ-со-ПОВ (содержание оксивалерата от 4 до 30 мол. %) не включали краситель, то есть сохраняли высокую жизнеспособность в отличие от взятого для сравнения полиэтилена. Культивирование фибробластов на полимерных пленках в течение трех суток не влияло на синтез белка в культуре. Время удвоения фибробластов, культивируемых при прямом контакте на полимерных пленках всех типов соответствовало времени генерации клеток, культивируемых в контроле на стекле, и составляло 25 ± 2 ч. (Шишацкая с соавт., 2001).
Далее под руководством доктора биологических наук Н. А. Сеткова было исследовано влияние пленочных образцов ПОА на синтез ДНК в клетках in vitro, стимулированных к пролиферации (Шишацкая с соавт., 2001) (рис. 6.1), так как такие клетки наиболее чувствительны к повреждающим воздействиям цитотоксических факторов (Епифанова с соавт, 1983). Были взяты фибробласты мыши NIH 3Т3, относящиеся к минимально трансформированным клеточным линиям, а также первичные культуры паренхимных (гепатоциты) и непаренхимных (главным образом, эндотелиальных) клеток печени мыши. Выбор культур обусловлен следующим: фибробласты непосредственно участвуют в процессах воспаления и инкапсулирования любых инородных включений, а клетки печени, помимо детоксикационной функции, обладают повышенной, по сравнению с другими клетками, чувствительностью к воздействию цитотоксических факторов.
210
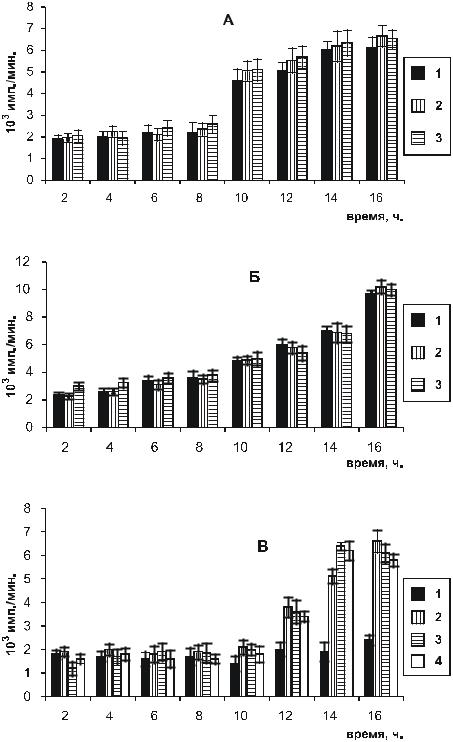
Рис. 6.1. Кинетика включения 3Н-тимидина в фибробасты мыши линии NIH 3T3 (А), клетки эндотелия (Б) и гепатоциты (В) в среде с 10 % ЭТС, культивируемых на:
1 – стекле (контроль), 2 и 3 – мембранах из ПОБ и ПОБ-со-ПОВ, 4 – на стекле, покрытом коллагеном. Метка – кумулятивная.
211
Культуру покоящихся фибробластов линии NIH 3Т3 получали по стандартной методике. Стимуляцию пролиферативной активности клеток проводили путем смены среды на свежую, содержащую 10 % эмбриональной телячьей сыворотки (ЭТС). Гепатоциты выделяли с помощью нерециркуляционной двухэтапной (неэнзиматической и энзиматической) перфузии печени наркотизированных мышей по методу Дудиной-Барковской и Миттельмана. Клетки NIH 3Т3 культивировали на среде DМЕМ с добавлением 10 % эмбриональной телячьей сыворотки (ЭТС) (НПО «Вектор», Новосибирск), 1.0 мМ L-глют- амина, 10 мМ HEPES буфера и 100 мкг/мл канамицина сульфата (BDSL, UK). Гепатоциты ресуспендировали в смеси сред
DMEM+NCTC-135 (1:1) (BDSL, UK), содержащей 5 % инактивирован-
ной при 56°C ЭТС; 0.1 % глюкозы; 0.2 % сывороточного альбумина для клеточных культур; 0,5 мкг/мл инсулина; 50 нг/мл дексаметазона; 0.2 мкг/мл глюкагона (Sigma, США); 0,02 мМ β-меркаптоэтанола; 10 мМ HEPES буфера и 100 мкг/мл канамицина сульфата. Эндотелиальные клетки ресуспендировали в среде Ham´s F12 (BDSL, UK) c добавлением 10 % ЭТС, в которой наращивали их количество, проводя 2–3 пассажа с помощью 0.2 % раствора коллагеназы, разбавленного 0,02 % раствором версена.
Клетки высевали в пенициллиновые флаконы (по 5 флаконов на каждую экспериментальную точку), содержащие пленки изПОА и в качестве контроля – стекло; объем среды составлял в 2 мл с добавлением 3Н-тимидина (37 кБк/мл; 92,5 ГБк/мМ). Исходная концентрация фибробластов и эндотелиальных клеток составляла по 30 000, гепатоцитов – 50 000 в 1 мл. Культивирование проводили в течение 16 ч. в гумидной атмосфере с 5 % CO2 с периодическим отбором клеток для исследований.
В ходе культивирования клеток в среде с 10 % эмбриональной телячьей сывороткой (ЭТС) на поверхности мембран из ПОБ и ПОБ- со-ПОВ не обнаружено снижения включения 3Н-тимидина ядрами всех типов клеток, стимулированных к пролиферации, по сравнению с контролем (стекло). Следовательно, прямой контакт клеток с поверхностью мембран из ПОА обоих типов не приводил к подавлению синтеза ДНК и не ингибировал клетки.
Культивирование фибробластов и гепатоцитов в течение трех суток при прямом контакте с поверхностью мембран из ПОБ и ПОБ-со-ПОВ не влияло на время генерации клеток и синтез белка. Эти результаты свидетельствуют о том, что очищенные образцы полиоксибутирата, а также сополимеров оксибутирата с оксивалератом, не оказывали токсического воздействия не только на морфологию и рост клеток, но и на синтез белка, а также активность матричных процессов.
212
Физико-механические свойства и степень биосовместимости изделий на их основе определяются не только структурой и базовыми физико-химическими свойствами исходного полимерного материала, но в существенной степени зависят от чистоты образцов и способа получения изделий (Williams et al., 1999). Когда в работе (Чапут с соавт., 1995; Chaput et al.,1995a, b) исследовали цитотоксичность ПОБ- со-ПОВ в культуре фибробластов, культивируемых при прямом контакте с полимером и на агаре с добавлением водных экстрактов ПОА, было установлено, что не только увеличение доли оксивалерата (от 7 до 22 мол. %) вызывает незначительный цитотоксический эффект, но также и условия получения экстрактов (температура, длительность экстракции и др.). В серии работ Cаада с соавторами показано, что пористые DegraPol® – хороший материал для роста животных клеток разных типов (Saad et al., 1996;1997a,b). Вместе с тем, при увеличении концентрации частиц материала в среде и их размеров (от 1 до 20 мкм) клетки разных типов в различной степени снижали скорость роста и продукцию метаболитов, например, коллагена, фибронектина и др. (Saad et al., 1999). Существенное влияние на адгезию и рост клеток оказывает структура поверхности полимерных изделий. В этой связи значимыми являются результаты работы (Rouxhet et al., 1998), в которой было исследовано влияние модификации поверхности полимерных пленок различными белками на адгезию и пролиферацию мононуклеарных макрофагов. Авторы установили, что модификация поверхности полимерных пленок фибронектином в отличие от альбумина или коллагена улучшает адгезию клеток оказывает. Есть сведения о том, что при обработке поверхности пленок и мембран из полиоксиалканоатов, например, лазерной резкой (Lootz et al., 2001), плазмой при низком давлении (Nitschke et al., 2002), а также ферментативно (липазами) или химическим гидролизом (NaOH (Yang et al., 2002), влияющими на пористость и гидрофильность пленок, значительно улучшаются функциональные характеристики изделий, повышается адгезия и рост клеток.
В отношении других типов ПОА пока данные весьма ограниченны. Недавно показано, что поверхность пленок из сополимера оксиоктаноата и оксигексаноата обладает хорошими адгезионными свойствами по отношению к животным клеткам (Stock et al., 1998). Хорошие адгезионные свойства пленок, изготовленных из сополимера оксибутирата и оксигексаноата (ПОБ-со-ПОГ), по отношению к фибробластам мыши показаны в работе (Yang et al., 2002). Авторы отметили, что клетки росли на таких пленках лучше, чем на полилактидных или изготовленных из полиоксибутирата.
Как было отмечено в Главе 1, все большую значимость при создании биоискусственных органов и тканей приобретают пористые пленочные и трехмерные матриксы на основе биодеградируемых
213

Рис. 6.2. Стволовые клетки костного мозга крысы линии Вистар на поверхности ПОБ-cо-ПОВ включение оксивалерата 15 мол. %). Время культивирования клеток
– 9 дней. Увеличение 200 (неопубликованные данные В. И. Севастьянова).
биополимеров. Рисунок 6.2 иллюстрирует положительный результат применения для культивирования клеток пленочного матрикса «ЭластоПОБ» (ЗАО «Биомир-сервис», Москва), изготовленного из разработанной в НИИ трансплантологии и искусственных органов композиции на основе сополимера ПОБ-со-ПОВ (Институт биофизики СО РАН), высокомолекулярного гидрофильного пластификатора и порообразователя. При культивировании стволовых клеток костного мозга крысы линии Vistar (лаборатория стволовых клеток НИИ трансплантологии и искусственных органов), оказалось, что клетки хорошо прикрепляются с последующей пролиферацией на поверхность полимерных мембран, и их рост сопоставим с контролем на полистирольных планшетах.
6.2. Гемосовместимые свойства ПОА
Одной из ключевых задач применительно к новым биоматериалам является доказательство их абсолютной безвредности для организма. Особые требования, как известно, предъявляются к биоматериалам, предназначенным для длительного контакта с кровью, так как гемосовместимость является наиболее важным аспектом биологической совместимости. Гемосовместимые материалы при контакте с кровью не должны вызывать тромбозов, тромбоэмболий, антигенного ответа, деструкции форменных элементов крови и белков плазмы (Биосовместимость, 1999). Индикатором гемосовместимости биоматериалов служит состояние системы гемостаза (Севастьянов с соавт., 1987; Zinner et al., 1998), которое можно оценить по таким показателям, как морфология адгезированных тромбоцитов (Васин с соавт., 1998), активация комплемента (Sevastianov and Tseytlina, 1984), высвобождению моноцитами цитокинина (Zinner et al., 1997) и
214