Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Деградация полимерных нитей, изготовленных из ПОА двух типов, синтезированных бактериями R. eutropha B 5786 в Институте биофизики СО РАН, исследована in vivo при непосредственном контакте имплантированных нитей с тканями животных, а также с использованием диффузионных камер (Шишацкая с соавт., 2002ж). Применение диффузионных камер при имплантации испытуемых образцов исключает непосредственный контакт имплантата с тканями и препятствует формированию грубой фиброзной капсулы. Это дает возможность исследовать биосовместимость и биостабильность материала с точки зрения истиной клеточной реакции (Розанова, 1999).
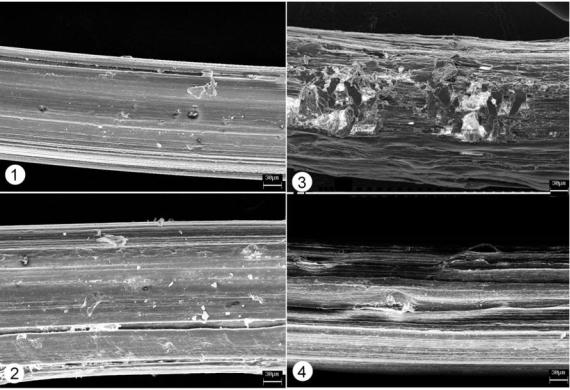
Силиконовые камеры собственной конструкции с размещенными в них образцами шовных нитей были имплантированы крысам подкожно в шейную складку (Шишацкая с соавт., 2002ж). В первый период (до 60 сут.), в отличие от условий in vitro, изменения массы были менее значительными по сравнению с последующим периодом (90–180 сут.). В течение последнего средняя скорость биодеструкции нитей из ПОБ и ПОБ-со-ПОВ-возросла, соответственно, до 0.0024 и 0.0035 мг/сут. Спустя 180 сут. остаточная масса нитей ПОБ и ПОБ- со-ПОВ составила 74 и 62 % от исходной. Таким образом, скорость биодеструкции сополимерных нитей по сравнению с ПОБ за наблюдаемый период была выше. На рис. 5.4 представлены микрофотографии нитей в ходе биодеградации in vivo.
Рис. 5.4. РЭМ снимки поверхности полимерных нитей из ПОБ-со-ПОВ в ходе деградации in vivo: 1 – исходная, 2 – 90, 3 – 120 и 4 – 180 суток.
Маркер 30 мкм (Шишацкая с соавт., 2002ж).
200
Спустя 90 сут. после имплантации существенных изменений топографии поверхности нитей не зафиксировано, несмотря на достоверное уменьшение их массы. Кроме незначительных шероховатостей (аналогично изменениям in vitro), более существенных дефектов нитей не отмечено. На более поздних сроках (120 и 180 сут.) на поверхности нитей зафиксированы адгезированные клетки. После их удаления в ряде случаев отмечены локальные дефекты на поверхности нитей – возможно, результат лизосомальной деятельности полиядерных макрофагов, доля которых в клеточном содержимом камер на этих сроках составляла 20–30 % от общего числа клеток. Показатели величины абсолютной прочности и модуля упругости нитей в целом аналогичны экспериментам in vitro: за 180 сут. экспозиции камер in vivo абсолютная прочность размещенных в них нитей ПОБ и ПОБ-со-ПОВ снизалась от 7.1 ± 0.21 и 9.40 ± 0.19 до 5.2 и 6.0 Н, то есть всего на 33–37 % от исходных значений.
Как видно на рис. 5.4, нити представляют из себя «пучок» тонких фибрилл, диаметром несколько микрон, соединенных между собой аморфным материалом. Фибриллы, в свою очередь, представляют из себя образования микрофибрилл с диаметром около 50–100 нм. Последние состоят из выпрямленных полимерных цепей, имеют степень кристалличности, близкую к 100 %, и являются основными элементами структуры, несущими механическую нагрузку при растяжении. Поскольку деградация ПОА происходит в первую очередь в аморфных областях, с течением времени происходит лишь «вымывание» аморфных межфибриллярных прослоек, а количество и структура микрофибрилл остаются неизменными. Это приводит к незначительному (по-видимому, пропорционально их объему) падению абсолютной прочности.
Анализ клеточного содержимого камер показал, что с увеличением длительности имплантирования количество клеток в них возрастало, главным образом за счет одноядерных клеток макрофагального типа. Параллельно отмечено некоторое увеличение клеток типа гигантских клеток инородных тел. У последних количество ядер на клетку колебалось в эксперименте от 1,66 ± 0,92 до 5,75 ± 1,77. Следовательно, в условиях in vivo имплантаты подвержены не только воздействию ферментов тканевой жидкости, но и клеток, которые, проникая в камеры, адгезировали на поверхности нитей.
Следующий этап был связан с изучением состояния нитей, имплантированных непосредственно в мышечную ткань животных, где они, помимо воздействия гуморальных факторов и клеток, дополнительно подвержены динамическим нагрузкам. В постоперационном периоде в результате формирования вокруг нитей фиброзной капсулы с течением времени вновь образованные ткани плотно окружали нити, «врастая» в них и образуя на границе «полимерные нити – ткани» плотный контакт. Тем не менее, в после завершения экспери-
201
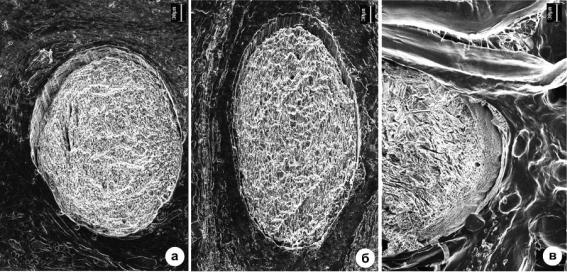
Рис. 5.5. РЭМ снимки топографии протравленной NaOH поверхности срезов на разных сроках постоперационного периода: а – 14, б – 120, в – 180 суток после имплантации.
Маркер 30 мкм. (Шишацкая с соавт., 2002ж).
мента структура нитей в целом не изменилась и грубых дефектов типа узур, раковин и трещин обнаружено не было.
Возник вопрос, имело ли место разрушение нитей в объеме? Для ответа на вопрос исследованы ультраструктура срезов фрагментов тканей с имплантатами (рис.5.5).
На срезе после 14 сут. имплантации (рис.5.5а) видны единичные микротрещины. Спустя 120 и180 сут. после имплантации состояние нитей принципиально не изменилось (рис. 5.5б, в). Отсутствие усиления дефектов структуры нити в объеме на течение 180 сут. свидетельствует в пользу предположения о том, что происхождение микротрещин и пор скорее всего связано с неравномерным травлением щелочью отдельных микрообластей нитей, возможно, межфибриллярного аморфного матрикса, так как известно, что ПОА гидролизуются в щелочной среде.
Полученные результаты изучения биодеструкции нитей из двух типов ПОА позволяют заключить, что биодеструкция полиоксиалканоатов происходит с достаточно низкими скоростями, при постепенном (послойном) выщелачивании материала с поверхности без образования грубых дефектов и резкой потери прочности шовных нитей. Показано, что деградация исследованных шовных нитей из полиоксиалканоатов в биологических средах происходит по гуморальному и клеточному пути с активным участием макрофагов и гигантских клеток инородных тел. Скорость биодеструкции сополимеров ПОБ-со-ПОВ превосходит таковую у ПОБ. В целом имеющиеся данные позволяют констатировать пригодность ПОА для изготовления биодеградируемых имплантатов длительного функционирования.
202
Глава 6. БИОСОВМЕСТИМОСТЬ ПОЛИОКСИАЛКАНОАТОВ
Одно из основных требований, предъявляемых к материалам медицинского назначения, заключается в том, что данные материалы должны быть биологически совместимы с живым организмом. Такие материалы при вживлении в организм и пребывании в нем длительное время не должны вызывать негативных реакций со стороны тканей и организма в целом.
Следует отметить, что понятие «биосовместимость» не имеет четкого толкования до настоящего времени (Севастьянов, 1999). Биосовместимыми называют материалы, способные сосуществовать совместно с живым организмом, не нанося ему вреда (Танзава, 1981). По определению Н. А. Платэ и В. А. Васильева биосовместимыми являются «Полимеры, способные к метаболизму…» (Платэ, Васильев,1986). На конференции по биосовместимости, состоявшейся в 1994 г в Великобритании, было предложено под биосовместимостью «…понимать способность материала, изделия или устройства выполнять свои функции и не вызывать отрицательных реакций в организме «хозяина» (Consensus conference…, 1994). В расширенном толковании биосовместимости следует подразумевать не только взаимное «сосуществование» двух субстанций (искусственной и естественной), но и то, что искусственный материал должен выполнять функции живой материи. При этом совершенно очевидно, что биосовместимость того или иного материала или имплантируемого элемента определяется не только его химической и надмолекулярной структурой, но и формой, топографией поверхности, спецификой взаимодействия с окружающими тканями (Полимеры медицинского назначения, 1981; Пхакадзе, 1990; Biomedical Polymers, 1994; Биосо-
вместимость, 1999; Amass et al., 1999).
Биосовместимость полиоксибутирата (3ПОБ) основывается на том, что мономер, образующий данный полимер и являющийся продуктом биодеградации ПОБ – R-β-оксимасляная кислота, является естественным продуктом обмена высших животных и человека и присутствует в крови последних. Концентрация данной оксикислоты у взрослых организмов в норме составляет 3–10 мг на 100 мл крови (Hocking and Marchessault, 1994). Данную кислоту используют в терапевтических целях для восстановления уровня белков (Pawan and Semple, 1983), вводят внутривенно пациентам в качестве источника энергии (Hiraide and Katayma, 1990), а также используют в глазной хирургии как увлажняющий раствор для поддержания тканей (Chen and Chen, 1992).
203
Установлено, что помимо мономеров β-оксимасляной кислоты, в животных тканях в составе клеточных мембран присутствуют низкомолекулярные полимеры β-оксимасляной кислоты. Так, при исследовании группы из 24 доноров установлено (Reuch et al., 1992), что общая концентрация ПОБ в плазме человека существенно варьирует, от 0.6 до 18.2 мг/л. При этом до 20–30 % об общего пула ПОБ плазмы связано с липопротеинами; в т. ч.: 6–14 % – с очень низкоплотными липопротеинами, 8–16 % с низкоплотными липопротеинами и менее 3 % – с высокоплотными липопротеинами. Основная фракция ПОБ в плазме (около 70–80 %) имеет плотность 1.22 г/мл. Определено, что альбумин является основным ПОБ-связывающим белком, а общий уровень ПОБ положительно коррелирует с уровнем низкоплотного холестерина и отрицательно- с уровнем высокоплотного холестерина. В связи с последним, содержание ПОБ в плазме и его уровень во фракциях липопротеинов имеет важное физиологическое значение. Выявлено, что ПОБ обладает незначительной оральной токсичностью; его LD50 намного выше, чем 5 г/кг веса
(Holmes, 1988).
Мономерный компонент 4-полиоксибутират, 4-оксимасляная кислота, также является естественным продуктом обмена и присутствует в тканях внутренних органов, – в мозге, почках, печени, селезенке, а также в мышцах (Nelson, 1981). Установлено, что 4-оксимасляная кислота обладает анастезирующим и седативным эффектом (Entholzner et al., 1995) и используется в связи с этим в клинической практике.
Таким образом, полиоксибутират обладает высокой бисовместимостью, однако вследствие хрупкости и невысокой механической прочности имеет существенные ограничения для применения. Сополимеры оксибутирата с оксивалератом, сополимеры оксиоктаноата и оксигексаноата обладают лучшими в сравнение с ПОБ технологическими свойствами, поэтому привлекательны для использования (Sudeush et al., 2000) Однако наличие в материале, помимо оксимасляной кислоты, других мономеров делает необходимым проверку токсикологических свойств материала в полном объеме.
Имеющиеся результаты токсикологических исследований сополимеров оксибутирата и оксивалерата, выполненные в культурах животных клеток in vitro, а также на лабораторных животных in vivо, свидетельствуют о возможном проявлении воспалительных реакций, интенсивность которых коррелирует с содержанием оксивалерата в ПОА (Gogolewski et al., 1993; Chaput et al., 1995). Нельзя, однако, не отметить, что реакция клеток и тканей на имплантант зависит не только от химического состава материала, но также и от способов переработки и формы изделий, характеристик поверхности и методов ее обработки, степени химической чистоты материала.
204