Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
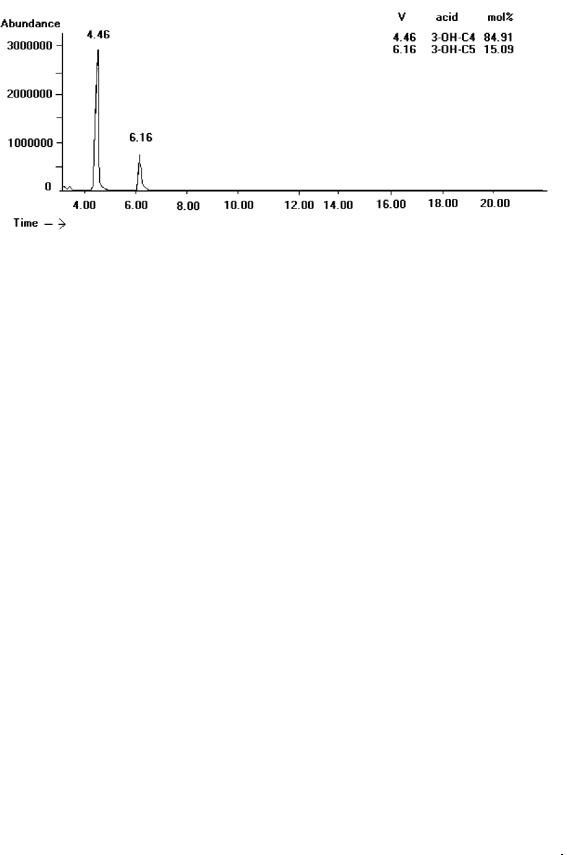
Рис. 6.7. Хроматограмма образца ПОБ/ПОВ после дополнительной очистки;
соотношение С4:С5 = 84.91:15.09 мол. % (Sevastianov et al., 2003).
Таблица 6.5 Абсолютные (ВРП) и относительные (ОВРП) значения времени
рекальцификации плазмы для дополнительно очищенных образцов ПОА (Севастьянов с соавт., 2001)
Образец |
ВРП, с |
ОВРП |
||
|
|
|
|
|
Исходная плазма |
201 7 (n = 6) |
1.0 |
0.1 |
|
|
|
|
|
|
ПОБ |
136 1 (n = 4) |
0.68 |
0.05 |
|
|
|
|
|
|
ПОБ-со-ПОВ (15 мол. %) |
153 2 (n = 4) |
0.80 |
0.06 |
|
(однократная очистка) |
||||
|
|
|
||
|
|
|
|
|
ПОБ-со-ПОВ (15 мол. %) |
160 3 (n = 4) |
0.76 |
0.06 |
|
(двукратная очистка) |
||||
|
|
|
||
|
|
|
|
|
Таблица 6.6 Значения абсолютной (kинд)обр и относительной (Кинд) констант скоростей
активации системы комплемента, индуцированной поверхностью очищенных образцов ПОА (Севастьянов с соавт., 2001)
Образец |
(kинд)обр см–2с–1 |
(Кинд) |
|
|
(n = 3) |
(n = 3) |
|
|
|
|
|
Купрофан (контроль 1) |
(2.5 0.2) 10–6 |
1.00 0.08 |
|
|
|
|
|
ПЭ (контроль 2) |
(2.1 |
0.1) 10–6 |
0.84 0.09 |
|
|
|
|
ПОБ |
(2.3 |
0.2) 10–6 |
0.92 0.10 |
|
|
|
|
ПО-со-ПОВ (15 мол. %) |
(2.0 |
0.1) 10–6 |
0.80 0.07 |
(однократная очистка) |
|
|
|
ПОБ-со-ПОВ (15 мол. %) |
(1.10 |
0.08) 10–6 |
0.44 0.05 |
(двукратная очистка) |
|
|
|
220
Из сравнения данных таблиц 6.3–6.4 и с аналогичными данными таблиц 6.5–6.6 видно, что дополнительной очисткой удалось полностью устранить выявленный отрицательный, с точки зрения гемосовместимости, эффект активации ферментных систем крови для очищенных по ранее принятой схеме образцов как ПОБ, так и ПОБ- со-ПОВ. Следует отметить, что дополнительная двукратная процедура перерастворения и очистки ПОБ-со-ПОВ не изменила значение ОВРП образцов (таблица 6.5), но существенно снизила индуцированную поверхностью сополимера активацию системы комплемента (таблица 6.6).
Эти результаты показали, что фактoром, активирующим ферментные системы крови являются микропримеси длинноцепочечных жирных кислот – компонентов ЛПС клеточных стенок бактерий R.eutropha – продуцента исследуемых ПОА. Дополнительно очищенные образцы ПОБ и ПОБ-со-ПОВ, не содержащие данных примесей, в реакции активации системы комплемента показали себя лучше с точки зрения гемосовместимости по сравнению с взятыми в качестве контроля купрофаном и полиэтиленом.
Таким образом, специальные технология очистки позволяет получать образцы ПОА, свободные от длинноцепочечных гидроксикислот – компонентов клеточной стенки, 99.9 % чистоты, пригодные для контакта с кровью.
6.3. Результаты исследования биосовместимости ПОА in vivo
Результаты исследований медико-биологических свойств полиоксиалканоатов на экспериментальных животных, представленные в литературе, немногочисленны и посвящены главным образом выявлению токсичности материала. Развитие тканевой инженерии – нового направления трансплантологии и биоматериаловедения явилось сильным стимулом для медико-биологических исследований ПОА.
Полиоксибутират и его смеси с полиэтиленом изучены в качестве заменителя кожи в сравнении с полилактидами при имплантации лабораторным крысам на длительное время (Beumer et al., 1978). Отмечено наличие воспалительных реакций тканей в первый период, однако далее, на фоне формирующегося фиброза происходила деградация полимеров, и воспалительные реакции прекращались. Примерно через две недели после имплантации во всех исследованных полимерных матриксах наблюдали формирование пор и прорастание их новыми клетками. Отрицательного влияния ПОБ на структуру и морфологию тканей внутренних органов экспериментальных животных не обнаружено.
221
В работе (Harrison et al., 1994) изучены свойства и кинетика деградации ПОБ и его смесей с полиэтиленом при имплантации крысам на срок до 52 недель. Макро- и микроскопия тканей показала наличие неспецифического воспаления тканей в раннем периоде (первые две недели), при этом отмечено, что имплантанты были достаточно прочными и не влияли на пролиферативную активность клеток в окружающих тканях. При имплантации пленочных образцов композита «полиоксибу- тират-полиуретаны» под кожу лабораторным животным в области брюшины не обнаружено признаков перерождения тканей и образования опухолей. Через год толщина капсулы вокруг имплантатов составляла у разных животных от 60 до 250 мкм (Saad et al., 1997b).
Однако в одной из последних работ в ходе исследования ПОБ применительно к сердечно-сосудистой хирургии получены отрицательные результаты (Unverdorben et al., 2002). Стенты, изготовленные из ПОБ и имплантированные в подвздошную артерию кроликам, вызывали выраженную воспалительную реакцию, повышенную продукцию коллагена, а также сужение и повреждение стенок сосудов.
Профессором Гоголевски с сотрудниками (Gogolewski et al., 1993a, b) изучена реакция тканей на ПОБ и ПОБ-со-ПОВ in vivo в сравнении с полилактидами при имплантации внутрибрюшинно мышам. Вокруг полимерных имплантатов отмечена типичная реакция тканей с участием мононуклеарных макрофагов, фагоцитирующих ПОА, и формирование фиброзной капсулы. Однако воспалительная реакция тканей проявлялась в разной степени в зависимости от типа материала. При использовании полилактидов она исчезала к исходу первого месяца после операции, а у животных, которым были имплантированы ПОБ и ПОБ-со-ПОВ, воспалительные реакции сохранялись в течение трех месяцев. При этом наличие оксивалерата усиливало воспаление. На более поздних сроках (от 3 до 6 месяцев после имплантации) негативные проявления воздействия оксивалерата исчезали, и состояние тканей было одинаковым во всех группах животных. Негативных реакций вокруг полимерных имплантатов из ПОА в виде абсцессов и некрозов тканей не отмечено. Близкие результаты получены при имплантации сополимеров ПО-со-ПОВ с различным включением оксивалерата (7, 14 и 22 мол. %) внутримышечно овцам на срок до 90 недель (Сhaput et al., 1995 a,b). Неблагоприятных реакций в виде некрозов или абсцессов в месте имплантатов не обнаружено. В течение первой послеопрерационной недели зарегистрировано небольшое воспаление тканей вокруг имплантатов с участием нейтрофиллов, лейкоцитов, макрофагов и фибробластов и начало формирования фиброзной капсулы. Воспалительная реакция была более значительной на имплантаты, содержащие 14 и 22 мол. % оксивалерата. К трем месяцам после имплантации воспаление тканей значительно уменьшилось, сформированная плотная капсула была
222
представлена высоко организованными мышечными волокнами и хорошо васкулиризированной. На более поздних сроках, спустя полгода и далее после имплантации, в капсуле и близлежащих тканях отмечено много жировых клеток. На всех сроках исследования в зависимости от доли включения оксивалерата в ответе тканей, характере и длительности тех или иных реакций отмечены некоторые различия, усиливающиеся с ростом включения оксивалерата.
Однако в работах других авторов (Borkenhagen et al., 1998) негативного влияния оксивалерата in vivo не обнаружено. Были исследованы сополимеры ПОБ-cо-ПОВ с различными включениями оксивалерата в качестве нервопроводящих каналов на лабораторных животных в ходе четырехмесячного эксперимента. Зависимости процесса регенерации аксона от химического состава имплантата не выявлено. Отмеченные незначительные воспалительные реакции не влияли на регенерацию тканей, а наличие оксивалерата не усиливало постоперационного воспаления. В целом, результаты по регенерации нервопроводящих каналов, полученные при использовании сополимера ПОБ-со-ПОВ, не отличались от таковых при исследова-
нии ПОБ-имплантатов (Hazari et al.,1999).
Таким образом, однозначного ответа на вопрос о биологической инертности сополимерного материала по сравнению с полиоксибутиратом на сегодня нет. Нельзя не отметить, однако, что воспалительные и другие нежелательные реакции при испытаниях новых биоматериалов и конструкций могут быть обусловлены не только составом, формой изделия и местом имплантации, но в значительной мере химической чистотой материала. Например, в работе (Tang et al., 1999) в ходе исследования тканевой реакции крыс, которым был имплантирован полиоксибутират, было установлено, что выщелачиваемые в ходе деструкции полимера примеси, в том числе низкомолекулярные фракции полиоксибутирата, могут быть в значительной мере ответственными за развитие воспаление и, в частности, повышенное отложение коллагена.
6.3.1. Биологическое воздействие ПОА in vivo
Сравнительное исследование биологической совместимости полиоксиалканоатов двух типов, гомогенного ПОБ и сополимеров ПОБ- со-ПОВ, выполнено в серии острых и хроническом экспериментах на лабораторных животных с использованием образцов ПОА, синтезированных Ralstonia eutropha B 5786 (Севастьянов с соавт., 2001; Шишацкая с соавт., 2002а–г; к; Шишацкая, 2003; Volova et al., 2003).
Определение раздражающего действия водных вытяжек ПОБ и ПОБ-со-ПОВ с различным включением оксивалерата (4 и 18 мол. %), выполненное на белых мышах линии Balb/c в виде накожных аппликаций и при введение проб в коньюктивальную полость глаза кроликам, показало отсутствие раздражающего эффекта в обоих вариан-
223
тах. На месте кожных аппликаций у опытных животных не отмечено явлений гиперемии, отека, сухости, шелушения и других реакций по сравнению с контролем. При введении вытяжек ПОА в коньюктивальную полость животным раздражающее действие на слизистые отсутствовало. Аллергической реакции немедленного типа у животных при этом также не наблюдали (Севастьянов с соавт., 2001).
Сенсибилизирующее действие ПОА определяли по реакции дегрануляции тучных клеток лабораторных крыс (по 5 животных в каждой группе), вводя в наружную поверхность уха 0.02 мл исследуемых вытяжек. На третий день животным проводили 7 накожных аппликаций по 0.5 мл вытяжки на выстриженные участки кожи бока размером 1 1 см. Контрольным животным проводили аппликации модельной среды в том же режиме. Через сутки после последней аппликации проводили провокационную внутрикожную пробу 0,02 мл свежеприготовленной вытяжки в противоположный аппликациям бок каждого животного. Ответную реакцию наблюдали через 15 мин., 24 и 48 ч. По стандартной методике определяли образование комплекса антиген-антитело. Препараты микроскопировали под большим увеличением, считая тучные клетки (клетки-мишени), подвергшиеся дегрануляции, и нормальные.
Во всех экспериментальных группах животных, сенсибилизированных по вышеописанной методике, дегрануляция тучных клеток составила менее 10 % относительно контроля. Это позволяет сделать вывод об отсутствии сенсибилизирующего эффекта испытуемых образцов.
Далее авторами было исследовано общетоксическое действие ПОБ и ПОБ-со-ПОВ в виде вытяжек в остром опыте (7 суток) на белых мышах линии Balb/c (общее число животных 28). Животным однократно внутрибрюшинно вводили вытяжки ПОБ и ПОБ-со-ПОВ (включение оксивалерата 15 мол. %) и наблюдали в течение 7 суток. Положительному контролю вводили физиологический раствор, отрицательным контролем служили интактные животные. Оценивали общее состояние и поведение животных, массу тела и внутренних органов и макроскопию внутренних органов (см. таблицы 6.7–6.9).
Внешних проявлений интоксикации у животных после введения вытяжек в течение наблюдаемого периода не выявлено. Поведение мышей в опыте не отличалось от контрольных групп. Отклонений в массе тела, а также массе внутренних органов у экспериментальных животных относительно контроля не зафиксировано (таблица 6.7). Макроскопические исследования внутренних органов животных через 7 дней от начала эксперимента патологических изменений не выявили.
Анализ морфологического состава периферической крови мышей в контрольных и опытных группах показал, что колебания концентрации эритроцитов и лейкоцитов были в пределах физиологических величин (таблица 6.8). Достоверных сдвигов в лейкоцитарной формуле крови животных, получивших вытяжки полимеров, также не выявлено.
224