Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny

Рис. 7.8. Пористый протез сосудистого клапана, изготовленного с использованием отливки из алюминия
(Sodian et al., 2000а).
снизилась за 24 недели примерно на 26 %. У контрольных животных через 4 недели сформировались тромбы на всех створках клапана.
Элaстичный, резиноодобный полиоксиоктаноат (PОO) исследован в качестве матриц сердечных клапанов (Sodian et al.,1999; 2000а). Для изготовления пористой конструкции матрицы частицы хлорида натрия размером от 180 до 240 мкм смешивали с раствором полимера. После высушивания полученные матрицы промывали водой; образованные пористые конструкции использовали для конструирования протеза сердечного клапана (рис. 7.8).
В течение 8 суток клетки не только хорошо пролиферировали, заполняя поры материала, но также синтезировали коллаген и формировали соединительную ткань между наружной и внутренней поверхностями матрицы. Конструкции, изготовленные из пористого сополимера ПОО-со-ПОГ, предварительно засеянные клетками сосудистой ткани, испытаны в биореакторе с пульсирующим током среды (Sodian et al., 1999). Далее была показана пригодность высокоэластичного с низкой температурой плавления полиоксиоктаноата (ПОО) для культивирования клеток эндотелия (Sodian et al., 2000b–d).
Недавно в работе (Hoerstrup et al., 2000) проведена успешная пересадка протезов трехстворчатых сердечных клапанов ягнятам. В качестве матрицы был использован сетчатый полигликолид, покрытый слоем 4-ПОБ. Через 20 недель функциональные характеристики имплантированных клапанов были сходны с нативными. Гистологический анализ подтвердил формирование нормально организованной слоистой ткани с эндотелием. Эхокардиографией продемонстрировано, что створки клапана функционировали в нормальном режиме. Образования стенозов, тромбозов или аневризм не обнаружено. Важно отметить, что с течением времени внутренний диаметр конструкции клапана увеличился с 19 мм в начале эксперимента до 23 мм спустя 20 недель. Отмеченная особенность функционирования ткане-инженерного клапана очень важна, так как может быть использована при операциях у детей.
7.1.2. ПОА в челюстно-лицевой хирургии
Полимерные мембраны перспективны для регенерации костных тканей, например, при исправлении дефектов челюсти. Полимерные барьерные мембраны применяют при направленной регенерации ко-
255
стных тканей для предотвращения заполнения костных дефектов мягкими тканями.
Вработе (Galgut et al., 1991) исследован гистологический ответ челюстных тканей крыс на имплантацию сополимерных мембран (3- ПОБ-со-3-ПОВ), которые использовали в качестве барьера. Показана хорошая переносимость данных мембран животными. По сравнению с мембранами из политетрафлюороэтилена (PTFE) в случае применения полиоксиалканоата зафиксировано незначительное врастание эпителиальной ткани в область дефекта.
Известно, что при закрытии дефектов неба микроэпителиальные лоскуты в ходе операций могут сдвигаться к средней линии неба, оставляя оголенными области кости, прилегающие к зубному ряду. В заживлении таких ран принимают участие фибробласты и керотиноциты. Успех заживления определяется степенью контракции раны. В работе (Leenstra et al., 1995) на собаках в опыте длительностью 24 недели оценен эффект применения непористых пленок из 3- ПОБ-со-3-ПОВ для сохранения микропериоста и отделения костных тканей. Через 8 и 12 недель пленки оставались без изменения и были окружены сформированными фиброзными капсулами. Это способствовало нормальному процессу восстановления костных тканей. Результат применения данного сополимера превосходил эффект применения полилактида.
Помимо использования полимерных барьерных мембран для формирования периодентальных связок, мембраны из ПОА также могут быть применены в качестве матриц для регенерации костных дефектов челюсти. В работе (Kostopoulos and Karring, 1994a) использовали мембраны из сополимера 3-ПОБ-со-3-ПОВ для направленной регенерации костной ткани в месте дефекта нижней челюсти крыс. Наблюдение в течение 180 суток показало, что в месте имплантации полимерной мембраны происходил рост нормальной костной ткани, в то время как у контрольных животных (дефект челюсти оставался открытым) дефект заполнялся костной тканью только на 35–40 %, остальной объем заполнялся другими тканями. Далее авторы, используя полимерные мембраны, показали, что на их основе за 6 мес. дефект полностью заполнился костной тканью у 2/3 крыс. В нескольких случаях, однако, мягкие ткани мигрировали в область имплантата. В результате, рост костной ткани ингибировался (Kostopoulos and Karring, 1994b). Таким образом, в принципе возможно использование ПОА в челюстной восстановительной хирургии, однако для применения их в качестве барьера для мягких тканей необходима модификация мембран.
Вработе (Kramp et al., 2001) для закрытия дефекта незаращенного неба были использованы пленки и пластины из полиоксибутирата, которые с помощью болтов, также изготовленных из ПОБ, прикручивали в месте дефекта (рис. 7.9).
256
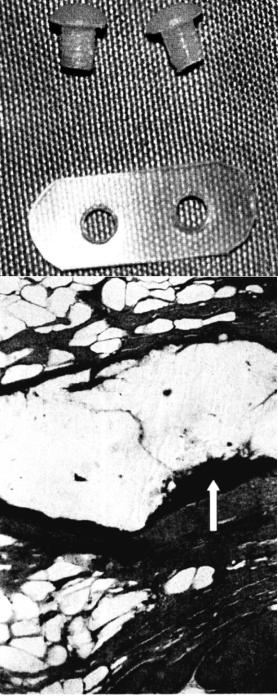
Рис. 7.9. Конструкции из ПОБ для закрытия дефекта неба (Kramp et al., 2001).
Рис. 7.10. 20 месяцев после имплантации пластины из ПОБ (Kramp et al., 2001).
Приживление всех имплантатов прошло хорошо. Макро- и микроскопически проявления воспаления в месте имплантатов зафиксировано не было. Через 6 месяцев дефекты полностью закрылись регенерированными тканями. При этом следует отметить весьма медленную деструкцию материала пластин. Только спустя 20 и 25 месяцев наблюдали частичную абсорбцию ПОБ (рис. 7.10).
Барьерные мембраны из 3-ПОБ-со-3-ПОВ, усиленные полигликолидными волокнами, были использованы для покрытия зубных имплантатов в опыте на собаках. Для этого мембраны помещали в
257
зубные лунки сразу после экстракции зубов у животных. Дополнительно в мембрану были введены лекарственные препараты. Незначительная инфильтрация не препятствовала костной регенерации. Спустя 12 недель наблюдали нормальную регенерацию костной ткани. В контроле (полимерная мембрана отсутствовала в лунке) наблюдали недостаточное костное заполнение (Gotfredsen et al., 1994). Cопоставление этих результатов с результатами использования в аналогичных целях мембран из синтетических полигликолидов позволяет надеяться, что мембраны из ПОА в будущем смогут выполнять функцию применяемых в настоящее время зубных мембран из полиглактинового компонента.
7.1.3. Ортопедия
ПОА представляют интерес также для восстановительной хирургии костных тканей. Установлена возможность получения механически прочных композитов ПОА с гидроксиапатитом. При этом выявлено, что добавление гидроксиапатита к ПОБ повышает прочностные характеристики полимера (Doyle et al., 1990). Наблюдение в течение 12 месяцев после имплантации такого композита в поврежденные костные ткани показало отсутствие воспалительных реакций и хорошую регенерацию ткани без каких-либо структурных нарушений. Авторы другой работы (Holland et al., 1990a) также показали, что добавление гидроксиапатита улучшает свойства ПОБ, увеличивая пористость матрикса. Остеобласты при контакте с таким материалом, проникая в пористую структуру композита, закрепляются в ней и нормально пролиферируют. Хорошие результаты получены также при смешивании гидроксиапатита с сополимером ПОБ-со-ПОВ. В течение нескольких месяцев после имплантации данного композита лабораторным животным зарегистрировано постепенное снижение молекулярного веса материала (Holland et al., 1990b). По мере формирования пор в матриксе композита скорость биодеградации последнего возрастала; костная ткань при этом нормально развивалась.
ПОБ и сополимеры ПОБ-со-ПОВ, усиленные гидроксиапатитом, исследованы для восстановления костных дефектов конечностей. Показано, что физико-механические характеристики данных композитов близки по прочности костям конечностей и могут быть использованы для изготовления сложных костных протезов, включая моделирование губчато-кортикальных конструкций (Boeree et al.,1993).
Поскольку для ПОА подтвержден пьезоэлектрический эффект, данный материал перспективен для костной регенерации. В этой связи изучены пьезоэлектрические свойства композитов 3-ПОБ-со-3- ПОВ с гидроксиапатитом и 3-ПОБ-со-3-ПОВ со стекловолокном с различным соотношением фракций (Knowles et al., 1991). Обнаружено генерирование пьзоэлектрического потенциала у данных компо-
258
зитов, по силе, близкому к таковому у кости. Далее эти композиты исследованы в опытах in vitro и in vivo (Knowles and Hastings, 1993a, b). В системах in vitro показано снижение массы композита в результате вымывания стекловолокна.
Аналогичная картина также зафиксирована in vivo. Данные композиты были имплантированы крысам подкожно, а также в качестве имплантатов бедра, не несущих нагрузки. В начале была отмечена достаточно интенсивная клеточная активность окружающих тканей, что было обусловлено высвобождением ионов из керамики. Однако в целом ответ тканей был мягким. Со временем клеточная активность снижалась. Через четыре недели пролиферирующие клетки внедрялись в пористую поверхность композита, в котором поры формировались в результате растворения керамики. Далее было отмечено формирование костной ткани на поверхности имплантата. Авторы изучали характеристики сополимеров 3-ПОБ-со- 3-ПОВ в композиции со стекловолокном и в сравнении с композитами данного сополимера, усиленного гидроксиапатитом (Knowles et al., 1992). Конструкции, изготовленные из данных композитов, были имплантированы кроликам в бедренные кости и оценены в динамике, включая тесты с использованием механических нагрузок на имплантат. В течение восьми недель наблюдения показано, что приживление композитного имплантата с гидроксиапатитом проходило лучше по сравнению с композитом 3-ПОБ-со-3-ПОВ со стекловолокном. Торможение приживления имплантата и формирования костной ткани авторы обусловили ионами, высвобождаемыми из стеклокомпонента конструкции.
В работе (Jones et al., 2000) cравнивали имплантаты, изготовленные из 3-ПОБ-со-3-ПОВ в композиции с фосфатом кальция с имплантатами из композита фосфата кальция с полилактидом, которые имплантировали подкожно и в бедренные кости животным. В ходе эксперимента установлено, что биодеградация композита с 3-ПОБ-со- 3-ПОВ происходила в четыре раза медленнее, чем из полилактида.
Полиоксибутират (ПОБ), усиленный частицами синтетического гидроксиапатита, исследован in vivo в качестве заменителя костной ткани в сравнение с нативным ПОБ (Lukinska et al., 1997). Имплантированные в бедренную кость кроликов полимерные конструкции из ПОБ и композита «ПОБ-гидроксиапатит» наблюдали в течение 6 мес. В этой работе также подтверждены преимущества композитного материала для восстановительной костной хирургии, так как при его использовании отмечено эффективное взаимодействие в системе «имплантат – кость». В результате этого по мере деградации ПОБ происходит взаимопроникновение частиц имплантата в костную ткань, а клеток костной ткани – в матрикс полимерного имплантата.
259