Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
длиной углеродной цепи, от С2 до С22. Выход полимера составляет до 50 % от АСБ, при этом его молекулярный вес зависит от длины углеродной цепи исходной кислоты. Максимальные значения (до 1 000 000 Da) соответствуют росту на С7–9 и С13–16 жирных кислотах (Akiyama et al., 1992). Оптимизация процесса с использованием в качестве субстрата пальмового масла повысила выход полимера до 60%. Проблема достижения высокого общего выхода полимера со значительными включениями валерата связана с тем, что индукторы синтеза оксибутирата короткоцепочечные жирные кислоты (пропионат и валериат), токсичны для продуцента. Поэтому выходом из этой ситуации может стать как оптимизация самого процесса ферментации за счет изменения режима дозирования индуктора (жирных кислот), а также поиск и использование новых микроорганизмов.
С целью нахождения условий для синтеза сополимеров оксибутирата с оксивалератом и определения влияния режима углеродного питания бактерий на состав образуемых полимеров на примере несколько штаммов проведено сравнительное исследование органических углеродных субстратов (ацетата, фруктозы и др.) и косубстратов (жирных кислот – масляной, пропионовой, пентановой) (Волова с соавт., 1992). Были взяты водородные бактерии Alcaligenes eutrophys Z1 и B 5786, а также быстрорастущая карбок-
сидобактерия Seliberia carboxydohydrogena Z 1062, для которой была выявлена способность к синтезу полиоксибутирата (Волова с соавт., 1994б). Органотрофное культивирование бактерий сопровождалось по сравнению с автотрофными условиями биосинтеза более высокими урожаями клеток (на 20–25 %) и вследствие более быстрого роста более ранним (на 6–10 ч) наступлением стационарной фазы (фазы максимального содержания полимера в биомассе). Все штаммы показали способность утилизировать масляную, пропионовую и пентановую кислоты. Две последние, как известно, являются индуктором для синтеза мономеров оксивалерата (Steinbüchel and Schübert, 1989). При внесении небольших добавок (1-2 г/л) данных кислот в культуру бактерий, находящуюся в условиях накопления полимера, зарегистрирована способность всех штаммов включать мономеры оксивалерата в полимерную цепь оксибутирата (таблица 2.4). Однако выходы полимера и соотношение мономеров в нем было различным. Общий выход полимеров по величине был сопоставим у двух штаммов R. eutropha и существенно ниже у карбоксидобактерии. Последняя, однако, показала наибольшую способность включать в сополимер оксивалерат. При равных условиях культивирования содержание оксивалерата в полимере, синтезированном штаммом Z1062, было самым высоким.
75

Таблица 2.4 Состав ПОА, синтезируемых водородокисляющими бактериями
на смешанном углеродном субстрате (Волова с соавт., 1992)
|
|
Содержание |
Состав ПОА (мол. %) |
||
Штамм |
Источник углерода |
ПОА в клетках |
|||
|
|
||||
|
|
(%) |
3-ОБ |
3-ОВ |
|
|
|
|
|||
|
|
|
|
|
|
Z1 |
CО2 |
69 |
100 |
– |
|
|
ацетат |
68 |
100 |
– |
|
|
фруктоза |
72 |
100 |
– |
|
|
CО2+пропионат |
78 |
95 |
5 |
|
|
CО2+валерат |
67 |
97 |
3 |
|
|
фруктоза+пропионат |
74 |
83 |
21 |
|
|
ацетат+пропионат |
69 |
80 |
20 |
|
|
ацетат+валерат |
69 |
92 |
8 |
|
|
|
|
|
|
|
B5786 |
CО2 |
78 |
100 |
– |
|
|
ацетат |
68 |
100 |
– |
|
|
фруктоза |
82 |
100 |
– |
|
|
глицерин |
75 |
100 |
– |
|
|
CО2+пропионат |
78 |
85 |
15 |
|
|
CО2+валерат |
67 |
92 |
18 |
|
|
фруктоза+пропионат |
72 |
79 |
21 |
|
|
ацетат+пропионат |
79 |
80 |
20 |
|
|
ацетат+валерат |
70 |
88 |
12 |
|
Z1062 |
CО2 |
24 |
100 |
– |
|
|
ацетат |
27 |
100 |
– |
|
|
CО2+валерат |
32 |
76 |
24 |
|
|
ацетат+валерат |
29 |
68 |
32 |
|
В процессе исследования биосинтеза сополимерных ПОА было обнаружено, что скорости синтеза оксибутирата и оксивалерата различны, и динамика накопления полимера в клетках не совпадает со скоростью включения в него оксивалерата. Оказалось, что максимальное содержание оксивалерата в полимере фиксируется спустя 8- 10 ч после добавки пропионата или валерата в культуру. Далее доля данной фракции в сополимере падает на фоне повышения общего пула полимера и содержания в нем оксибутирата (рис. 2.8).
Рис. 2.8. Динамика накопления полимера (1) в R. eutropha B 5786 и соотношения фракций оксибутирата (2) и оксивалерата (3) в нем после подачи пентановой кислоты в культуру на 10 ч
(Volova et al., 2002).
76
Установление данного факта нестабильности фракционного состава сополимеров оксибутирата побудило детально исследовать процесс с целью нахождения условий для регулируемого включения оксивалерата в полимер. С учетом токсичности более высоких концентраций (свыше 2–3 г/л) оксивалерата для культуры был принят иной режим культивирования, в ходе которого сочетанием количества добавок валерата в культуру (1, 2, 3 и более) и последующего времени культивирования удалось разработать режимы биосинтеза, при которых обеспечивается синтез сополимера с варьированием соотношения мономеров оксибутират/оксивалерат в широких пределах, от 9:1 до 1:9 (мол. %) (Волова с соавт., 1996е). Однако для получения сополимера с более высоким содержанием оксивалерата, как правило, приходится жертвовать общим выходом биомассы.
Следующим был вопрос о возможности синтеза водородокисляющими бактериями трехкомпонентных полиоксиалканоатов, содержащих в своем составe, помимо оксибутирата и оксивалерата, мономеры с более длинной углеродной цепью.
Для выявления способности бактерий R. eutropha В5786 и S. carboxydohydrogena Z1062 синтезировать одновременно коротко- и среднецепочечные ПОА бактерии культивировали на смешанном углеродном субстрате, содержащем углекислоту (или фруктозу) и добавки углеводородных кислот. В качестве индуктора синтеза гетерополимерных ПОА исследованы гексановая, гептановая, октановая, нонановая кислоты и их соли. Установлено, что оба штамма утилизируют данные соединения в качестве источника углеродного питания. Практически сразу после внесения в культуру кислот бактерии начинали их утилизацию. Спустя 1.5–2.0 часа остаточная концентрация кислот в культуральной среде падала в 2–3 раза от исходной, а спустя 4–5 часов – до следовых концентраций. Определены предельно допустимые для роста бактерий концентрации данных кислот в среде вследствие их токсичности. Доза одноразовых добавок углеводородных кислот в культуру не должна превышать 0.5–0.7 г/л.
Далее проведена серия экспериментов в режиме периодической ферментации, в ходе которой в растущую при дефиците азота автотрофную культуру (обычно через 10–15 час. от начала ферментации), аккумулирующую полимер, вносили добавку одной их углеводородных кислот или ее соль; ферментацию продолжали в течение 15–25 час. В ходе экспериментов перед добавкой кислоты, спустя 30 мин. и далее через 1–2 часа производили отбор проб для определения концентрации биомассы в культуре, общего содержания полимера в клетках и его состава, а также остаточной концентрации углеводородной кислоты.
Ферментация бактерий на смешанном углеродном субстрате сопровождалась накоплением в клетках полиоксиалканоатов, кон-
77
центрация и состав которых имели различные значения в зависимости от условий эксперимента. Оба штамма показали способность к синтезу трехкомпонентных полимеров (рис.2.9–2.10) (Волова с со-
авт., 1996 в; 1998).
Обе культуры, независимо от типа используемой углеводородной кислоты, как с четным, так и нечетным числом атомов углерода в цепи, синтезировали в качестве доминирующего компонента ПОА оксимасляную кислоту, и включали в качестве сополимеров только оксивалерат и оксигексаноат. Однако соотношение сополимеров в ПОА и их концентрация в клетках у двух культур в аналогичных условиях роста и углеродного питания были различными.
У водородных бактерий при использовании ими в качестве дополнительного углеродного питания кислот с нечетным числом атомов углерода (С7 и С9) в составе ПОА практически всегда обнаруживали включения оксивалерата, однако его доля в гетерополимере с увеличением длины углеродной цепи у добавок падала. Так, при внесении в культуру в качестве добавки гептановой кислоты доля оксивалерата достигала 10–15 мол. % и выше, а при использовании нонановой кислоты – ниже на порядок. Помимо оксибутирата и оксивалерата в составе гетерополимеров, синтезируемых данным штаммом при росте на гептановой или нонановой кислотах, обнаруживали также в небольших концентрациях включения оксигексаноата, однако эти включения не носили регулярного характера. При использование водородными бактериями в качестве добавок кислот с четным числом атомов углерода (С6, С8 и С10) в составе ПОА с большей регулярностью обнаруживали включения оксигексаноата и нерегулярные включения оксивалерата. Доля данных включений, однако, не превышала 1–2 мол. %, следовательно, их можно классифицировать в качестве минорных. Спорадически в отдельных экспериментах у водородных бактерий при наличии в среде октановой кислоты наблюдали включение в качестве сополимера оксиоктаноата, при этом его доля в ПОА составляла, как правило, менее 1 мол. %.
Карбоксидобактерии, в отличие от водородных бактерий (рис. 2.10), при росте с аналогичными добавками углеводородных кислот оксивалерат в ПОА в заметных количествах включали не всегда, а, как правило, только при росте на углеводородных кислотах с нечетным числом атомов углерода в углеродной цепи и его доля была невысокой, единицы и десятые доли мол %. Включение оксигексаноата, однако, в этом случае было более выраженным, его доля в ПОА достигала в отдельных экспериментах 20 мол. % и более, однако включения оксиоктаноата в состав ПОА у карбоксидобактерий в описываемых экспериментах не отмечено. Все это позволяет говорить о специфичности микробного метаболизма углеводородных субстратов и метаболизма ПОА.
78
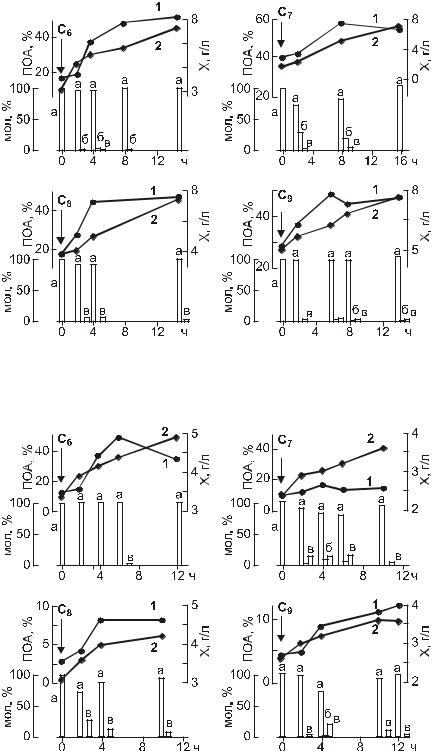
Рис. 2.9. Динамика образования трехкомпонентных ПОА бактериями R. eutropha B 5786: концентрация в культуре полимера в % (1), биомассы в г/л (2); а, б, в – сополимеры, соответственно, 3-оксибутират, 3-оксивалерат и 3-оксигексаноат (Волова с соавт., 1998).
Рис. 2.10. Динамика образования трехкомпонентных ПОА бактериями
S. carboxydohydrogena Z1062:
концентрация в культуре полимера в % (1), биомассы в г/л (2); а, б, в – сополимеры, соответственно, 3-оксибутират, 3-оксивалерат и оксигексаноат (Волова с соавт., 1998).
79