Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
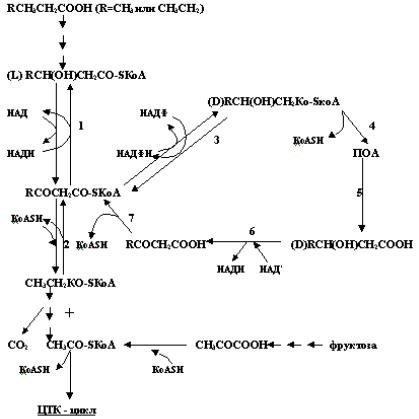
Рис. 2.5. Цикл полиоксиалканоатов у A. eutrophus:
1 -НАДН-зависимая ацетацетил-КоА редуктаза, 2 – 3-кетотиолаза, 3 – НАДФН-зависимая ацеацетил-КоА редуктаза, 4 – ПОБ-синтаза (полимераза), 5 – ПОБ -деполимераза,
6 – D(-)-3-оксибутират дегидрогеназа, 7 – ацетацетил-КоА синтаза (тиофораза)
(Doi et al., 1990).
ряде микроорганизмов все phb гены объединились в один оперон, а в других – разделились на отдельные транскрипционные единицы.
Таким образом, ключевыми ферментами синтеза ПОА являются кетотиолаза, редуктаза и ПОА-полимераза (синтаза). Путь внутриклеточной деградации ПОБ заключается в деполимеризации ПОБ деполимеразой (гидралазой) до димеров и мономеров; мономеры под воздействием бутиратдегидрогеназы превращаются в ацетацетат, который ацетацетил-КоА синтазой (тиофоразой) в трансферазной реакции превращается в ацетацетил-КоА, являющийся субстратом для кетотиолазы, трансформирующей его в ацетил-КоА. Последний утилизируется внутриклеточно в системах катаболизма и анаболизма. Таким образом, кетотиолаза является первым ферментом синтеза и последним ферментом деградации в цикле ПОБ
(Oeding, Schlegel).
В последние годы все чаще появляются, в большей степени предположительные, сообщения о циклической природе системы синтеза и деградации ПОБ в клетках. Например, об этом свидетельствуют опыты по изучению переключения синтеза ПОБ на ПОБ-со-
65
ПОВ у A. eutrophus на разных углеродных субстратах (Doi et al., 1990). Клетки, содержащие 55 % ПОБ от абсолютно сухого вещества клетки, выращивали на пентановой кислоте в условиях азотного лимита. В течение 96 часов гомополимер был заменен сополимером, содержащим 44 мол. % бутирата и 56 мол. % валерата. После пересева клеток в среду, содержащую бутират, уровень оксивалерата в полимере упал с 56 % до 19 %. Эти результаты авторы объясняют тем, что в клетках одновременно идет синтез и деградация полимера. Это позволяет перестраивать состав полимера в зависимости от подаваемого углеродного субстрата. Циклический процесс ПОА метаболизма можно проиллюстрировать схемой (рис. 2.5) из работы (Doi et al., 1990). Аналогичная модель цикличности внутриклеточного процесса синтеза и деградации ПОБ предложена для Azospirillum brasilense (Tal et al., 1990).
Однако изучение обмена ПОБ у водородных бактерий, выращиваемых в условиях непрерывной культуры на среде с высоким соотношением С/N и с добавлением меченой глюкозы, показали, что радиоактивность в биомассе и в полимере падает с одинаковой скоростью. Авторы считают, что в течении роста не происходит существенного обмена ПОБ, а активность деполимеразы или очень низкая, или не проявляется совсем (Haywood et al., 1989).
2.5. Продуценты полиоксиалканоатов
Список микроорганизмов, способных с теми или иными выходами внутриклеточно аккумулировать полиоксибутират или продукты сополимеризации ПОБ с другими оксипроизводными жирных кислот, быстро пополняется. К настоящему времени он насчитывает свыше
300 организмов (Anderson, Dawes, 1990; Steinbüchel, Valentin, 1995; Braunegg et al., 1998; Madison, Huisman, 1999). Среди описанных ор-
ганизмов – аэробные и анаэробные бактерии, гетеротрофы, хемооргано- и хемотрофы, фототрофные прокариоты. (Azotobater, Alcaligenes, метанотрофы Bacillus, Nocardia, Methylobacter, Pseudomonas, Rhizobium, Zoogloea); аэробные фотобактерии (Chloroglaea, Chloroflexus); олиготрофные полипростековые бактерии (Labrys, Prosthecomicrobium, Stelle), архебактерии (Haloferax), анаэробные фототроф-
ные бактерии (Chromatium, Rhodosperillum) и другие.
Несмотря на имеющееся разнообразие изученных микроорганизмов, аккумулирующих ПОА, для промышленного использования рассматривается очень небольшое число продуцентов. Среди них – хемоорганотрофный организм Ralstonia (до недавнего времени известный как Alcaligenes), способный использовать различные источники углерода и гетеротрофные микроорганизмы, относящиеся к трем таксонам – Methylotrophus, Methylobacterium и Pseudomonas
66
(Anderson, Dawes, 1990; Lee, 1996; Choi, Lee, 1997; 1999; Steinbüchel,
Valentin, 1995; Braunegg et al., 1998; Madison, Huisman, 1999).
В качестве критериев для выбора потенциального продуцента полиоксиалканоатов принято рассматривать следующие показатели: химический состав (по соотношению С-мономеров, в % к полимеру), выход полимера (в % по отношению к весу абсолютно сухого вещества клетки), затраты углеродного субстрата (ед. веса/ед. веса ПОА), концентрацию биомассы клеток в культуре (вес/ед.объема), продуктивность процесса (ед. веса ПОА/ед. объема культуры/ед. времени). Результаты продукции полиоксиалканоатов наиболее перспективными продуцентами представлены в таблице 2.3.
Таблица 2.3 Образование полиоксиалканоатов различными микроорганизмами
(Lee et al., 1996b)
|
|
Основной |
|
|
ПОА, |
Продуктив- |
|
Бактерии |
ПО ПОА |
источник |
Х, г/л |
ПОА, г/л |
в % |
ность, |
|
|
|
углерода |
|
|
к АСБ |
г/л/час |
|
|
|
|
|
|
|
|
|
Alcaligenes |
ПОБ |
глюкоза |
164.0 |
121.0 |
76.0 |
2.42 |
|
eutrophus |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Al.еutrophus |
ПОБ |
СО2+Н2 |
91.3 |
61.9 |
67.8 |
1.55 |
|
|
|
|
|
|
|
|
|
Al. еutrophus |
ПОБ |
гидролизат |
106.0 |
61.9 |
57.5 |
1.03 |
|
тапиоки |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Al. еutrophus |
ПОБ-ПОВ |
глюкоза + |
158.0 |
117.0 |
74.0 |
2.55 |
|
пропионат |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Alcaligenes |
ПОБ |
сахароза |
143.0 |
71.4 |
50.0 |
3.97 |
|
latus |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Al. latus |
ПОБ |
сахароза |
– |
16.2 |
50.0 |
2.6 |
|
|
|
|
|
|
|
|
|
Azotobacter |
ПОБ |
глюкоза |
40.1 |
32.0 |
79.8 |
0.68 |
|
vinelandii |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Methylobacterium |
ПОБ |
метанол |
250.0 |
130.0 |
52.0 |
1.86 |
|
organophilum |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Chromobacterium |
ПОВ |
валерат |
39.5 |
24.5 |
62.0 |
– |
|
violaceum |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Protomonas |
ПОБ |
метанол |
233 |
149.0 |
64.0 |
0.88 |
|
extorquens |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Pseudomonas |
ПОГ-ПОО |
n-октан |
11.6 |
2.9 |
25.0 |
0.58 |
|
oleovorans |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Ps. oleovorans |
ПОГ-ПОО |
n-октан |
37.11 |
12.1 |
33.0 |
0.32 |
|
|
|
|
|
|
|
|
|
рекомбинант |
ПОБ |
глюкоза |
101.4 |
81.2 |
80.1 |
80.1 |
|
E. coli |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
рекомбинант |
|
|
|
|
|
|
|
Klebsiella |
ПОБ |
меласса |
37.0 |
24.0 |
65.0 |
65.0 |
|
aerogenes |
|
|
|
|
|
|
67
2.5.1. Природные штаммы – продуценты ПОА
Первыми в 70-х гг. существенный коммерческий интерес вызвали метилотрофные микроорганизмы в связи с доступностью и относительно низкой ценой метанола.
Принципиальная возможность использования метанола в качестве углеродного субстрата для получения полиоксиалканоатов была продемонстрирована на примере различных микроорганизмов:
Protomonas, Methylobacterium, мутантных штаммов Ralstonia eutropha, а также Pseudomonas denitrificans. Так, Methylobacterium extorquens, выделенный из почвы, синтезирует гомогенный полиоксибутират и его сополимеры с валератом (Bourque et al., 1992), соответственно, на метаноле и смесях метанола с валератом. В режиме с подпиткой субстратом на комплексном азотном источнике (с добавками рыбного экстракта), при контролируемой ЭВМ подаче метанола в культуру, скорость образования ПОА достигает 1.7 г/л ч; включение валерата в полимер может составлять до 20 мол. %. Другой изолят, M. extorquens sp. KCTC0048, помимо сополимеров 3-ПОБ-со-3-ПОВ, способен аккумулировать сополимеры 3-ПОБ-со-4-ПОБ при различном соотношении фракций 3-ПОВ и 4-ПОБ (Kang et al., 1993). К продукции ПОБ на метаноле при лимитировании роста азотом, а также магнием или фосфатом, способен факультативный метилотроф
Pseudomonas 135 (Daniel et al., 1992); мутантный штамм R. eutropha,
аккумулирующий ПОБ и ПОБ-со-ПОВ в периодической культуре при лимите азота (Alderete et al., 1993; Park, Damodaran, 1994), в т. ч. на средах с этанолом и пропанолом.
Детальное изучение метилотрофных организмов показало, что они не отвечают всем необходимым критериям, так как выходы полимера у метилотрофов недостаточно высокие (50–60 % к АСБ), а синтезируемый полимер характеризуется низкой молекулярной массой (40 000–60 000 Da). Затраты субстрата на образование полимера высоки (экономический коэффициент образования ПОА на мета-
ноле, Y, г/г, 0.18–0.20).
Azotobacter был следующим микроорганизмом, рассматриваемым в качестве потенциального продуцента ПОА. Интересен в этом плане организм Azotobacter vinelandii UW, синтезирующий полиоксибутират на доступных углеродных субстратах (Page, Knops, 1989). Обнаружив очень низкий уровень НАДН оксидазной активности в выделенном организме, авторы связали эту особенность со способностью организма эффективно синтезировать полиоксибутират с высоким выходом (до 65–75 % к сухому веществу клетки) во время экспоненциального роста, посчитав, что процесс синтеза ПОБ есть один из путей, в котором возможно восстановление НАД. Далее было показано, что синтез ПОБ связан с азотфиксацией (Page, 1992; Page, Cornish, 1993). Авторы показали, что при азотфиксации в штамме
68
UWD во время истощения азота в ассимиляционных условиях этот процесс зависит от полиоксибутирата, так как последний обеспечивает энергией реакцию нитрогеназы. Добавки в среду рыбного пептона в качестве комплексного источника азота стимулируют высокую скорость синтеза ПОБ на фоне высокого урожая биомассы. Штамм также способен утилизировать мелассу, а при индуцирующих добавках пропионата накапливает сополимеры 3-ПОБ-со-3-ПОВ. Максимум продукции полимера при этом составляет до 1 г/л в час. При росте на среде с валератом в качестве единственного источника углерода уровень 3-ПОВ в полимере достигает 45 мол. %. Однако процесс синтеза полиоксиалканоатов в азотобактере не стабилен и сопровождается накоплением в клетках полисахаридов, что затрудняет процедуру экстракции полимера и отражается на его свойствах. Ряд штаммов Azotobacter beijerinckii рассматривают в качестве потенциальных продуцентов ПОА на средах с мелассой, продуктах гидролиза кукурузы и т. п. Возможности оптимизации процесса позволяют надеяться на достаточно продуктивный процесс синтеза полимера при оптимальной концентрации мелассы, равной 65.4 г/л
(Purushothaman et al., 2001).
Третьими организмами, вызвавшими интерес, в частности ICI, были хемоорганотрофные водородные бактерии Ralstonia (Alcaligenes), которые синтезировали высокомолекулярный полимер с высокими выходами (до 80 % и выше), используя в качестве источника углерода при автотрофном росте диоксид углерода (в смеси с водородом), а при гетеротрофном – фруктозу. В результате был реализован первый крупномасштабный процесс получения полиоксибутирата на фруктозе при стерильной ферментации в аппарате объемом 200 000 л (Byron, 1987).
Бактерии, относящиеся к таксону Ralstonia eutrophа, синтезируют полиоксиалканоаты с высокими выходами на минимальной солевой среде при нормальном рН и 30 С, используя в качестве источника углерода углекислоту, а также разнообразную органику, однако из сахаров – только фруктозу. Усиление скорости синтеза ПОА начинается в конце линейной фазы роста бактерий в условиях периодической культуры по мере снижения скорости синтеза белка и достигает максимума на стационарной фазе. Происходит это у R. eutrophus при так называемом несбалансированном росте, лимитированном одним из элементов минерального питания (азотом, фосфором, серой и др.). Выходы ПОА, длительность ферментационного цикла на различных субстратах при различных режимах выращивания и продуктивность процесса варьируют в широких пределах, соответственно,
70–87 %, 60–120 час, 0.3–2.42 г/л/час (Byron, 1992; 1994).
В литературе описано много штаммов данного микробного вида. Наиболее изученными и используемыми в качестве продуцента
69