Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
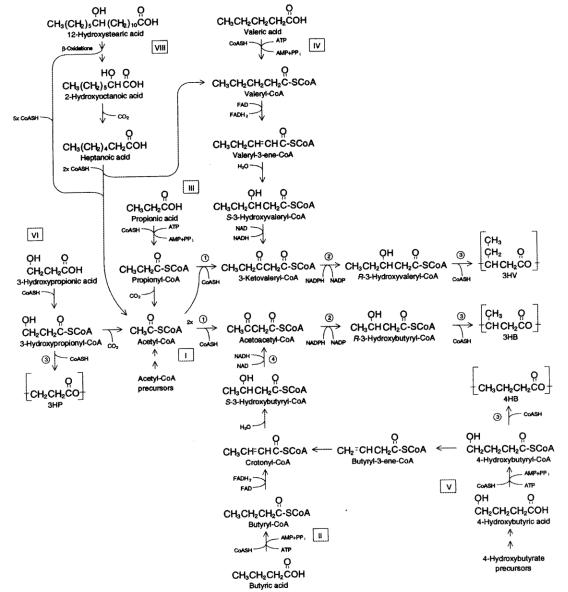
практически одинаковы у различных микроорганизмов (Alcaligenes, Azotobacter, Pseudomonas) (рис. 2.2).
Условия, обеспечивающие изменение направления анаболизма клеток с белковой программы в сторону синтеза и аккумуляции полиоксибутирата, определяются окислительно-восстановительным состоянием цитоплазмы, внутриклеточной концентрацией пирувата и свобод-
ного КоА (Oeding and Schlegel, 1973; Senior and Dawes, 1973). При оп-
тимальных условиях роста пируват, а также восстановительные эквиваленты в виде НАДН и НАДФН расходуются в основном в цикле трикарбоновых кислот на образование аминокислот, а также преобразование энергии в клетке, при этом сохраняется высокий уровень сво-
Рис. 2.2. Обобщенная схема синтеза ПОА у R. еutrophа
1 – β-кетотиолаза; 2 – НАДФН-зависимая ацетоацетил-КоА редуктаза; 3 – ПОА-синтаза; 4 – НАДН-зависимая ацетоацетил-КоА редуктаза (Braunegg et al., 1998).
60
бодного КоА, что является препятствием для синтеза ПОБ. При несбалансированном росте, например при отсутствии азота в среде или дефиците кислорода, пируват не включается в цикл трикарбоновых кислот, а подвергается карбоксилированию с образованием ацетил-КоА, уровень свободного КоА при этом низок, что является благоприятным условием для активизации ферментов цикла ПОБ.
Полиоксибутират и другие ПОА ассоциируются в клеточной цитоплазме в виде включений (гранул); предложенная модель их фор-
мирования (Gerngross, Martin, 1995) показана на рис. 2.3.
Прежде всего, растворимая ПОБ-полимераза (синтаза) взаимодействует с возрастающими концентрациями 3-оксибутирил-КоA в цитоплазме, приводя к праймингу фермента. По мере роста длины цепи олигомеры далее формируются в мицеллы. Мицеллоподобные
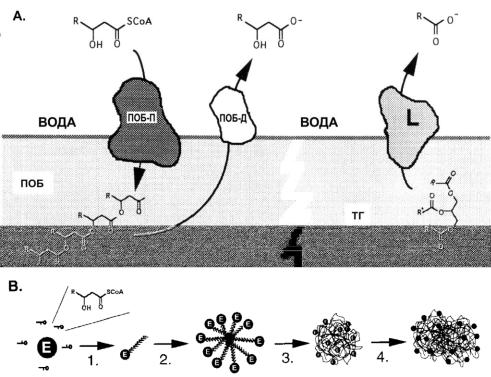
Рис. 2.3.
А. Сходство между ПОБ полимеразой и липазой. ПОБ-полимераза (ПОБ-П) действует на поверхности гранулы ПОБ, где происходит полимеризация растворимых предшественников, которые собираются в гидрофобной области на поверхности гранулы. ПОБдеполимераза (ПОБ-Д) также действует на поверхности, высвобождая мономеры из полимера. Обе эти реакции сходны с реакциями, катализируемыми липазами (L), которые гидролизуют эфирные связи триглицеридов (ТГ) на границе раздела фаз вода/триглицериды.
В. Предполагаемый механизм образования гранул ПОБ. Растворимый фермент конвертирует мономер КоА в олигомеры, которые остаются связанными с ферментом (этап 1). При критической длине олигомера и концентрации комплекса «фермент-олигомер» образуются мицеллы (этап 2). Мицеллы постепенно укрупняются и приобретают форму гранул (этап 3). С ростом числа гранул происходит их слияние, что приводит к образованию крупных агрегатов ПОБ (этап 4).
61
частицы дают границу раздела фаз с полимеразой, расположенной внутри. Фермент затем быстро продолжает ПОБ синтез, вытесняя большее количество ПОБ в возрастающую гранулу. Авторами установлено также, что минимальные условия, необходимые для активации синтеза ПОБ, заключаются в наличии 3-гидоксибутирил-КоA как субстрата и ПОБ-полимеразы.
В последующих исследованиях было показано, что с увеличением размеров гранул в анализируемых пробах возрастает количество белка независимо от того, является ли этот белок ПОБ-поли- меразой или несвязанным белком типа сывороточного альбумина
(Martin, Gerngross, 1996). Белок, кодированный phaP геном, опреде-
ляющий размер ПОА гранул, был идентифицирован в генетических исследованиях R. eutropha. Иммунохимический анализ с антителами показал, что этот белок всегда связан с гранулами и не присутствует в цитоплазме дикого типа в свободном виде. Характеристики phaP связанных белков напоминают таковые олеозинов, – белков, которые связываются исключительно с жировыми телами, выполняя структурную роль и предотвращая сращивание тел. По этой причине, рhaР-подобные белки обычно упоминаются как фазины. К настоящему времени организующая роль белков, связанных с гранулами полимера, показана и для других полимерсинтезирующих микроорганизмов (Stuart et al., 1998; Valentin et al., 1998; Fuller and Clinton, 1999).
Деполимеразы, вызывающие деструкцию полимера, синтезируются микроорганизмами как внутриклеточно, так и внеклеточно. Внутриклеточная деградация ПОБ исследована не так детально, как синтез и внеклеточная деградация полимера, хотя этот процесс может играть решающую роль для физиологии бактерий, продукции полимера в клетке, его качественного состава. Гидролиз полимера осуществляется последовательно ферментами ПОА-деполимеразой, (Д)-оксибутират дегидрогеназой и ацетоацетил-КоА-синтазой (кетотиолазой) (Doi, 1990). Продуктом деградации ПОБ являются мономеры, димеры и короткоцепочечные полимеры Д(-)-3-гидроксибути- рата в соотношении 80–85 %, 15–20 % и следовых количествах, соответственно. Димеры и мономеры Д(-)-3-гидроксибутирата, образованные на первом этапе деградации ПОБ, гидролизуются под действием димер-гидролаз (эстераз) до мономеров. Гидролаза не проявляет активности в отношении других эфиров, а также нативных гранул ПОБ или очищенного ПОБ и ингибируется диизопропилфторфосфатом. Мономеры 3-гидроксибутирата превращаются под действием НАД-зависимой гидроксибутиратдегидрогеназы в ацетоацетат. Ацетоацетат вступает в трансферазную реакцию с сукцинил-КоА, катализируемую тиофоразой (ацетоацетат: сукцинил-КоА КоАтрансфераза), в результате которой образуется ацетоацетил-КоА
62
(Saito et al., 1995; 1996). Под действием кетотиолазы ацетоацетилКоА превращается в ацетил-КоА, который поступает на энергетические и анаболические нужды клетки.
2.4. Генетика внутриклеточной системы синтеза ПОА
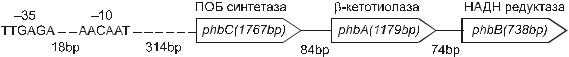
Начиная со второй половины 80-х годов, исследования по проблеме микробиологического синтеза полиоксиалканоатов начали существенно обогащаться работами по молекулярной генетике микроорганизмов, синтезирующих ПОА. Биосинтетический путь образование полиоксибутирата, как было показано, представлен тремя реакциями, которые катализируются тремя ферментами (рис. 2.4). Первый фермент – кетотиолаза – кодируется геном phbA; второй – редуктаза – геном phbB; и третий – полимераза – геном phbC.
Во второй половине 80-х годов была создана библиотека генов Z. ramigera и клонирована в E. coli. С помощью анти-тиолазных антител был выделен ген phbА и было показано, что phbА и phbВ образуют один оперон, а phbС локализуется на другом участке хромосомы (Peoples, Sinskey, 1989 a, b). Практически одновременно с этими работами были клонированы и охарактеризованы гены синтеза ПОБ из R. eutropha (Schübert et al., 1988). Было показано, что гены 3-
кетотиолазы (phbА), ацетил-КоА редуктазы (phbВ), ПОА синтазы (phbС) образуют один оперон с промотором, оператором и структурными генами (Schübert et al., 1991). Установлено, что три фермента синтеза ПОА кодируются в следующем порядке – синтаза, тиолаза и редуктаза (Peaples, Sinskey, 1989b). Синтез ПОА контролируется на уровне транскрипции (Slater et al., 1988). Недавно были выделены, секвенированы три гена синтеза ПОБ из A. latus и и экспрессированы в E. coli (Genser et al., 1998). Результаты секвенирования свидетельствуют о высокой гомологии (71–80 %) этих генов с генами R. eutropha, идентичности ориентации и организации соответствующих оперонов. Существенные отличия выявлены только в структуре и активности промотора, которая значительно выше в A. latus. На основании этих результатов авторы предполагают общность происхождения генов, ответственных за синтез ПОБ, у A. latus и R. eutropha.
Рис. 2.4. Организация оперона синтеза ПОА у A. eutrophus (Peoples, Sinskey, 1989; Steinbüchel et al., 1992)
63
К настоящему времени клонировано 42 структурных гена ПОА синтазы из 38 различных микроорганизмов, относящих к различным физиологическим группам. Для 30 генов определена нуклеотидная последовательность, что должно помочь в дальнейшем в понимании функционировании этого фермента (Rehm, Steinbüchel, 1999).
Структура оперонов, ответственных за синтез ПОА, из различных организмов существенно отличается по расположению генов. Так, в
Acinetobacter spp., Pseudomonas acidophila, подобно вышеописанным
A. latus и R. eutropha, гены phbСАB образуют один оперон, хотя порядок их расположения может отличаться (Peaples, Sinskey, 1989; Umeda et al., 1998; Madison, Huisman, 1999). В Paracoccus dinitrificans,
Rhizobium meliloty and Z. ramigera локусы phbАB и phbС генов не связа-
ны (Tombolini et al., 1995; Ueda et al., 1996; Peoples, Sinskey, 1989). ПОА полимераза из Chromatium vinosum, Thiocystis violacea, Synechocystis
представлена двумя субъединицами и кодируется двумя генами phbЕ и phbС. В этих организмах phbАB и phbЕС гены находятся в одном локусе, но имеют дивергентную ориентацию (Hein et al., 1997; Liebergesell,
Steinbüchel, 1992;1993). В Methylobacterium extorquens, Nocardia corallina, Rhizobium etli, Rodococcus ruber, Rodobacter sphaeroides был идентифицирован только ген ПОА полимеразы (Сevallos et al., 1996; Hall et al., 1998; Hustede, Steinbüchel, 1993; Pieper, Steinbüchel, 1992;
Valentin, Steinbüchel, 1993). Полимеразный ген у Aeromonas caviae соседствует с phbJ геном, участвующим в синтезе мономеров ПОА (Fucui, Doi, 1997). В продуцентах средне- и длинноцепочечных ПОА (P. oleovorans и P. Aeruginosa) содержатся два phаС гена, разделенных геном phbZ, кодирующим внутриклеточную ПОА деполимеразу. Две полимеразы, как оказалось, идентичны на 50–60 % по первичной структуре и обладают очень близкой субстратной специфичностью
(Huijberts et al., 1992; Huisman et al., 1991; Timm, Steinbüchel, 1992).
Данные по разнообразию структуры генома, кодирующего систему синтеза ПОА, дают почву для некоторых рассуждений по поводу ее эволюции. Когда бактерии впервые приобрели способность синтезировать полимер, то, вероятнее всего, он не играл роль запасного материала. Образование ПОА было, возможно, минорным метаболическим путем у этих организмов и результатом какой-либо побочной реакции. Когда синтез полимера стал физиологически значимым для микробов, вероятно, произошла селекция штаммов, аккумулирующих ПОА под воздействием определенных условий, которые в настоящее время неизвестны. Знание этих условий могут быть чрезвычайно полезными для оптимизации процессов получения ПОА рекомбинантными организмами. В процессе эволюции ген, кодирующий фермент ПОА-синтазу, комбинировался с генами, ответственными за синтез мономеров, или с генами, включенными в другие реакции ПОА метаболизма, например phbZ. В результате селекции в
64