Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
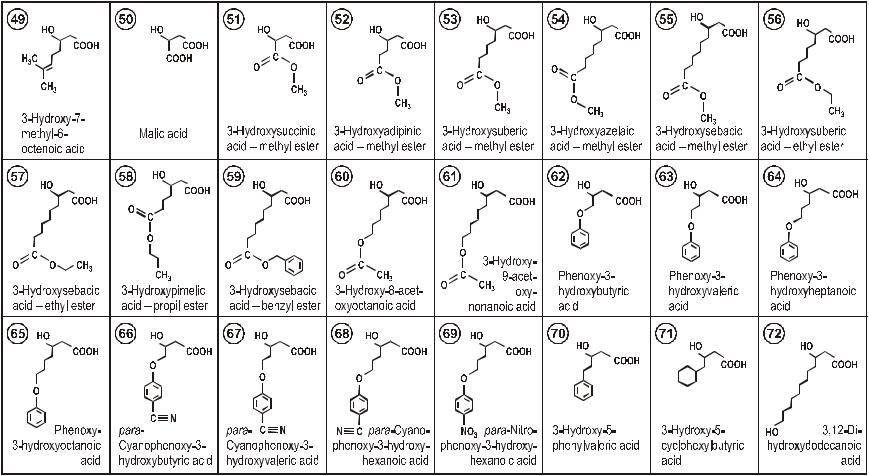
Таблица 2.1 – продолжение
55
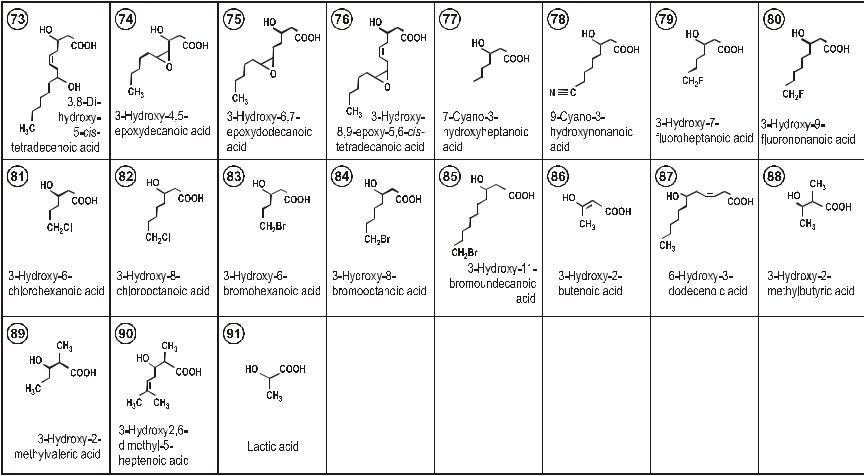
56
Таблица 2.1 – окончание

57
Таблица 2.2
Возможные типы полиоксиалканоатов*
длина гидроксиалкановых кислот
|
C1 |
C2 |
C3 |
C4 |
C5 |
C6 |
C7 |
C8 |
C9 |
C10 |
C11 |
C12 |
C13 |
C14 |
C15 |
C16 |
C17 |
C18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1–OH |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2–OH |
– |
глико- |
лактат |
2HB |
2HV |
2HHx |
2HHp |
2HO |
2HN |
2HD |
2HUD |
2HDD |
2HTriD |
2HTD |
2HPD |
2HHxD |
2HHpD |
2HOD |
лат |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3–OH |
– |
– |
3HP |
3HB |
3HV |
3HHx |
3HHp |
3HO |
3HN |
3HD |
3HUD |
3HDD |
3HTriD |
3HTD |
3HPD |
3HHxD |
3HHpD |
3HOD |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4–OH |
– |
– |
– |
4HB |
4HV |
4HHx |
4HHp |
4HO |
4HN |
4HD |
4HUD |
4HDD |
4HTriD |
4HTD |
4HPD |
4HHxD |
4HHpD |
4HOD |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5–OH |
– |
– |
– |
– |
5HV |
5HHx |
5HHp |
5HO |
5HN |
5HD |
5HUD |
5HDD |
5HTriD |
5HTD |
5HPD |
5HHxD |
5HHpD |
5HOD |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6–OH |
– |
– |
– |
– |
– |
6HHx |
6HHp |
6HO |
6HN |
6HD |
6HUD |
6HDD |
6HTriD |
6HTD |
6HPD |
6HHxD |
6HHpD |
6HOD |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7–OH |
– |
– |
– |
– |
– |
– |
7HHp |
7HO |
7HN |
7HD |
7HUD |
7HDD |
7HTriD |
7HTD |
7HPD |
7HHxD |
7HHpD |
7HOD |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*Steibüchel, Valentin, 1995 b: выделены гидроксиалкановые кислоты, которые постоянно определяются как элементы ПОА биосинтеза (остальные – не всегда). Кислоты: HB – оксимасляная, HV – оксивалериановая, HHX – оксигексановая, HHP – оксигептановая,
HO – гидроксиоктановая, HN – гидроксинонановая, HD – гидроксидекановая, HUD – гидроксиундекановая, HDD – гидроксидодекановая, HtriD – гидрокситридекановая, HTD – гидрокситетрадекановая, HPD – гидроксипентановая, HHxD – гидроксигексадекановая,
HHpD – гидроксигептадекановая, HOD – гидроксиоктадекановая. HASCL, HAMCL, HALCL, соответственно, коротко – , средне – и длинноцепочечные ПОА.
В целом, исходя из длины углеродной цепи оксикислот, образующих полимеры, полиоксиалканоаты подразделяют на три основные группы (таблица 2.2):
1)короткоцепочечные (short-chain-length, SCL), состоящие из кислот с длиной углеродной цепи от 3-х до 5-ти углеродных атомов;
2)среднецепочечные (medium-chain-length, MCL), в составе которых от 6 до 14 атомов углерода;
3)длинноцепочечные (long-chain-length, LCL) с содержанием ки-
слот С17 и С18.
Данное разделение полимеров на группы базируется на существующем представлении о субстратной специфичности ПОАсинтаз, акцептирующих определенные оксикислоты при строительстве полимерной цепи в процессе полимеризации (Anderson, Dawes, 1990). Ранее считалось, что ПОА синтаза A. eutrophus и других природных штаммов способна полимеризовать оксикислоты, состоящие из 3–5 углеродных атомов, но не взаимодействует с оксикислотами с длиной углеродной цепи 6 и более. Поэтому представлялось невозможным получение коротко- и среднецепочечных ПОА природными штаммами Alcaligenes. Однако к настоящему моменту подтверждена более широкая субстратная специфичность PHA-синтез у природных штаммов, включая Ectothiorhodospira shaposhnikovii (Chen et al., 2001), Ralstonia eutropha (Волова со соавт., 1998; Grenn et al., 2002) и
продемонстрирована способность данных организмов к одновременному синтезу коротко- и среднецепочечных ПОА.
Синтазы из различных штаммов P. oleovorans, обладающие более широкой субстратной специфичностью, акцептируют оксикислоты, содержащие от 6 до 14 атомов углерода, поэтому способны синтезировать разнообразные, как средне-, так и длинноцепочечные ПОА (Doi, 1990; Steinbüchel, 1991; 2001; Byron, 1992, Steinbüchel, Valentin, 1995).
Последовательность реакций синтеза полиоксиалканоатов иллюстрирует схема (рис. 2.1). Процесс можно подразделить на три этапа: на первом происходит транспорт источника углерода, необходимого для синтеза полимеров, из внешней среды в клетку, который катализируется специфическими ферментными транспортными системами, локализованными в цитоплазматической мембране или расположенными диффузно внутри клетки. Вторая фаза, включающая комплекс анаболических и катаболических реакций, конвертирует компоненты в гидроксиацил коэнзим-А, тиоэфир которого является субстратом для ПОА-синтазы. На третьем этапе, ПОА синтаза (ключевой фермент биосинтеза данных полимеров), использует тиоэфиры как субстраты и катализирует образование эфирных связей между ними при участии КоА. Данное представление не допускает, что ПОА синтаза для образования полимеров также использует другие
58
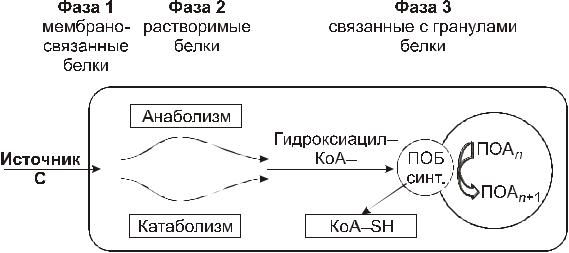
Рис. 2.1. Этапы синтеза ПОА в бактериях (Steinbüchel, Valentin, 1995b).
тиоэфиры гидроксикислот. Вторая фаза – очень существенна для процесса в целом, т. к. во время нее источник углерода конвертируется в субстраты, необходимые для синтеза ПОА. Многие бактерии способны превращать КоА последовательно в ацетацетил КоА и далее – в D(-)-3-гидроксибутирил-КоА, дающий начало полиоксибути-
рату (Anderson, Dawes, 1990).
Охарактеризованные к настоящему моменту типы ПОА теоретически могут дать возможность для получения нескольких миллионов вариантов полимеров. Комбинирование генов систем биосинтеза коротко-, средне- и длинноцепочечных ПОА и варьирование условий выращивания микроорганизмов уже сейчас позволяет получать полиоксиалканоаты разнообразнейших структур: полиоксибутират, полиоксивалерат, полиоксигексаноат, полиоксиоктаноат и двух-, трех- и четырехкомпонентные смеси с различным набором и соотношением гидроксибутирата и гидроксивалерата, гидроксигексаноата и гидроксиоктаноата
(Tim et al., 1992; Steinbüchel, Valentin, 1995b; Braunegg et al., 1998).
2.3. Биохимические пути синтеза полиоксиалканоатов
Полиоксиалканоаты синтезируются в ходе сложного многоступенчатого биосинтетического процесса, каждую стадию которого катализируют специфические ферменты. Знание закономерностей структурно-функциональной организации внутриклеточного цикла ПОА дает возможности управления этим процессом и основу для синтеза полимеров с новыми свойствами.
На примере наиболее изученного из полиоксиалканоатов – полимера β-оксимасляной кислоты, установлено, что пути его синтеза
59