Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
полиоксибутирата за рубежом является штамм Н16 (АТСС 17699), полученный на его основе глюкозоутилизирующий мутант, зарегистрированный в коллекции NCIMB под номером 11599; природные изоляты R. eutrophus SH-69, Alcaligenes sp. AK201.
В России наиболее изученным является организм Alcaligenes eutrophus Z1, выделенный сотрудниками отдела литотрофных культур Института микробиологии РАН под руководством академика Г. А. Заварзина (Cавельева, Жилина, 1968) и отселектированный в проточной автотрофной культуре его высокопродуктивный вариант, зарегистрированный в Российской коллекции промышленных продуцентов как A. eutrophus B5786 (Стасишина, Волова, 1996). Процесс культивирования бактерий реализуется в автотрофных условиях на минеральной солевой среде с использованием в качестве источника углерода и энергии двуокиси углерода и водорода в периодическом режиме в лабораторных аппаратах объемом от 10 до 30 л, оснащенных в качестве перемешивающего устройства турбинной мешалкой открытого типа с частотой 1000 об/мин. Объемный коэффициент массопереноса по кислороду (KLα) составляет порядка 450–600 ч–1. Газовая смесь подается в культуру компрессором мембранного типа с расходом 8–12 л/мин. Соотношение компонентов в газовой смеси для СО2, О2 и Н2 поддерживается близким 1:2:6 по объему (Волова с соавт., 1992).
В связи с тем, что аккумуляция полиоксиалканоатов у подавляющего количества микроорганизмов (за исключением Alcaligenes latus) наиболее активно происходит при несбалансированном росте, вызванном дефицитом одного из биогенных элементов (азот, фосфор, кислород), основной проблемой в ходе создания технологии становится нахождение условий, позволяющих получать одновременно высокие выходы полимера и достаточно высокие выходы биомассы. Как правило, для этого предлагаются периодические двухстадийные процессы, включающие наращивание биомассы на первом этапе при оптимальных условиях культивирования и синтез собственно полимера в неоптимальных условиях – на втором, например, на безазотной среде. Разработанный режим, включающий культивирование бактерий на первом этапе при определенном уровне дефицита азота, позволяет в ходе его накопить достаточную биомассу с определенным уровнем полимера и существенно сократить время второй стадии на безазотной среде (Волова с соавт., 1990; 1992; Волова и Калачева, 1996).
Основные кинетические параметры культуры Ralstoia eutropha в автотрофном режиме биосинтеза полиоксибутирата представлены на рис. 2.6. На первом этапе (30–35 ч.) в растущей и лимитированной по азоту культуре (подача азота составляла 50 % от физиологической потребности клеток) происходит наращивание биомассы до
70
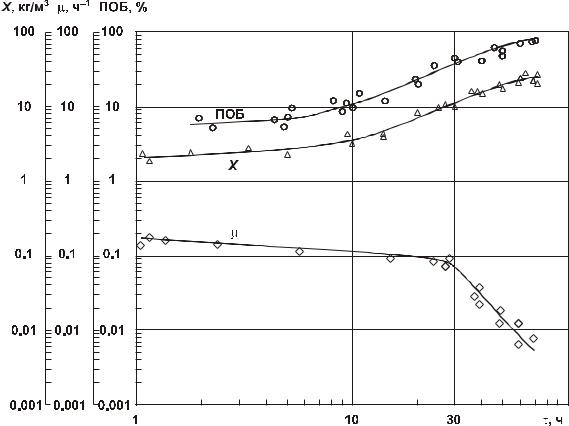
Рис. 2.6. Динамика урожая X, концентрации полиоксибутирата и удельной скорости роста |
автотрофной культуры R. eutropha В 5786 (Волова с соавт., 1992). |
10–12 кг/м3 на фоне постепенного снижения удельной скорости роста бактерий (от 0.15–0,17 до 0.08–0,1 ч.–1) по мере увеличения концентрации клеток в культуре. Содержание полимера в биомассе к концу этапа составляет, как правило, 45–50 %. В течение второй стадии культивирования, реализуемой без подачи азота, концентрация полимера в клетках возрастает до максимальных значений (80 ± 5 %). Повышение величины Х в этот период отражает главным образом увеличение массы полимера в биомассе, а не прирост бактериальной биомассы, т. к. процессы роста и деления собственно клеток, не получающих азота, практически прекращаются.
Данный режим позволяет в течение 60–70 ч. получать высокие выходы полимера при общей концентрации биомассы до 25–30 кг/м3, что сопоставимо с известными зарубежными решениями синтеза ПОА на водороде в биореакторах с близкими массообменными характеристиками.
В ходе ведения процесса синтеза полиоксибутирата и анализа физиологических параметров культуры выявлено возникновение размерной гетерогенности в бактериальной популяции, аккумулирующей ПОБ, усиливающиеся по мере увеличения внутриклеточной концентрации полимера. Электронномикроскопическими исследова-
71
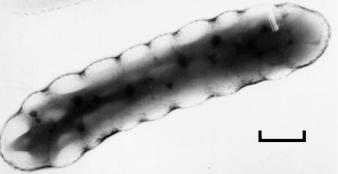
Рис. 2.7. Клетка Ralstonia eutropha B 5786 в периоди-
ческой культуре в стадии максимальной аккумуляции ПОБ (свыше 85 %). Маркер 0.2 мкм (Волова с соавт., 1996б).
ниями показана связь между фазой роста, длиной клеток и гранулообразованием, и внутриклеточным пулом ПОБ (Волова с соавт., 1996б). Установлено, что состояние клеток с максимальными (свыше 70 %) запасами полимера и утратившими способность к синтезу азотсодержащих компонентов и делению, является обратимым в результате эндогенной деструкции и утилизации полимера (Волова с соавт.,1996д).
При изучении физиологической роли полиоксибутирата проанализированы закономерности внутриклеточной деградации полимера (Волова с соавт., 1999) и установлено его участие в процессах репарации клеток в экстремальных условиях роста. Показано, что внутриклеточный пул ПОБ (свыше 40 %) обеспечивает клеткам возможность для роста при неоптимальных значениях рН и температуры среды со значениями удельной скорости роста, в 2.0–2.5 превышающими таковую у клеток, не содержащих ПОБ, а также рост без экзогенного источника углерода и энергии (Волова с соавт., 1996д).
Исследованы кинетические параметры культуры водородокисляющих бактерий Ralstonia eutropha (рис. 2.7) в режиме автотрофного биосинтеза полиоксибутирата на газовом субстрате; определены удельная скорость потребления субстрата, физические свойства культуральной среды, коэффициенты тепло- и массоотдачи, позволяющие реализовать управление и оптимизацию процесса в условиях инженерной практики (Volova, Voinov, 2003).
Замена газового субстрата органическими источниками углерода (ацетатом, фруктозой, глицерином и др.) позволяет увеличить урожай бактерий и сократить время ферментации при сохранении максимальных выходов полимера (Волова с соавт.,1990; 1992). Для расширения сырьевой базы биотехнологии ПОА и возможности привлечения продуктов переработки природного углеродсодержащего сырья (низкосортных бурых углей, гидролизного лигнина и пр.) и в связи с уникальным физиологическим свойством данного штамма – СО-резистентностью, исследована возможность синтеза полиоксиалканоатов в присутствии монооксида углерода как компонента син- тез-газа, получаемого газификацией углеродсодержащего сырья. Исследованы закономерности накопления ПОА в условиях одновре-
72
менного воздействия двух факторов: ограничения роста бактерий дефицитом азота (фактор, стимулирующий накопление полимеров) и ингибирования СО (компонент синтез-газа). У данного штамма на модельных газовых смесях в диапазоне концентрации СО 5–2 0% об. под воздействием ингибитора не отмечено подавления активностей ключевых ферментов синтеза полиоксиалканоатов (β-кетотиолазы, ацетоацетил_КоА-редуктазы, бутиратдегидрогеназы и синтазы), накопление полимера при этом достигает 70–75 % (к абсолютно сухому веществу) без существенного изменения затрат газового субстрата. Хромато-масс-спектральный анализ показал, что синтезируемый полимер является сополимером, в котором доминирует поли-β- оксибутират (ПОБ) (свыше 99 мол. %) со следовыми включениями β- оксивалерата. Полимер по изученным свойствам (молекулярный вес, кристалличность, температурные характеристики) не отличается от ранее полученного на водороде электролизного происхождения (Волова с соавт., 2002; Volova et al., 2002). Эти результаты составили основу для проведения оптимизации процесса газификации бурых углей с целью получения газового сырья для синтеза ПОА (Щипко с соавт., 2003) и разработки способа синтеза полимеров на продуктах газификации углей (Волова с соавт.,2003).
Среди изучаемых организмов известны штаммы, синтезирующие сополимеры 3- и 4-оксибутирата, а также продуценты сополимеров оксибутирата и оксивалерата. Одни из них накапливают сополимерный ПОА при лимитировании роста фосфором на глюкозе с добавками пропионовой кислоты, при этом доля оксивалерата в полимере контролируется величиной добавки пропионата и может со-
ставлять до 30–50 % (Holmes ,1985; Byron, 1992). У других высокий уровень оксивалерата в полимере (до 90 мол. %) достигается при культивировании бактерий на смесях масляной и валериановой кислот, этаноле и валериановой или пентановой кислоте как единственном источнике углерода (Doi, 1990; Kim et al., 1994b; Park,
Damodaran, 1994; Koyama N., Doi Y.,1995). Эти процессы с использо-
ванием дорогостоящих субстратов не рассматривают в качестве возможных для промышленной реализации. Однако штамм (A. eutrophus B5786) способен синтезировать сополимеры оксибутирата с различным включением оксивалерата (от 0.5 до 80 мол. %) при автотрофном росте на смесях углекислоты и водорода при небольших (1–2 г/л) добавках валерата в среду (Волова и др., 1992; 1998).
Бактерии R. eutrophus, помимо полиоксибутирата (ПОБ) и сополимеров оксибутирата-со-оксивалерата (ПОБ-со-ПОВ) (Steinbüchel, Valentin, 1995; Волова с соавт., 1996а), способны синтезировать сополимеры (3-оксибутирата) и (4-оксибутирата ) – (3ПОБ-со-4ПОБ) (Saito et al., 1996); трехкомпонентные полимеры – поли (3-ПОБ-со-3-
ПОВ-со-5-ПОВ) и (3-ПОБ-со-4ПОБ-со-3ПОВ) (Steinbüchel, Valentin,
73
1995) и (3ПОБ-со-3ПОБ-3ПОГ) (Волова с соавт., 1998). Показана также возможность синтеза гомополимера 4- оксимасляной кислоты
– (4ПОБ) на смесях 4-оксимасляной кислоты и цитрата, однако при крайне низком выходе полимера (2 % от АСБ) (Nakamura et al., 1992).
Способность организма синтезировать различные сополимеры вызывает большой интерес в связи с возможностью направленного получения полимеров с заданными свойствами. Поэтому данным исследованиям уделено особое место. Первые исследования по включению 3-ПОБ мономерных единиц в ПОА показали, что оксивалерат может образовываться при конденсации пропионил-КоА с ацетил-КоА при участии кетотиолазы. Различное соотношение ацетата и пропионата в среде как субстрата для роста Ralstonia обеспечивает включение мономеров оксивалерата до 50 % от веса сухого вещества клеток.
С использованием источников углерода, меченых по 13С, установлено, что в образовании поли(3-ПОБ-со-3-ПОВ) сополимеров участвуют 3-кетотиацил-КоА тиолаза, ацетацетил-КоА редуктаза и ПОБполимераза. Когда единственным источником углерода служит валерат, у штамма NCIMB 11599 включение поли(3-оксивалерата) достигает в полимере 85 мол. %. При использовании смеси 5-хлорвалерата и валерата количество синтезируемого трехкомпонентного полимера поли(3-ОБ-со-3-ОВ-со-5-ОБ) достигает 46 % к АСБ, при доле 5-ПОВ, равной 52 % (Doi, 1990; 1995). При использовании в качестве источника углерода смеси масляной и пентановой кислот у штаммов NCIMB 11599 и Н16 включение валерата в виде 3ПОВ достигает, соответственно, 90 и 75 мол. %. Жирные кислоты конвертируют в сополимер (3- ПОБ-со-3-ПОВ) без обязательной полной деградации до ацетил-КоА и пропионил-КоА. При этом (S)-3-гидроксиацил-КоА или 3-кетоацил-КоА непосредственно превращаются в мономеры. Замечено, что этот путь реализуется в присутствии азотного источника в отличие от превра-
щений фруктозы (Doi et al., 1988).
R. eutropha H16 синтезирует сополимеры 3- и 4-оксибутирата на смесях бутирата и 4-оксимасляной кислоты, а также в присутствии 4- хлорбутирата, 1,4-бутандиола или бутуролактона (Kunioka et al., 1989a) Выход полимера достигает 40 % от веса сухой биомассы при доле включения (4-ПОБ) до 37 %. Процесс, тем не менее, вызывает интерес, т. к. увеличение доли данного включения влияет на свойства полимера, снижая температуру плавления и степень кристалличности (Kunioka et al., 1989b), существенно повышая при этом скорость деградации. Известны мутантные штаммы, способные накапливать полимеры с высокими включениями 3-ПОВ и 4-ПОБ, до 96 и 84 %, соответственно, однако при крайне низком общем выходе по-
лимера (Kitamura, Doi, 1994).
Штамм Alcaligenes sp. AK201 образует сополимеры оксибутирата и оксивалерата, используя для роста жирные кислоты с различной
74