Материал: III. хтс
К сожалению, из-за того, что реакция окисления диоксида серы – обратимая, она не протекает на 100%. Рассмотренные выше мероприятия позволяют достичь степени превращения SO2 не выше 98-98,5%. Возможность снижения температуры ограничена активностью имеющихся катализаторов, увеличение давления усложняет инженерное оформление процесса, и потому эти методы пока не получили промышленного применения. Количество выбрасываемого в атмосферу SO2 составляет 10-15 т в сутки. В атмосфере SO2 может окисляться до SO3 под действием солнечной энергии и частиц пыли как катализатора (например, оксиды железа – хорощий катализатор окисления, применявшийся в промышленности).
Этого нельзя допустить. Надо искать решения этой экологической проблемы. Кроме температуры, давления, концентрации есть еще один способ сдвига реакции вправоэто удаление продукта реакции. Предлагается на каком-то этапе протекания реакции, удалить из реакционной смеси образовавшийся SO3 а оставшуюся реакционную смесь направить на повторное окисление остатков SO2. В результате была разработана и действует в настоящее время:
Система двойного контактирования и двойной абсорбции (ДК/ДА)..
(для интенсификации процесса (↑степень превращенияSO3) снизить Т ниже 610К в последних слоях катализатора(но ограничено возможностью катализатора), увеличением Р>1,2МПа (↑Р усложняет конструкцию), удаление продукта)
Метод ДК/ДА позволяет решать концепцию более полного использования сырья (повышение степени окисления SO2) и концепцию минимизации отхода по линии основного материального потока.
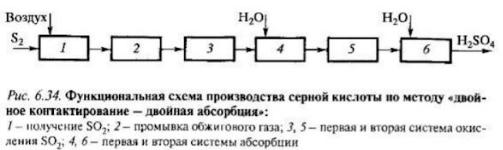
Подсистема получения сернистого газа (обжиг серосодержащего сырья) принципиально не меняется. Полученный сернистый газ частично окисляется в первом реакторе, после чего в первой (промежуточной) ступени абсорбции из него удаляется SO3. Далее оставшийся SO2, окисляется во втором реакторе, и газ направляется на вторую абсорбцию. В отсутствие SO3, окисление SO2, во втором реакторе будет более полным. Каждый реактор состоит из адиабатических слоев катализатора с промежуточными теплообменниками подобно реактору в схеме одинарного окисления
Организация данной схемы требует двойной нагрев реакционной смеси: в первом реакторе от 320 до 690 К, необходимой перед первым слоем, и после его охлаждения до 320-340 К для промежуточной абсорбции SO3, - перед вторым реактором. Нагрев осуществляется за счет теплоты реакции. Но во второй ступени окисляется низкоконцентрированный газ, теплоты реакции выделяется мало - необходимы теплообменники с большой поверхностью теплообмена. Увеличить общее количество выделяемой теплоты можно за счет увеличения начальной концентрации SO2. По этой причине в системах ДК/ДА используют газ, содержащий не менее 10% SO2, Во избежание перегрева катализатора в первом слое значения температуры на входе не должны превышать 695 К, для чего используют низкотемпературные катализаторы.
Количество непревращенноro SO2 (и, следовательно, выбросов в атмосферу) в системе ДК/ДА уменьшается почти в 10 раз по сравнению с системой однократного контактирования, что требует дополнительных экономических затрат, так как поверхность теплообменников увеличивается в 1,5-1,7 раза.
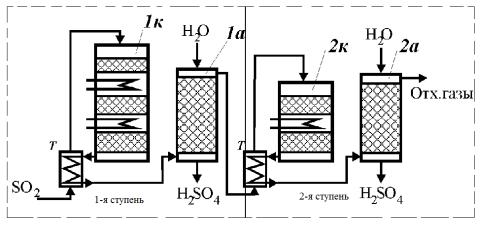
Рис. 4. Технологическая схема контактного отделения окисления SO2 и абсорбции SO3 по методу ДК/ДА: 1к, 2к – контактные аппараты (реакторы); 1а, 2а – абсорберы; Т – теплообменники
На первой ступени окисления использован трехслойный реактор 1к,. Концентрация SO2 в поступающем газе - 9,5-10,5%. Степень превращения на выходе из реактора 90-95%. Промежуточная абсорбция SO3 идет в включает абсорбер 1а,. После него газ содержит только 0,6-1%. Поскольку во второй ступени тепла выделяется мало (из-за низкой концентрации SO2), для нагрева газа до температуры реакции используют теплообменник после второго слоя реактора 2к. Степень превращения оставшегося SO2 составляет примерно 95%, общая степень превращения - 99,6-99,8%. В этой схеме реакционную смесь приходится нагревать дважды сначала до температуры реакции перед головным слоем первого реактора, и после его охлаждения, что необходимо для промежуточной абсорбции SO3 перед вторым реактором. Нагрев осуществляется за счет тепла реакции (прием, который называется регенерация тепла).
Концепция более полного использования сырья в ХТС производ-
ства серной кислоты решается путём повышения степени обжига колчедана, повышения степени окисления диоксида серы и увеличения степени абсорбции триоксида серы.
Концепция эффективного использования энергоресурсов в ХТС производства серной кислоты решается путём использования тепла сгорания серосодержащего сырья в котле-утилизаторе и путём регенерации теп-
ла окисления диоксида серы для подогрева обжигового газа перед его подачей в реактор окисления. Одновременно при этом охлаждается поток га-
за между слоями катализатора так, что процесс окисления диоксида серы протекает вблизи линии оптимальных температур.
ХТС производства азотной кислоты
Немного истории, это интересно. В 1914 г. разработан и в 1916 г. в г. Юзовка (ныне Донецк) пущен в эксплуатацию цех азотной кислоты на основе аммиака из коксового газа. Разработка велась под руководством русского инженера И.И. Андреева. Сейчас получение азотной кислоты из аммиака - основной способ ее производства.
Химическая м функциональная схемы производства азотной кислоты.
Сырьем является синтетический аммиак, кислород воздуха и вода. Протекают
реакции: |
|
окисление аммиака кислородом воздуха |
|
4NH3 + 5O2 = 4NO + 6H2O + Q1; |
(1) |
доокисление оксида азота до диоксида азота |
|
2NO + O2 = 2NO2 + Q2; |
(2) |
поглощение NO2 водой с образованием азотной кислоты |
|
3NO2 + H2O = 2HNO3 + NO + Q3. |
(3) |
Одновременно с третьей реакцией проводят вторую, так что весь NO2 |
можно |
превратить в HNO3. Все реакции экзотермические. |
|
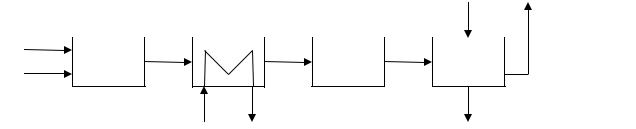
Исходя из химической схемы (1-3), функциональная схема будет включать подсистемы окисления аммиака, последующее охлаждение газов (реакция (1) протекает с выделением тепла при высокой температуре) и утилизация тепла реакции, окисление оксида азота и абсорбцию образовавшихся нитрозных газов водой (рис. 1). Не забыть об отделении очистки аммиачновоздушной смеси (АВС) от разного рода примесей, которые вредят работе катализатора окисления аммиака.
|
|
|
|
|
|
|
|
Отходящие |
|
|
|
|
|
|
|
|
газы |
Воздух |
|
|
|
3 |
|
4 |
|
|
1 |
2 |
|
|
|
||||
Аммиак
НNO3
Рис.1 Функциональная схема производства азотной кислоты:
1 – подсистема очистки АВС; 2 – окисление аммиака и утилизация тепла реакции; 3 – окисления оксида азота и охлаждение нитрозных газов; 4 – абсорбция диоксида азота
Остановимся на физико-химическом обосновании отдельных стадий производства.
Окисление аммиака. Ф и з и к о - х и м и ч е с к и е с в о й с т в а п р о ц е с с а . Окисление аммиака - сложная необратимая экзотермическая каталитическая
реакция. Аммиак окисляется до N2 |
и NO. Превращение описывается двумя |
||
независимыми стехиометрическими уравнениями: |
|
||
4NH3 |
+ 5O2 |
= 4NO + 6H2O + 904 кДж; |
(4) |
4NH3 |
+ 3O2 |
= 2N2 + 6H2O + 1269 кДж. |
(5) |
Катализатор - платина или платинапалладийродиевый сплав (содержание Pt 81-92%). Температура процесса - 1100-1200 К. В этих условиях практически не образуется закись азота N2O. Из-за обратимости экзотермической реакции (2) ее равновесие при температуре окисления аммиака сдвинуто влево, и диоксид азота также отсутствует.
Схема превращения отличается от системы стехиометрических уравнений (4 и 5) - реакция окисления аммиака включает четыре частные реакции, (исключая образование закиси азота):
NO
1
NH3 |
4 |
3 |
(6) |
|
2
N2
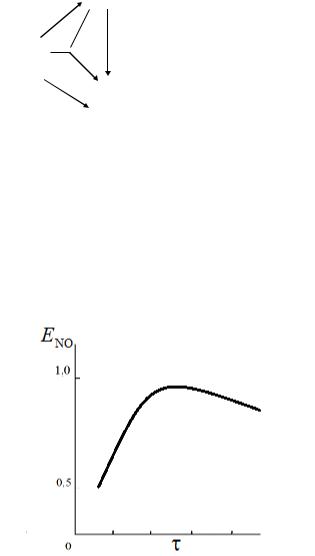
Эта схема была установлена экспериментально: подавая только NO на катализатор, наблюдали образование азота и кислорода по реакции 2NO = N2 + O2; подавая смесь NH3 и NO, наблюдали образование N2 по реакции 4NH3 + 6NO = 5N2 + 6H2O. Такая схема превращения объясняет экстремальную зависимость выхода оксида азота от времени превращения - рис. 2. С ростом реакционная смесь «задерживается» на катализаторе и создаются благоприятные условия для разложения образовавшегося NO до азота.
Рис. 2. Зависимость выхода оксида азота от времени контакта (пребывания)
У с л о в и я п р о ц е с с а . Окисление аммиака относится к гетерогеннокаталитическим процессам. Скорость реакции окисления аммиака при температуре проведения процесса значительно выше по сравнению со скоростью диффузионной стадии, вследствие слабой зависимости коэффициента диффузии от температуры по сравнению с температурной зависимостью константы скорости реакции. Поэтому скорость процесса лимитирует перенос вещёства и тепла из объёма газового потока к внешней поверхности катализатора и сама реакция,