Материал: III. хтс
Окисление диоксида серы.
Ф и з и к о - х и м и ч е с к и е с в о й с т в а п р о ц е с с а .
SO2 + 1/2O2 = SO3 + Qр
Реакция является каталитической, обратимой, экзотермической, протекает на катализаторе с уменьшением объема. Катализаторы окисления SО2 готовят на основе оксида ванадия (V2O5) с добавкой щелочных металлов, нанесенных на оксид кремния. Константа равновесия Кр определяется из уравнения:
Kp |
PSO |
3 |
, p |
|
, |
(5) |
|
|
|
|
|||
PSO 2 , p |
|
PO2 , p |
||||
|
|
|
|
|
где PSO3 ,p , PSO 2 ,p , PO 2 ,p - парциальные давления соответствующих компонентов в состоянии равновесия.
Равновесную степень п р е в р а щ е н и я диоксида серы xр |
получим из |
|||||||
стехиометрического уравнения и условия равновесия (5): |
|
|
|
|
|
|||
xp |
|
|
Kp |
|
|
|
|
(6) |
|
|
|
|
|
|
|
||
Kp |
1 0,5axp |
|
|
|
|
|||
|
|
|
|
|
|
|||
|
P b 0,5axp |
|
|
|||||
|
|
|
|
|||||
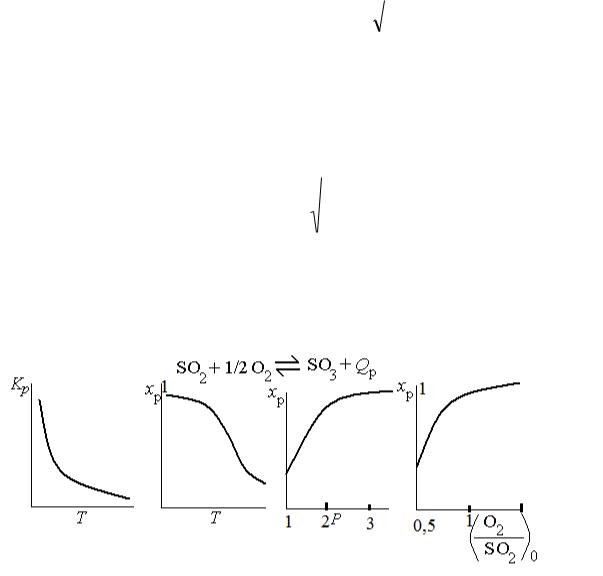
Выражение 1 - 0,5axp показывает относительное изменение (уменьшение) объема реакционной смеси. Уравнение (6) определяет xp в неявном виде и решается подбором или на компьютере. Зависимости Кр, xp от температуры, состава реакционной смеси и давления, состава газа показаны на рис.3.
Из графиков видно, что чем ↑Т, тем ↓хр. С ростом Р => ↑хр. Чем больше
[О2/SO2], тем ↑хр
Промышленно нужные степени превращения (около 99%) достигаются при температурах 675-695 К. Давление не сильно влияет на xp. Поэтому в промышленности процесс проводят при давлении, близком к атмосферному.
С к о р о с т ь р е а к ц и и r описывается уравнением:
|
|
PSO 2 |
|
PSO3 |
|
|
|
|
r kP |
|
1 |
|
|
|
( |
||
|
|
|
|
|
||||
O2 |
PSO2 |
|
|
KpPSO2 |
|
|
|
|
|
A' PSO3 |
PO2 |
|
|||||
где k = koexp(-E/RT) - константа скорости реакции, A' = 0,8 - константа, PSO3 , PSO 2 , PO 2 - парциальные давления соответствующих компонентов, атм.
Для обсуждения и анализа удобно использовать более простой вид
r = (k1 + k 1) с0 (xp x), (8)
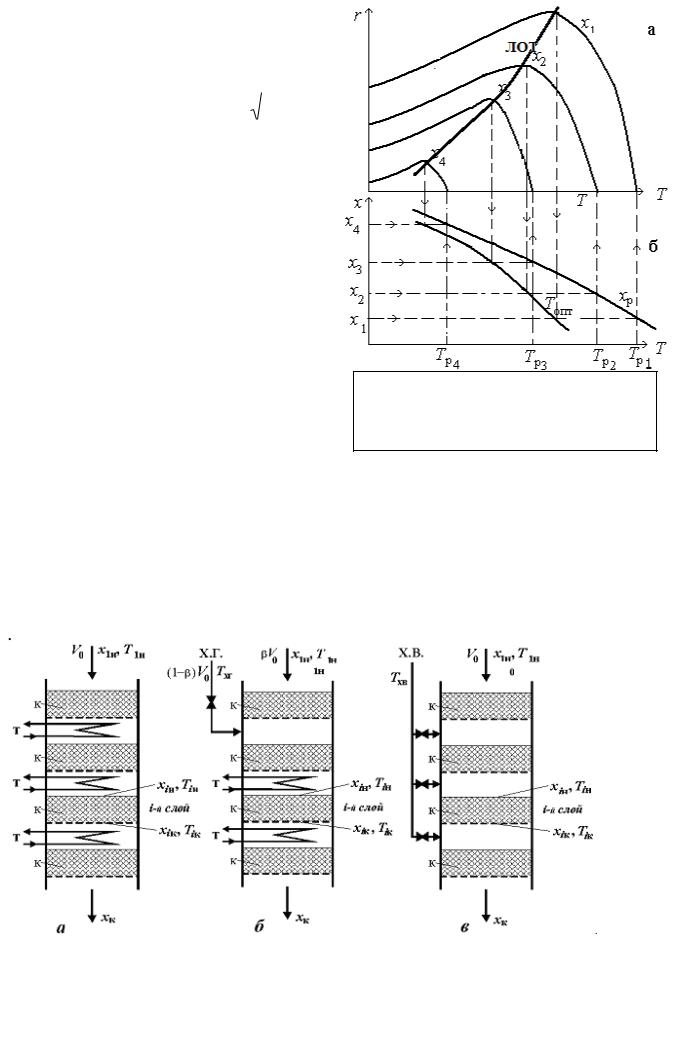
Из уравнений (7-8) видно, что с ростом температуры обе скобки справа ведут себя по разному. В итоге зависимость скорости от температуры проходит через max.
Рис. 4. Зависимость скорости реакции (а) и степени превращения (б) от температуры, x1 x2 x3 x4
С х е м а р е а к ц и о н н о г о у з л а .
В промышленности приближение к теоретической температуре Топт (ЛОТ) осуществляют в многослойном реакторе с адиабатическими слоями катализатора и промежуточным отводом тепла. Охлаждение между слоями осуществляют в теплообменниках или поддувом воздуха или холодного газа (обычно только первого слоя). Наиболее распространенная схема реактора показана на рис. 5.
Рис. 5. Схемы многослойных реакторов окисления диоксида серы с адиабатическими слоями катализатора (к): а – с промежуточными теплообменниками (т); б – с вводом холодного газа (х.г.) после первого слоя и теплообменниками (т) после остальных слоев; в – с вводом холодного воздуха (х.в.)
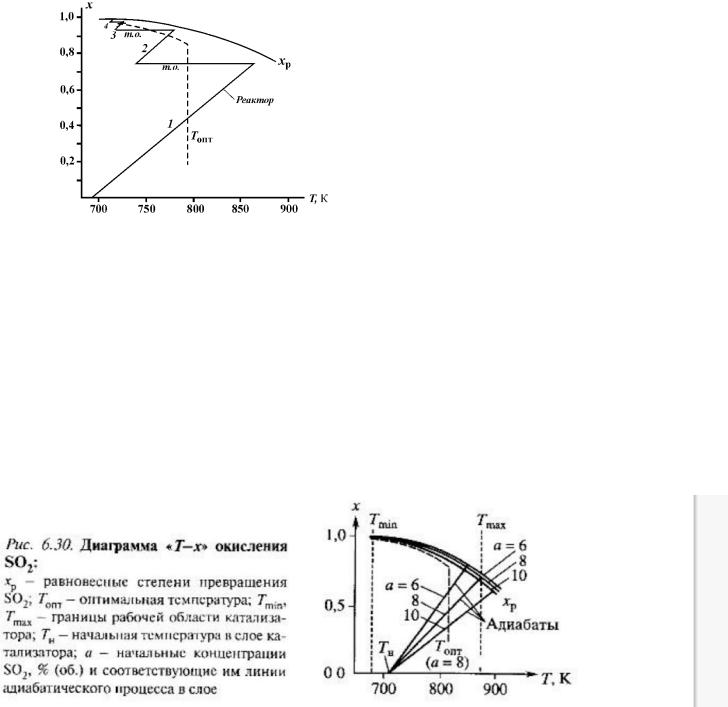
На рис. 6 для варианта а изображены профили температуры и степени превращения по высоте реактора
Рис.6. Графики хр – равновесные степени
превращения; Топт – оптимальные емпературы;
Реактор – режим реактора окисления SO2: 1, 2, 3, 4 – слои катализатора; т.о. – теплообменники
Если по мере протекания реакции с изменением степени превращения х температуру поддерживать равной Топт, то окисление будет протекать с наибольшей скоростью или интенсивностью – это будет теоретический температурный режим. В промышленности его реализуют в многослойном реакторе с адиабатическими слоями катализатора и промежуточным отводом теплоты. Охлаждение межд слоями происходит либо за счет т/о или поддувом холодного газа.
Исходная концентрация перерабатываемого газа выбирается так, чтобы режим процесса находился в пределах рабочих температур катализатора. Начальная Т>713К (температура зажигания), а если будет меньше, то большое значение Е приведет к резкому уменьшению скорости реакции с уменьшением Т.
Адиабатический процесс - прямая линия, наклон которой определен величиной адиабатического разогрева . Чем больше Тад(или исходная концентрация SО2), тем больше разогрев. Процесс может развиваться до установления в сис-ме равновесия, а max Т не должна превышать допустимую.
При выборе процесса в реакторе необходимо проверить его устойчивость. Первый слой в катализаторе с т/о является системой “р-р с внешним теплообменом”, в котором существующий режим м.б. неустойчивым.
Абсорбция триоксида серы
SO3 + H2O = H2SO4 + Qр
Взаимодействие протекает достаточно интенсивно как в жидкой, так и газообразной (паровой) фазах. Кроме того, H2SO4 может растворять в себе SO3, образуя олеум. Этот продукт удобен для транспортировки, поскольку он не вызывает коррозии даже обычных сталей. Растворы серной кислоты чрезвычайно агрессивны. Олеум является основным продуктом сернокислотного производства.
Ф и з и к о - х и м и ч е с к и е ус л о в и я а б с о р б ц и и .
Абсорбция триоксида серы водой описывается экзотермической гетерогенной реакцией газ–жидкость
SO3(г) + H2O(ж) = H2SO 4 + Qр
Реакция быстрая, процесс лимитируется диффузией триоксида серы из газовой фазы в жидкую. Вспомним рекомендации ПАХТ относительно влияния на скорость процесса абсорбции. Скорость записывается в виде:
W βF ( p0SO3 pравнSO3 ) ,
Где -коэффициент массообмена, F-поверхность контакта фаз, p0SO3 и pравнSO3 - парциальные давления SO3 в газовом потоке и равновесное значение над раствором жидкости. Видно, что чем больше , F и разность парциальных давлений (движущая сила) тем больше скорость. Практически это означает, что в абсорбере надо обеспечить хорошие скорости движения контактирующих фаз (турбулентность), использовать насадку для развития поверхности контакта, снижать температуру, что приводит к увеличению растворимости газа в жидкости
и снижению при этом pравнSO |
. Чтобы минимизировать |
pравнSO |
3 |
есть еще один важный |
||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
прием. Посмотрим на фазовую диаграмму тройной системы H2O - H2SO4- SO3. |
||||||||||||
|
|
|
Процесс лимитируется диффузией SО3 |
|||||||||
|
|
|
из газовой фазы в жидкую. Скорость |
|||||||||
|
|
|
абсорбции зависит от парциального |
|||||||||
|
|
|
давления SО3 в газовом потоке и |
|||||||||
|
|
|
равновесного парциального давления |
|||||||||
|
|
|
SО3 над образующимся р-ром Н2SО4, а |
|||||||||
|
|
|
также от Т ( |
↓Т ведет к ↑процесса, т.к. |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
↑растворимость газа |
), пов-ти контакта |
||||||||
|
|
|
фаз и турбулизации потоков. |
|||||||||
|
|
|
Абсорбцию ведут конц. Н2SО4 - 98,3% |
|||||||||
|
|
|
(азеотропная точка): наиболее полное |
|||||||||
|
|
|
поглощение SО3 (max движущая сила). |
|||||||||
|
|
|
Если поглощать р-ром меньшей |
|||||||||
|
|
|
концентрации, то р-я будет протекать в |
|||||||||
|
|
|
паровой фазе - будет образовываться |
|||||||||
|
|
|
сернокислый туман, который уйдет из |
|||||||||
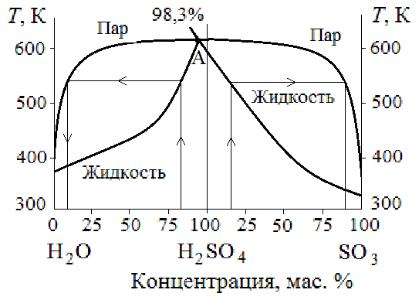
Рис. 7 Фазовая диаграмма тройной системы |
|
абсорбера с газовой фазой (левая часть |
||||||||||
|
графика); либо |
↑ С( |
SО3 |
) приводит к |
|
|||||||
H2O - H2SO4- SO3 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
затрудненной абсорбции |
(правая часть |
|||||||||
|
|
|
||||||||||
|
|
|
графика) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Впаровой фазе левой части графика над раствором серной кислоты присутствуют практически пары воды, реакция поглощения триоксида серы будет протекать в паровой фазе с образованием тумана серной кислоты, который уйдет из абсорбера с газовой фазой.
Впаровой фазе левой части графика присутствует практически чистый триоксид серы, который затрудняет абсорбцию триоксида серы из газового потока.
Вазеотропной точке А в паровой фазе присутствует только кислота и нет SO3, что обеспечивает максимальную движущую силу процесса.
Минимальное содержание воды в паровой фазе наблюдается в азеотропной точке при значении концентрации серной кислоты 98,3 % и образование паров серной кислоты будет минимальным, а абсорбция триоксида серы будет наиболее полной.
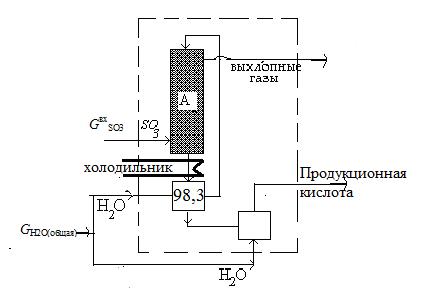
Схема абсорбции
Основные требования:
продукт - олеум
max возможное поглощение SО3
min содержание Н2SО4 в отходящих газах.
Чтобы обеспечить нужную концентрацию H2SO4 в поглощающей жидкости, организована ее интенсивная циркуляция, так что поглощение осуществляется при концентрации H2SO4 98,3 %. Вследствие большого орошения в абсорбере увеличение концентрации за проход жидкости составляет не более 1-1,5%. Все рассмотренные выше условия обеспечивают полное поглощение SO3 и минимальное образование сернокислотного тумана (т.е. решаются концепции ресурсосбережения и минимизации отходв)
Рис.8. Схема абсорбции