Материал: II. хим реакторы

На рис. 4.13 в одинаковом |
|
|
|
масштабе показаны зависимости С( ) |
|
|
|
для режимов ИС-н и ИВ (n = 1). Из |
|
|
|
графика видно, что ив < ис, а значит и |
|
|
|
vp,ив < vp,ис, т.е. процесс в режиме ИВ |
|
|
|
интенсивнее режима ИС. |
Рис. 4.13. |
Зависимость С( ) для |
|
|
|
проточных |
реакторов идеального |
|
|
вытеснения (ИВ) и смешения (ИС) |
|
|
|
|
|
|
|
|
|

Рис. 4.14. Графический метод определения условного времени в реакторах идеального смешения ( ис) и вытеснения ( ив). Пояснения см. в тексте
Этот вывод подтверждает зависимость 1/r(С) для реакторов ИС и ИВ представленная на рис. 4.14 (для обратимой реакции зависимость представлена штриховой линией). Площадь под интегральной кривой (заштрихованный участок “СК – а – b – С0”) равна ив, в то время как ис есть произведение обратной величины скорости реакции при конечной концентрации 1/r(СК) и разности концентраций (С0 - СК) (прямоугольник “ СК – а – d - С0”). Очевидно, что ив < ис. Таким образом, РИВ более интенсивен, чем РИС и с увеличением степени превращения эта разница нарастает. Зависимость, представленная на рис. 4.14, позволяет графически определить условное время реакции .
Такое различие в интенсивности процессов объясняется тем, что концентрация исходного компонента в реакторе ИВ в течение превращения изменяется от С0 до СК, в то время как в реакторе ИС-н процесс протекает при конечном значении концентрации, следовательно, скорость процесса в реакторе ИВ выше.

При протекании сложных реакций реакторы сравнивают не только по интенсивности режимов в них, но и по селективности. На рис. приведена зависимость S' от концентрации для параллельной схемы превращения.
В режиме ИС интегральная селективность процесса будет равна дифференциальной при этой же концентрации - S'(СК) ( отмечено точками). В режиме ИВ селективность процесса будет равна среднеинтегральной величине между S'(С0) и S'(СК) (отмечено крестиками). Из этого следует (селективность определена по продукту R):
при n1 = n2: S'(С0) = S'(СК), SИВ = SИС; при n1 > n2: S'(С0) > S'(СК), SИВ > SИС; при n1 < n2: S'(С0) < S'(СК), SИВ < SИС.
В случае последовательной схемы превращения режим идеального вытеснения - и более интенсивен, и более селективен по промежуточному продукту, а также обеспечивает больший максимальный выход.

Для неизотермического режима
В 1-м случае выгоднее использовать РИВ, там выше скорость реакции при прочих равных условиях. Во 2-м случае, когда на скорость реакции сильнее влияет температура, чем концентрация, для получения максимальной скорости на всем протяжении процесса выгода взять систему из 2-х реакторов РИС-Н и РИВ
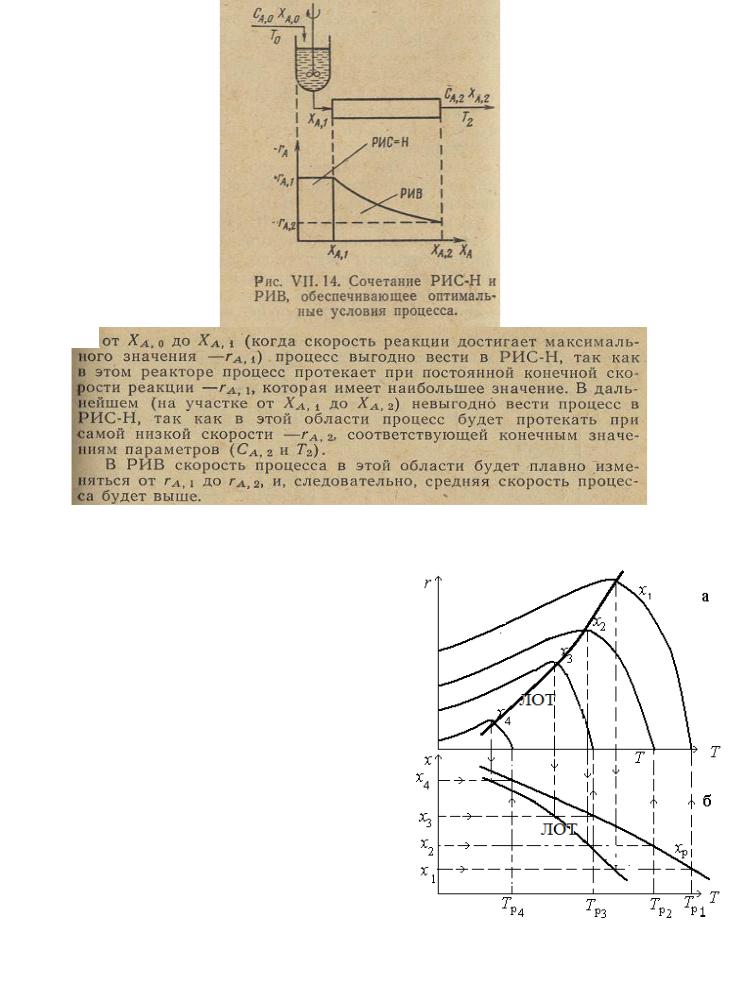
На участке
Реакторы для обратимой экзотермической реакции
Эффективное проведение обратимых экзотермических реакций требует, как известно (было раньше, см. лекцию «гомогенные процессы»), приближения режима процесса к ЛОТ «см. зависимости r(T) и х(Т)». Такое приближение к ЛОТ можно осуществить, например, если секционировать реакционную зону, т.е. разделить ее на участки, (слои катализатора, если реактор –каталитический) и отводить тепло от нагретой реакционной смеси за счет реакции после каждого участка (см. рис. реактора ниже).
Рис. 5. Зависимость скорости обратимой экзотермической реакции (а) и степени превращения (б) от температуры, x1 x2 x3 x4