Материал: II. хим реакторы
ТЕОРИЯ ХИМИЧЕСКИХ РЕАКТОРОВ
Химический реактор - устройство, предназначенное для проведения в нем химических превращений.
Общий вид реактора и схемы некоторых из них приведены на рис.
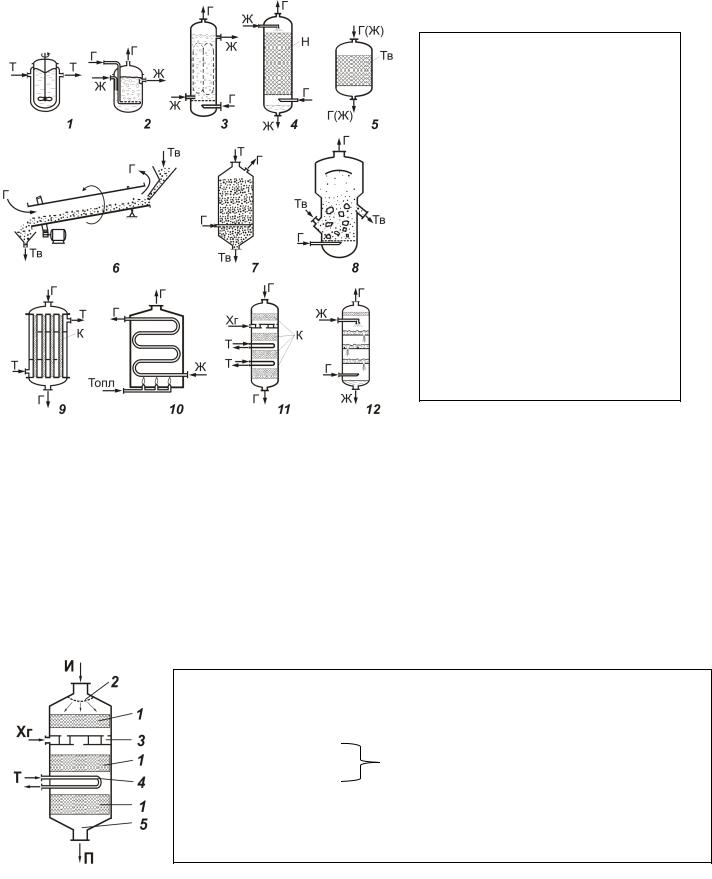
Схемы химических реакторов:
1,2 – емкостной;
3 – колонный;
4 – насадочный;
5-8 для систем Г – ТВ;
9, 10 – трубчатый;
11, 12 - многослойный реактор
Г - газ; Ж - жидкость;
Т - теплоноситель; Н - насадка;
Тв - твердый реагент; К - катализатор; Хг - холодный газ; Топл – топливо.
Классификация реакторов:
по организации мат. потоков (вытеснение, смешения, неидеальный)
по организации тепл. потоков (изотермический, адмабатический, автотермический, с теплообменом (внутренним или внешним))
принцип действия (периодический (непроточный), непрерывный (проточный), полупериодический)
по назначению (гомогенный, гетерогенный, каталитические)
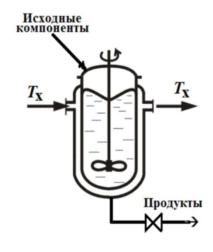
Функциональные (структурные) элементы реактора:
1 |
- реакционная зона (объем реактора, в котором протекает хим. реакция); |
||
2 |
- входное и распределительное устройство; |
||
3 |
- смеситель, |
|
|
Для изменения состава и температуры |
|
||
|
|
|
|
4 |
- теплообменник, |
потока между реакционными зонами |
|
5 |
- выходное устройство; |
|
|
|
|
||
Хг - холодный газ; Т - теплоноситель; И и П - исходный и конечный продукты соответственно
Общий вид математической модели процесса в химическом реакторе
Этапы построения математической модели реактора:
1.Изучить схему организации потоков и их структуру
2.Выбрать элементарный объем в котором отсутствуют градиенты любого параметра
3.Для элементарного объема получить наблюдаемую скорость превращения. Рассмотреть явления переноса, оказывающие влияние на протекание хим. процесса в элементарном объеме
4.Составить уравнение материального и теплового баланса для элементарного объема в алгебраической и дифференциальной форме.
5.Отнести балансовые уравнения ко всему объему или проитегрировать уравнение по всему объему.
Математическая модель процесса в химическом реакторе выглядит
следующим образом: |
|
dN/dt = Nвх + Nист; |
(4.1) |
dq/dt = Qвх + Qист. |
(4.2) |
Здесь dN/dt и dq/dt - накопление вещества и теплоты в выделенном элементарном объеме; Nвх, Qвх - материальные и тепловые потоки, входящие в выделенный объем (покидающие объем потоки имеют отрицательное значение); Nист, Qист - источники вещества и тепла внутри выделенного объема.
Источником вещества является химическая реакция, источником тепла - химическая реакция и фазовые превращения.
Режим (модель) идеального смешения периодический - ИС-п.(рактор1)
Все компоненты загружаются одновременно. За счет интенсивного перемешивания концентрации и температуры в каждый момент времени одинаковы по всему объему vp реакционной зоны (реактора).
ТX - температура теплоносителя
FT - площадь поверхности теплообмена КT - коэффициент теплообмена - КT.

Процесс - нестационарный. В реакторе нет входящих и выходящих потоков иNвх = 0. Источником i-го вещества является химическое превращение:
Nист,i = Wi(С, Т)vp.
Количество вещества в реакторе Ni = vpСi, тогда уравнение (4.1) принимает вид:
dСi/dt = Wi(С, Т); |
(4.3) |
Источник теплоты – тепловой эффект химического превращения |
(для |
единственной реакции Qист = QPr(С, Т)vp) и теплообмен с теплоносителем КTFT(ТX - Т). Уравнение 4.2 примет вид:
dq/dt = QPr(С, Т)vp + КTFT(ТX - Т).
Изменение количества теплоты в реакторе: dq = сpvpdТ (теплоемкость сp
неизменна), удельная поверхность теплообмена: Fуд = FT/vp: |
|
|
|
||||
|
|
сpdТ/dt = QPr(С, Т) - КTFуд(Т - ТX); |
(4.4) |
||||
|
|
|
|
|
|
|
|
|
|
|
dСi/dt = Wi(С, Т); |
|
|
|
|
Математическая модель РИС-п: |
сpdТ/dt = QPr(С, Т) - КTFуд(Т - ТX); |
|
|
||||
|
|
|
при нач. условиях: С=С0, |
Т=Т0, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Режимы работы РИС-п
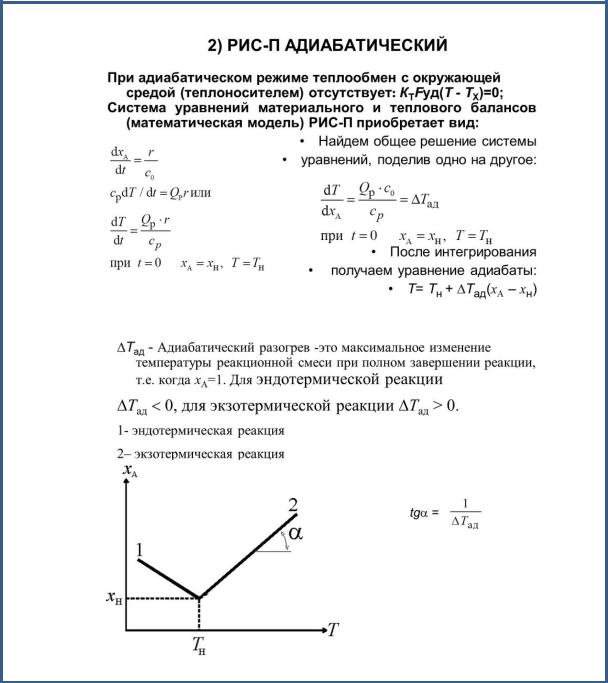
*Более подробно в РИВ