Материал: FTTLabRab
Контрольные вопросы
-
Чем определяется направленность и насыщенность ковалентной связи?
-
Почему ковалентные кристаллы не могут обладать высоким координационным числом?
-
По каким принципам формируются направления связей в ковалентных кристаллах?
-
Почему угол между направлениями связей в метане и алмазе равен 109,5
-
Почему алмаз и кремний обладают высокой прочностью, а графит, сурьма, селен хрупкие?
-
Как на модели трансформировать графит в нанотрубки – волокна, обладающие гигантской прочностью?
-
Почему ковалентные цепочки с координационным числом 2 не выстраиваются в прямую линию?
Лабораторная работа №4 моделирование структуры и дефектов ионных кристаллов
Цели работы
-
Изучить особенности формирования кристаллической решетки в результате взаимодействия разноименно заряженных ионов.
-
Смоделировать искажения решетки, вызванные растворением чужеродного элемента и дефектами кристаллического строения
Теоретическая часть
Простейшая идея о природе ионной связи сводится к тому, что некоторые элементы при химическом взаимодействии стремятся к полностью заполненной оболочке (ns)2(np)6. Металлы, имеющие небольшое число электронов вне полностью заполненной оболочки (ns)2(np)6, отдают эти электроны атомам элементов, к которым нужно добавить небольшое число электронов, чтобы получить полностью заполненную оболочку ближайшего инертного газа. Между получившимися разноименно заряженными ионами возникают силы электростатического притяжения, которые и стягивают ионы вместе. Потенциал сил кулоновского притяжения двух разноименных ионов на расстоянии r
![]() .
.
Разноименно заряженные ионы могут образовывать кристаллы, в которых ионы в узлах решетки удерживаются вследствие электростатического взаимодействия зарядов разного знака. Реально взаимодействие атомов на близких расстояниях не ограничивается электростатическими механизмами. Перекрывание волновых функций электронов вносит существенные поправки в привычное понимание природы ионной связи. Типичные ионные кристаллы образуют соединения щелочных металлов с галогенами – соли, но ионная связь присутствует во многих керамических материалах и, с этой точки зрения, представляет практический интерес.
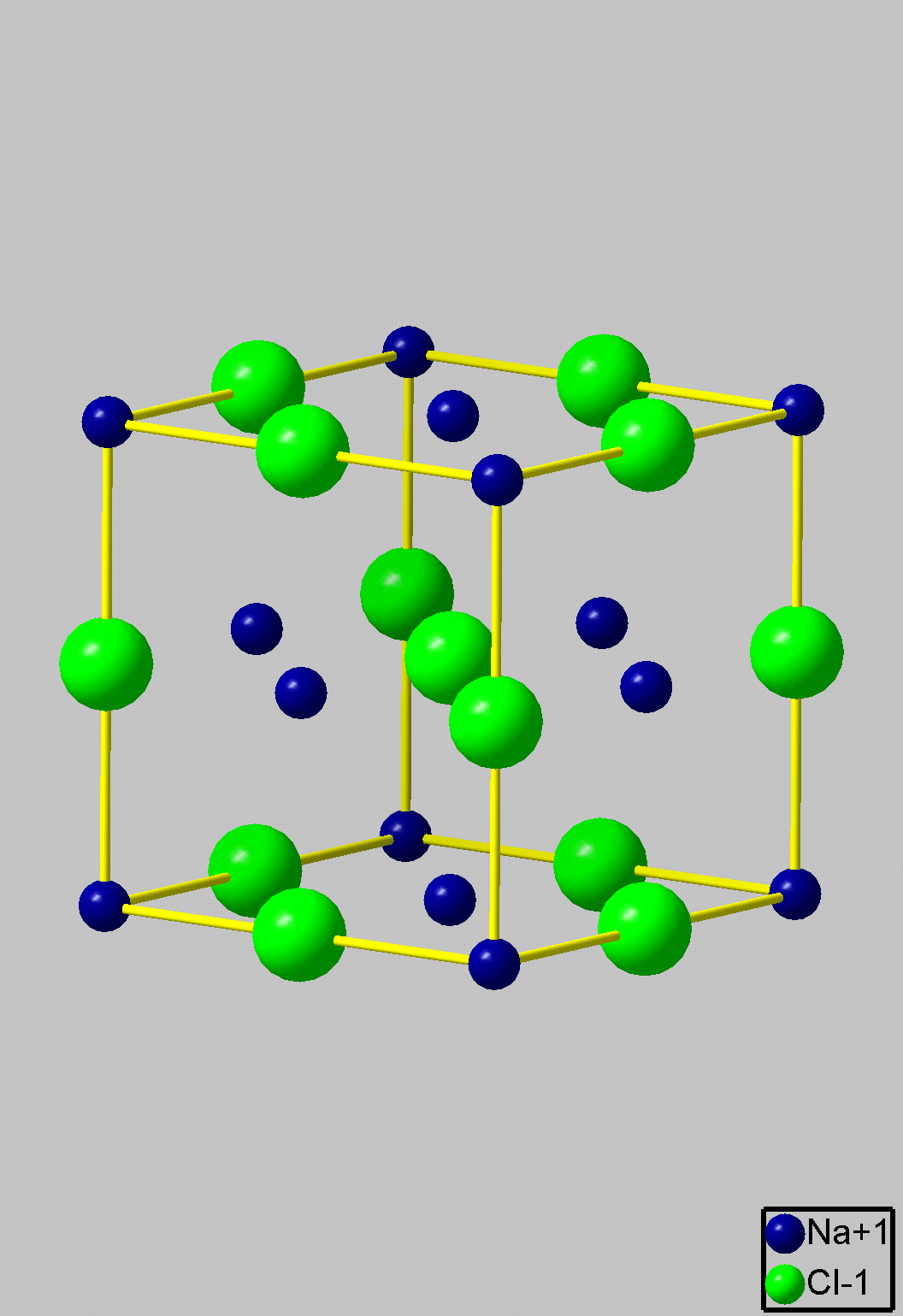
На рис. 6 приведена кристаллическая структура (элементарная ячейка) типичного ионного соединения NaCl. В таком кристалле в узлах решетки поочередно располагаются ионы Na+ и С1–, так что каждый ион натрия окружен шестью ионами хлора, далее следуют 12 ионов натрия... и наоборот, каждый атом хлора окружен шестью атомами натрия и т.д. Следовательно, для двухкомпонентных кристаллов, кулоновский потенциал в точке, занятой положительным ионом, можно вычислить как
![]() ,
,
или для неограниченной кристаллической решетки
![]() ,
,
где АM – константа, которую называют постоянной Маделунга; она зависит от типа кристаллической решетки и заряда ионов; r — расстояние между ионами.
Для возникновения устойчивой молекулы или ионного кристалла необходимо, чтобы силам кулоновского притяжения ионов противодействовали силы отталкивания, связанные с энергией Uот.
Полную энергию связи в ионном кристалле можно записать как
а
б
а б
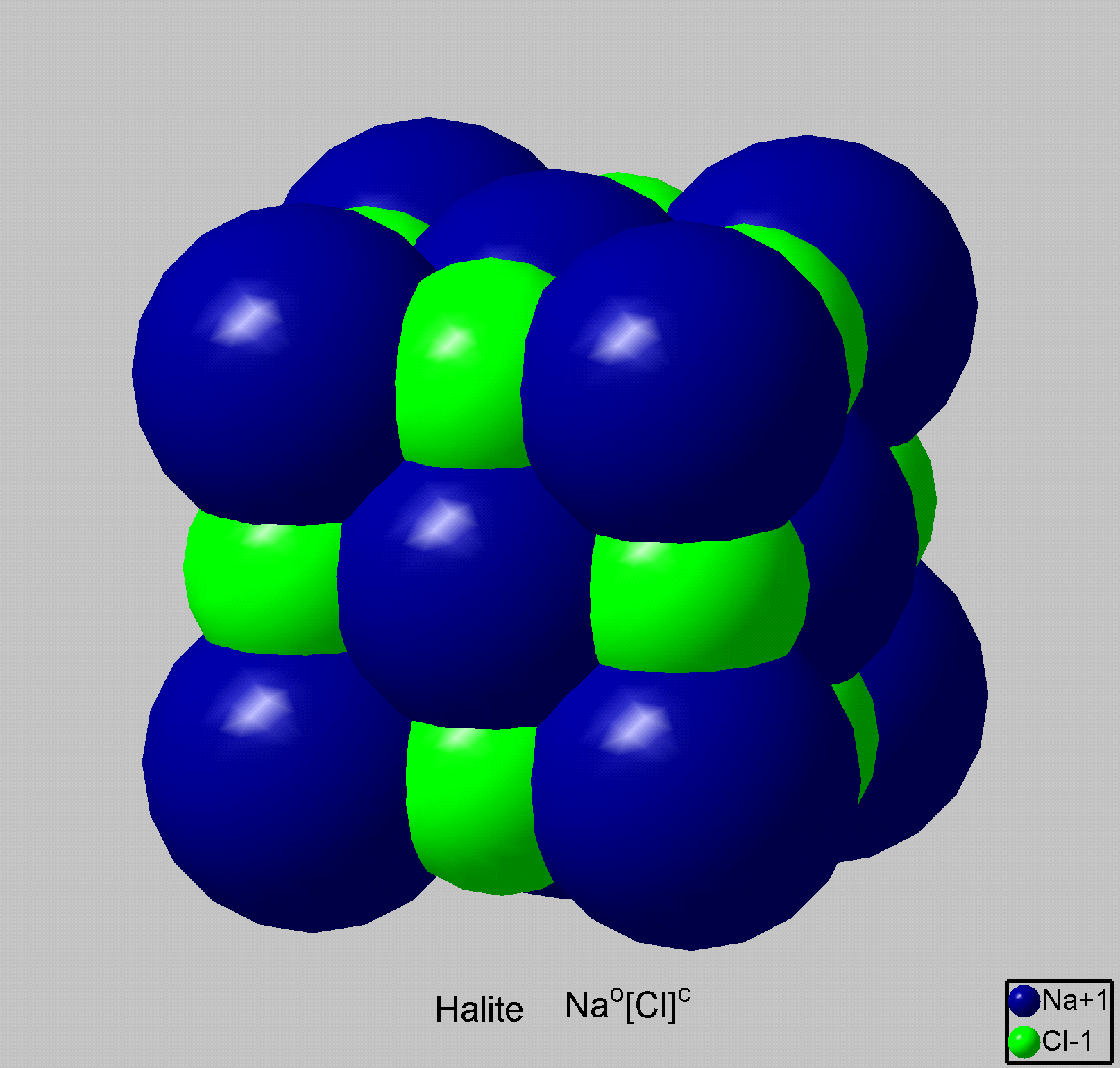
Рис. 6. Модель элементарной ячейки
кристалла NaCl. AM
= 1,748; K = 6, а –
схематичное изображение, б – перекрытие
внешних орбиталей
![]() ,
,
где Е – сродство к электрону; I – энергия ионизации.
При расстоянии между ионами, соответствующем минимуму потенциальной энергии, силы отталкивания равны силам притяжения, что соответствует равновесному, устойчивому состоянию молекулы или ионного кристалла.
Принципиально, электростатические силы могут притягивать любое количество ионов, и число ближайших соседей должно стремиться к максимальному (К=12). Иначе говоря, ненасыщенность и ненаправленность ионной связи предполагает тенденцию к образованию решеток координационного типа. Практически, ионные кристаллы имеют невысокие координационные числа. Этому способствует несколько причин.
Одна из них в том, что реальные значения координационных чисел определяются соотношением ионных радиусов ra/rk. Чем меньше разница радиусов анионов и катионов, тем выше возможное координационное число. Так для решетки NaCl (см. рис. 6, плоскость [100]) из представлений плотной упаковки твердых шаров следует, что ионы натрия заполняют октаэдрические пустоты между более крупными ионами хлора. Это соответствует
![]() ,
,
откуда ra/rk = 0,41.
В структуре другого типичного ионного кристалла CsCl ион цезия занимает октаэдрическую пору, образованную восемью соприкасающимися ионами хлора (К=8). При этом получается что ra/rk = 0,73. Реально наоборот, соотношение ra/rk = 0,73 предопределяет тип кристаллической решетки CsCl. Решетка хлористого цезия может быть представлена, как две кубические примитивные подрешетки, вставленные одна в другую со смещением на ½ периода по трем координатам.
В соединении ZnS двухвалентные ионы существенно отличаются своими радиусами ra/rk = 0,22. Отсюда, обе полиморфные модификации ZnS имеют невысокое координационное число (К=4).
Баланс сил притяжения и отталкивания строго периодичен только в идеальном кристалле. Примесные ионы и дефекты кристаллического строения нарушают баланс сил, вызывая искажения решетки. Вектор смещения узлов различен для разных координационных сфер. Например, при замещении иона Na+ на ион K+, имеющий больший радиус ионы первой координационной сферы (ближайшие 6 соседей) вынуждены раздвинуться по направлению от примесного иона. Ионы второй координационной сферы, наоборот, приближаются и т.д. При образовании вакансии можно ожидать сжатие первой координационной сферы, как это происходит в металлах. Но поскольку, в ионных кристаллах вакансии имеют заряд, то смещение ионов имеет свои особенности, которые предлагается изучить в настоящей работе.
Контрольные вопросы
-
Если ионная связь ненасыщенная и ненаправленная, то почему она не образует кристаллы с высокими координационными числами?
-
От каких факторов зависит координационное число ионного кристалла?
-
Почему ион, находящийся в углу кристалла, больше смещен от положения равновесия, чем ион, находящийся на ребре, и тем более чем ион, находящийся на грани кристалла?
-
Почему при замене одного иона на другой с идентичным зарядом энергия решетки повышается?
-
Почему в металлических кристаллах атомы, находящиеся в первой координационной сфере вокруг вакансии, смещаются в сторону вакансии, а в ионных кристаллах от нее?
Лабораторная работа №5 Построение зоны Бриллюэна для произвольных кристаллических решеток средствами Maple V
(4 часа)
1 Цель работы
Получить представления о возможностях расчетно-графического пакета Maple V для математического моделирования в области физики твердого тела, приобрести элементарные навыки работы с ним, построить и проанализировать изображения 1-й зоны Бриллюэна для различных кристаллических решеток.
2 Теоретическая часть
2.1 Зона Бриллюэна
Понятие зоны Бриллюэна в физике твердого тела возникает при анализе условий дифракции на заданной кристаллической решетке. Исторически сложилось так, что зоны Бриллюэна практически не используются в дифракционном рентгеноструктурном анализе, однако в теории электронных энергетических зон в кристаллах их применение совершенно необходимо. Эффективно это понятие используется и при анализе колебательных спектров кристаллических решеток.
Построение зон Бриллюэна основано на условии дифракции в форме Эвальда:
![]() ,
(1)
,
(1)
которое
связывает волновой вектор падающего
луча
![]() с вектором обратной решетки
с вектором обратной решетки
![]() .
Соотношение (1) эквивалентно закону
Брэгга 2dsinq=nl,
и по этой причине принято ссылаться на
него как на закон Брэгга.
.
Соотношение (1) эквивалентно закону
Брэгга 2dsinq=nl,
и по этой причине принято ссылаться на
него как на закон Брэгга.
Напомним
определение обратной решетки. Пусть
![]() векторы примитивных трансляций некоторой
кристаллической решетки. Объем
элементарной ячейки задается смешанным
произведением тройки базисных векторов
векторы примитивных трансляций некоторой
кристаллической решетки. Объем
элементарной ячейки задается смешанным
произведением тройки базисных векторов
![]() .
(2)
.
(2)
Как обычно, точкой обозначается скалярное произведение, а крестом - векторное. Векторы примитивных трансляций обратной решетки находятся с помощью соотношений:
![]() (3)
(3)
Узлы обратной решетки перечисляются тройкой целых чисел m1,m2,m3:
![]() (4)
(4)
Выберем
некоторый произвольный вектор
![]() ,
т.е. подставим три произвольных целых
числа mi
в формулу (4). Построим плоскость,
перпендикулярную к вектору
,
т.е. подставим три произвольных целых
числа mi
в формулу (4). Построим плоскость,
перпендикулярную к вектору
![]() и проходящую через его середину;
тогда
произвольный вектор
и проходящую через его середину;
тогда
произвольный вектор
![]() ,
проведенный до этой плоскости из точки,
выбранной за начало координат, будет
удовлетворять условию дифракции (1).
Иными словами:
условие дифракции (1) является уравнением
плоскости в пространстве векторов
обратной решетки. Построенная таким
образом плоскость образует часть
границы зоны Бриллюэна. Другие части
зоны получатся, при выборе других
векторов
,
проведенный до этой плоскости из точки,
выбранной за начало координат, будет
удовлетворять условию дифракции (1).
Иными словами:
условие дифракции (1) является уравнением
плоскости в пространстве векторов
обратной решетки. Построенная таким
образом плоскость образует часть
границы зоны Бриллюэна. Другие части
зоны получатся, при выборе других
векторов
![]() из совокупности (4). Будем производить
выбор векторов
из совокупности (4). Будем производить
выбор векторов
![]() по следующим правилам:
1) перечислим
все вектора, задающие ближайших соседей
в обратной решетке;
2)
для каждого из этих векторов построим
выше описанные плоскости
(они
вырезают в окрестности начала координат
некоторый полиэдр);
3) перечислим
вектора, задающие вторых соседей в
обратной решетке
и
построим соответствующие плоскости;
4)
проверим, отсекают ли новые плоскости
части полиэдра, построенного в пункте
2, если да, то уменьшим полиэдр на эти
части. Эту процедуру с рассмотрением
все более удаленных узлов обратной
решетки следует повторять до тех пор
пока сформированный полиэдр не перестанет
изменяться. Эта центральная ячейка
обратной решетки играет особо важную
роль в теории твердого тела и называется
первой зоной Бриллюэна. Первая зона
Бриллюэна является зоной с наименьшим
объемом;
она
полностью ограничена плоскостями,
которые делят пополам перпендикулярные
к ним векторы обратной решетки, проведенные
из начала координат. Построение Бриллюэна
показывает волновые векторы k
всех падающих лучей, которые могут быть
отражены кристаллом посредством
брэгговской дифракции.
по следующим правилам:
1) перечислим
все вектора, задающие ближайших соседей
в обратной решетке;
2)
для каждого из этих векторов построим
выше описанные плоскости
(они
вырезают в окрестности начала координат
некоторый полиэдр);
3) перечислим
вектора, задающие вторых соседей в
обратной решетке
и
построим соответствующие плоскости;
4)
проверим, отсекают ли новые плоскости
части полиэдра, построенного в пункте
2, если да, то уменьшим полиэдр на эти
части. Эту процедуру с рассмотрением
все более удаленных узлов обратной
решетки следует повторять до тех пор
пока сформированный полиэдр не перестанет
изменяться. Эта центральная ячейка
обратной решетки играет особо важную
роль в теории твердого тела и называется
первой зоной Бриллюэна. Первая зона
Бриллюэна является зоной с наименьшим
объемом;
она
полностью ограничена плоскостями,
которые делят пополам перпендикулярные
к ним векторы обратной решетки, проведенные
из начала координат. Построение Бриллюэна
показывает волновые векторы k
всех падающих лучей, которые могут быть
отражены кристаллом посредством
брэгговской дифракции.
Практическая часть
Работа выполняется с применением пакета программ Chem 3d Pro, который подробно описан в работе №1 настоящего сборника. Chem 3d Pro достаточно точно анализирует силы и энергию электростатического взаимодействия с помощью приложения ММ2, и позволяет моделировать системы, состоящие из нескольких сотен ионов. Однако, расчет больших систем требует много времени, особенно на компьютерах невысокой мощности, поэтому при выполнении настоящей работы не рекомендуется вводить более 300 ионов.
При построении модели кристалла следует помнить, что на его поверхности силы не уравновешены, что приводит к поверхностным искажениям. Величину этих искажений можно измерить на модели, а для правильного определения параметров самого кристалла нужно выбирать области, симметрично окруженные ионами со всех сторон. Вводить исследуемые дефекты нужно также во внутренние слои модели.
Для построения модели ионного кристалла, например NaCl, не следует набирать текстом эту формулу, т.к. Chem 3d Pro выведет на дисплей нейтральную молекулу. Текстом нужно набрать символ отдельного иона с указанием заряда: "Na+1"; или "Cl-1". Введя на экран дисплея две-три пары разноименных ионов можно подать команду минимизации энергии в приложении ММ2. Дальнейшее строительство кристалла рационально выполнять прогрессирующим копированием полученного блока. С целью ускорения счета и избежания ошибок старайтесь соединять блоки разноименными зарядами. Для замены какого-либо иона на другой нужно включить команду ввода текста, выделить курсором намеченный ион, в появившейся рамке набрать обозначение нового иона и нажать "Enter". Для создания вакансии выделите ион и нажмите "Delete". Краевую дислокацию можно создать, вырезав из кристалла полоску ионов. Обратите внимание, что для сохранения периодичности кристалла из него нужно вырезать не одну полуплоскость, а две. После каждой операции следует запускать команду минимизации энергии.
Задания
-
Постройте модель трех- или пятислойного кристалла NaCl размером 77 ионов в плоскости [001], что бы в центре находился анион. Измерьте период решетки для первой координационной сферы в центре (а0) и на краю (ак) кристалла, энергию формирования, оцените краевые искажения как = 100% (ак- а0)/а0. Измерьте период решетки для второй координационной сферы.
-
Замените центральный ион, на другой той же группы, например, Cl-1 на Br-1; после минимизации энергии определите смещение соседних ионов для первой и второй координационной сферы и вычислите изменение энергии системы.
-
Удалите центральный ион измерьте деформацию решетки вокруг вакансии для первой и второй координационной сферы и вычислите изменение энергии системы.
-
Постройте модель трех- или пятислойного кристалла NaCl размером 1212 ионов в плоскости [001], проведите минимизацию энергии, запишите значение последней. Вырежьте из кристалла полуплоскость размером 26 ионов и запустите команду минимизации энергии. Для упрощения счета рекомендуется слегка сблизить края разреза вручную. Оцените деформацию решетки вокруг полученной дислокации и вычислите изменение энергии системы.
-
Составьте отчет о выполненной работе. Зарисуйте схематически полученные изображения, укажите найденные параметры, сделайте выводы по каждому пункту задания.