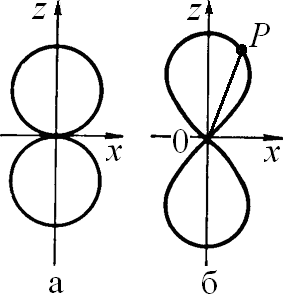Материал: FTTLabRab
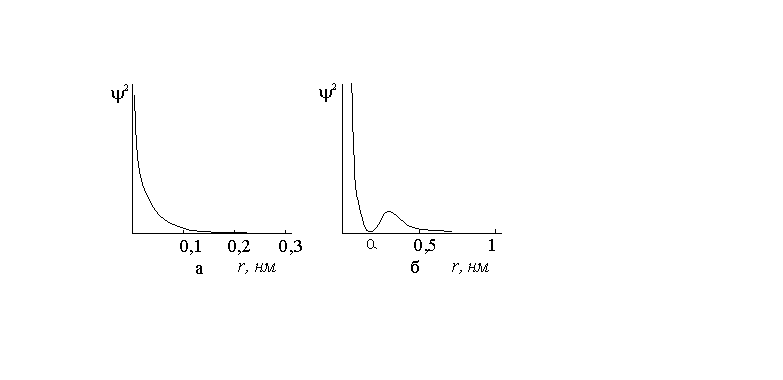
Как указывалось выше, физический смысл волновой функции заключается в том, что квадрат ее значения в какой-либо точке характеризует вероятность нахождения электрона в окрестностях этой точки. На рис. 2 приведен квадрат волновой функции для состояний 1s и 2s. Квадрат волновой функции, так же как и сама эта функция, имеет наибольшее значение в центре атома и монотонно убывает по мере удаления от него. Значения волновой функции наиболее сильно уменьшаются вблизи центра атома, и уже на расстояниях от ядра, превышающих 0,2 нм (2Å), значение квадрата волновой функции настолько мало, что вероятность нахождения электрона вне сферы радиусом 0,2 нм практически равно нулю.
Схематически эту картину можно представить в виде облака вероятностей, которое называют электронным облаком. Его плотность пропорциональна вероятности нахождения электрона в данной точке пространства, т. е. пропорциональна 2. Сечение электронного облака можно представить в виде «фотографии», при получении которой интенсивность освещения в различных точках была пропорциональна плотности электронного облака.
Рис.2. Зависимость квадрата волновой
функции от расстояния для состояний
1s (а) и 2s
(б).
Вероятность нахождения электрона в данной точке сильно убывает с увеличением расстояния от ядра, но не обращается в ноль. Все же большая часть электронного облака сосредоточена вблизи ядра. Поэтому условно размеры электронного облака ограничивают поверхностью, внутри которой сосредоточена определенная (например, 90 или 95 %) доля электронного заряда.
Эту граничную поверхность, приближенно характеризующую форму электронного облака, называют атомной орбиталью. Следует, однако, отметить, что форма электронного облака не совпадает с формой орбитали. Электронное облако – это облако вероятностей, не имеющее четких границ.
Величина 2 характеризует вероятность нахождения электрона в элементе объема на расстоянии r в одном определенном направлении. Чтобы оценить, насколько часто электрон находится на расстоянии r от ядра, надо найти вероятность Р(r) пребывания электрона в шаровом слое между сферами радиусами r и r+dr соответственно. Согласно определению волновой функции эта вероятность будет равна произведению квадрата волновой функции на объем шарового слоя:
![]() ШС, (7)
ШС, (7)
поскольку во всех точках шарового слоя при бесконечно малой его толщине значение квадрата волновой функции будет одно и то же.
Так как объем шарового слоя равен 4r2dr, то
P(r) = 4r22dr = U(r)dr,
где введенная новая функция U(r) определяется как величина, произведение которой на толщину шарового слоя дает вероятность пребывания электрона в шаровом слое на расстоянии r от центра атома.
Для состояния 1s функция U(r) имеет следующий вид:
![]() .
(8)
.
(8)
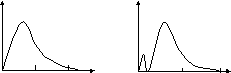
Методами математического анализа можно легко показать, что в точке r=0 функция (8) имеет минимум, а в точке r = а – максимум. График этой функции показан на рис. 3.
U(r)
U(r)
0 1 2 r,
Å 0 5 10 r,
Å
a
б
Рис. 3. Функция U(r)
для состояний 1s (а)
и 2s (б)
Таким образом, согласно волновой теории электрон может находиться, с некоторой вероятностью, в любой точке пространства вокруг ядра. Однако на очень близких расстояниях от ядра электрон бывает сравнительно редко, так же как и на очень больших расстояниях от него. Все же электрон может находиться с достаточно большой вероятностью в довольно большом объеме пространства от r = 0,2Å до r = 1,5Å. Интересно отметить, что величина а, равная 0,529Å, почти точно совпадает с радиусом первой боровской орбиты, равным 0,528Å.Таким образом, понятие орбиты в волновой механике заменяется геометрическим местом точек, отвечающих наибольшей вероятности нахождения электрона в шаровом слое.
Волновая функция для состояния 2s
также является сферически симметричной.
На рис. 2,б показано
изменение квадрата волновой функции с
расстоянием. Квадрат волновой функции
![]() имеет
наибольшее значение в центре атома, при
r=2а проходит
через нуль, а в точке r
= 4а принимает максимальное
значение. При еще большем удалении от
центра ядра волновая функция и ее квадрат
резко уменьшаются по абсолютной величине
и на расстоянии 6 Å от
центра атома практически обращаются в
нуль. Таким образом, вероятность
нахождения электрона в состоянии 2s
максимальна в двух точках: в центре
атома и на расстоянии от него, равном
4а.
имеет
наибольшее значение в центре атома, при
r=2а проходит
через нуль, а в точке r
= 4а принимает максимальное
значение. При еще большем удалении от
центра ядра волновая функция и ее квадрат
резко уменьшаются по абсолютной величине
и на расстоянии 6 Å от
центра атома практически обращаются в
нуль. Таким образом, вероятность
нахождения электрона в состоянии 2s
максимальна в двух точках: в центре
атома и на расстоянии от него, равном
4а.
Для наглядности картину атома водорода
для состояния 2s тоже
представляют в виде электронного облака,
плотность которого в каждой точке
пропорциональна квадрату волновой
функции
![]() .
Размеры электронного облака для
состояния 2s в
5 раз больше размеров электронного
облака для состояния 1s,
а плотность электронного облака для
состояния 2s в каждой
точке примерно в 50 раз
меньше, чем для состояния 1s.
.
Размеры электронного облака для
состояния 2s в
5 раз больше размеров электронного
облака для состояния 1s,
а плотность электронного облака для
состояния 2s в каждой
точке примерно в 50 раз
меньше, чем для состояния 1s.
Вероятность пребывания электрона в шаровом слое на различных расстояниях от центра атома для состояния 2s приведена на рис. 3, б в виде функции U(r). Функция U(r) для состояния 2s имеет два максимума: при r = а и r = 4а. Максимальное значение функции U(r) в точке r = 4а в несколько раз больше максимума в точке r = a, и, следовательно, электрон в состоянии 2s больше всего пребывает на расстоянии 4а от центра атома. Это расстояние соответствует второй боровской орбите. Однако, в отличие от теории Бора, согласно волновой механике электрон с достаточно большой вероятностью может находиться в довольно широкой области пространства, в том числе и на орбите, соответствующей 1s состоянию, хотя вероятность этого сравнительно мала.
Для более высоких s-состояний (3s, 4s и т. д.) наблюдаются следующие общие закономерности.
1. Волновые функции для s-состояний а, следовательно, и квадраты волновых функций и функция U(r) сферически симметричны.
2. Чем больше главное квантовое число п, тем более «размыто» электронное облако, тем на большие расстояния оно распространяется от центра и плотность электронного облака в соответствующих точках становится все меньше.
3. Функция U(r) имеет п максимумов, причем наибольшим по величине будет n-й максимум от центра, т. е. электрон в состоянии ns наибольшее время пребывает в области пространства, которой соответствует n-й максимум функции U(r). Следовательно, чем больше главное квантовое число п, тем на большем расстоянии от ядра чаще всего бывает электрон в этом состоянии. Электрон может быть и в любой другой точке пространства, но вероятность этого мала.
Рассмотрим теперь p-состояния атома водорода. Состояние 2р соответствует следующим значениям квантовых чисел: п = 2 и p = 1. Для этого состояния третье квантовое число принимает три значения: ml = 1; 0; +1, и в соответствии с этим состояние 2р описывается тремя волновыми функциями:
![]() ;
(ml
= 0);
;
(ml
= 0);
![]() ;
(ml
= +1); (9)
;
(ml
= +1); (9)
![]() ;
(ml
= −1).
;
(ml
= −1).
В этом случае волновые функции уже не являются сферическими симметричными и зависят от всех трех координат r, и .
Чтобы наглядно представить распределение электронной плотности в атоме водорода в 2p-состоянии, используют возможность разложения волновой функции на три сомножителя (см. уравнение 2):
![]() .
.
Для описания электрона в каком-либо состоянии рассматривают отдельно квадрат первого члена R2, который называют радиальным вероятностным множителем или радиальной функцией, и отдельно квадрат произведения двух остальных функций, зависящих только от направления и не зависящих от расстояния. Значения второго члена (ΘΦ)2 представляют в виде так называемой полярной диаграммы.
Радиальный вероятностный множитель R2 для всех трех функций ψ2pz, ψ2px и ψ2pg одинаков и равен:
![]() .
.
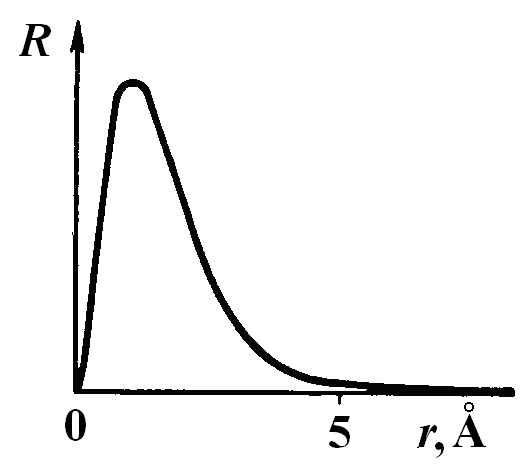
График этой функции приведен на рис. 4. Радиальный множитель электронной плотности для состояния 2р в центре атома равен нулю, с увеличением расстояния от центра атома возрастает, достигает максимума при r=a и далее уменьшается. На расстоянии, превышающем 5Å, радиальный множитель практически равен нулю.
Остальные два множителя ΘΦ для каждого значения третьего квантового числа различны. Для третьего квантового числа ml, равного нулю, произведение этих функций имеет вид:
![]() .
.
График этой функции в полярных координатах
выглядит как две окружности (рис. 5, а).
Функция (ΘΦ)2 отличается от ΘΦ тем,
что она во всех точках положительна и
образована не двумя окружностями, а
двумя лепестками, вытянутыми вдоль оси
z (рис. 5,
б). Так как функция (ΘΦ)2 не
зависит от φ, то для любой другой
плоскости, проходящей через ось
z и составляющей
угол φ с плоскостью z0x,
получим точно такую же кривую. В итоге
полярная диаграмма для состояния 2р
и ml
= 0 будет представлена фигурой,
полученной вращением вокруг оси
z приведенных
на рис. 5,б лепестков.
Полярная диаграмма для состояния 2р
(ml
= 0), вытянута вдоль оси z,
поэтому волновую функцию для этого
состояния обозначают
![]() .
.
|
|
|
|
|
Рис. 4. Радиальный множитель электронной плотности для 2p-состояния |
|
Рис. 5. Зависимость функций θΦ и (θФ)2 от угла θ в плоскости φ = 0 |
Аналогично полярные диаграммы для
состояний m = +1 и –1
представляют собой такие же поверхности,
как и для первого состояния, но
расположенные вдоль осей х и у
соответственно. В
соответствии с этим полярные диаграммы
для m = + 1
и –1 обозначают
![]() и
и
![]() .
Полярные диаграммы для различных
состояний электрона предлагается
построить в данной работе.
.
Полярные диаграммы для различных
состояний электрона предлагается
построить в данной работе.
Ни радиальный множитель, ни полярная диаграмма не определяют полностью вероятность нахождения электрона в окрестностях данной точки. В этом отношении не следует путать полярную диаграмму с электронным облаком.
Аналогично можно представить себе атом водорода для других состояний. Электронные облака для состояний ml = –1 и ml = 0 вытянуты вдоль осей y и z, как и соответствующие им полярные диаграммы. Обычно для простоты p-орбитали представляют в форме вытянутых вдоль осей лепестков.
Электронные облака для более высоких p-состояний (Зр, 4р и т. д.) сходны по общей форме с описанными выше для 2р-состояния. Они также вытянуты вдоль осей х, у и z. Отличие же состоит в следующем. Для 2p-состояния вдоль любой прямой, проходящей через начало координат, плотность облака с удалением от ядра сначала возрастает, достигает максимума, а затем уменьшается. Для более высоких состояний закономерность изменения плотности электронного облака от расстояния до ядра сложнее.
Поскольку для d-состояний возможны пять различных значений третьего квантового числа ml (–2; –1; 0; +1; +2), то они описываются пятью волновыми функциями
![]() ,
,
![]() ,
,
![]() , (10)
, (10)
![]() ,
,
![]() .
.
Полярные диаграммы функций (10) имеют более узкие и более вытянутые лепеспки, чем диаграммы p-состояний. Другая важная особенность полярных диаграмм d-состояния – это наличие четырех направлений в пространстве. Один электрон занимает две пространственные оси. Эта особенность важна для понимания направленности связей, образованных d-электронами.
Работа с программой Orbital Viewer
Orbital Viewer - программа для расчета и визуализации атомных и молекулярных электронных орбиталей. Орбитали могут отображаться в виде точек, каркасной модели и поверхностей. Пользователь может управлять изображением, в том числе, возможно получение изображения в стереорежиме.
При необходимости программа может быть загружена с сайта по адресу http://www.orbitals.com/orb/ Меню программы выглядит следующим образом:
![]()
As you can see there are a number of options. Most buttons on this menu open an additional menu providing further choices. However, it is possible to gain a great deal from the program by using only a few of the buttons.
When the program is started you should click on the leftmost icon (the blank sheet of paper) to open a new file.
Depending on how the particular copy of the program has been set up this action will probably produce a picture of an orbital. You should then click on the button indicated by the arrow in the figure below.
When the secondary menu opens click off the option of using quick rendering, and in the right-hand column select the rendering option that you wish to use (let’s begin with polygons).
You now need to decide which orbital you wish to plot. Click on the button labeled .

The secondary menu includes many options that you need to fill out.
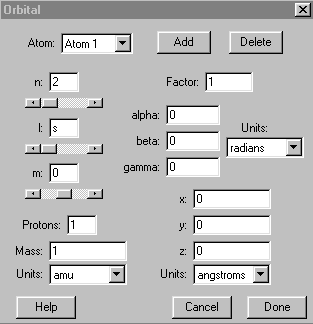
From this menu you can:
select the type of orbital you wish to plot (s, p, d etc.)
select the principle quantum number for the orbital – although it looks as if you could choose to plot something such as a 1f orbital, when you do so the program will plot a 1s orbital and reset the slider for the orbital to s – it does not tell you ahead of time that you have made a bad choice, but does know the rules about n and l
select the ml value – again you may make any correct or incorrect choice, but the program will rest the ml to the maximum allowed value based on your choice of orbital
choose the type of atom (number of protons and mass of the nucleus) – note that this option still uses hydrogen-like radial functions
plot more than one orbital – you do this by adding atoms (top right of menu) – you can use the x, y and z coordinates to position the different atoms on the screen – the plane of the screen is the xy plane – if you place the atoms too close to one another the orbitals overlap and form molecular orbitals – the factor box (contains a 1 by default) is the relative phase of the orbital – leave this at 1 unless you are making molecular orbitals in which case you might use a –1 for one orbital and a 1 for the second to produce an antibonding orbital – you could also use fractional coefficients – the alpha, beta and gamma refer to angular orientation and should be left at 0 for most purposes
The orbital selection menu shown above is set up to draw a 2s orbital at the center of the screen for a hydrogen atom.