Материал: Ekzamen-1
Электрофильный реакции (II) - это реакции, в которых реагентом выступает электрофил (Е +), что имеет положительный заряд и вакантную (свободную) орбиталь или высокое сродство к электрону. Эта свободная орбиталь участвует в об-нии ковалентной химической связи с атомом, с которым они вступают в реакцию. Все электрофильные реагенты условно можно разделить на три группы:1)Катионы:2)Соединения со свободными парами электронов:3)Соединения с полярными связями, в которых на атоме углерода существуют эффективные положительные заряды: нитрилы R-C º N, карбонильные соединения RCX = O и другие.
Электрофильный реакции обозначаются символом Е.
Радикальные реакции (iii) - это реакции, в которых реагентом выступает ради-кал (R ¢), не имеет заряда, но имеет неспаренный электрон на атомной орбита-ли. Этот неспаренный электрон образует ковалентную связь с атомом, с которым он вступает в реакцию. Наиболее распространены радикалы можно расположить в последовательности уменьшения их устойчивости в такой ряд:
Радикальные реакции обозначаются символом R.
3) от характера заместителя R (его длины, наличия сопряженной системы, делокализации электронной плотности).
Основания Бренстеда - нейтральные молекулы или ионы, способные присоединять протон.
При одинаковом структурном окружении для элементов одного периода с ростом электроотрицательности атома при основном центре основность соединений уменьшается: аммониевые основания > оксониевые основания
n основания - могут быть нейтральными или отрицательно заряженными частицами ( аммониевые )
пи основания - в них центром основность являются пи-связи ( алкины, алкены, диены, арены)
15) Влияние различных факторов на кислотные и основные свойства веществ. Примеры.
Все то, что усиливает кислотные свойства, уменьшает основные.
1) Сольватация - это совокупность всех процессов, сопровождающих перенос рассматриваемой частицы из состояния, где она максимально изолирована от взаимодействий с другими частицами (идеальный газ), в раствор.
2) Влияние заместителей - электронно-донорныйе усиливают свойства, электронно-акцепторные - уменьшают.
3) Влияние растворителя
4) Природа гетероатом в основном центре - сила оснований зависит от Э.О. гетероатом ( чем больше Э.О. атома, тем слабее основные свойства)
16) Спирты и фенолы. Многотомные спирты.
Однотомные спирты получают
1) Гидратацией алкенов в кислой среде
2) Гидролизом галогенпроизводных
3) Восстановлением карбонильных соединений
4) Взаимодействием первичных админов с азотистой кислотой.
Однотомные фенолы могут быть получены взаимодействием ароматических сульфокислот с гидроксидами щелочных металлов.
Медико-биологическое значение и применение в народном хозяйстве.
Этиловый спирт в больших количествах вызывает состояние, близкое к наркозу, используется для приготовления настоек и обеззараживающего средства
Метиловый спирт - сильный яд, в пищеварительном тракте образует формальдегид и муравьиную кислоту
ФЕНОЛЫ применят как дезинфицирующие средства.
ФЕНОЛ или карболовая кислота - первый антисептик введенный в хирургию, может вызвать ожог кожи, широко используется для производства пластмасс, лекарственных средств.
Многотомные спирты
Этиленгликоль C2H6O2 - токсичная жидкость
Глицерин C3H8O3 - нетактичная вязкая бесцветная жидкость сладкого вкуса
Получение многотомных спиртов
1. Каталитическая гидратация оксида этилена (получение этиленгликоля):
2. Взаимодействие дигалогенпроизводных алканов с водными растворами щелочей:
3. Из синтез-газа:
2CO + 3H2 250°,200МПа,kat → CH2(OH)-CH2(OH)
17)Химические свойства спиртов
1)Горение:
C2H5OH + 3O2
![]() 2CO2
+3H2O + Q
2CO2
+3H2O + Q
2)Реакции с щелочными и щелочноземельными металлами ("кислотные" свойства):Атомы водорода гидроксильных групп молекул спиртов, также как и атомы водорода в молекулах воды, могут восстанавливаться атомами щелочных и щелочноземельных металлов ("замещаться" на них).
2Na
+ 2H—O—H
2NaOH
+ H2![]()
2Na + 2R—O—H 2RONa + H2
3)Реакции с галогеноводородами:
C2H5OH
+ HBr
![]() C2H5Br
+ H2O
C2H5Br
+ H2O
4)Внутримолекулярная дегидратация (t > 140oС, образуются алкены):
C2H5OH
![]() C2H4
+ H2O
C2H4
+ H2O
5)Межмолекулярная дегидратация (t < 140oС, образуются простые эфиры):
2C2H5OH C2H5OC2H5 + H2O
6)Окисление (мягкое, до альдегидов):
CH3CH2OH
+ CuO
![]() CH3—CHO
+ Cu + H2O
CH3—CHO
+ Cu + H2O
Это качественная реакция на спирты: цвет осадка изменяется с черного на розовый, ощущается своеобразный "фруктовый" запах альдегида).
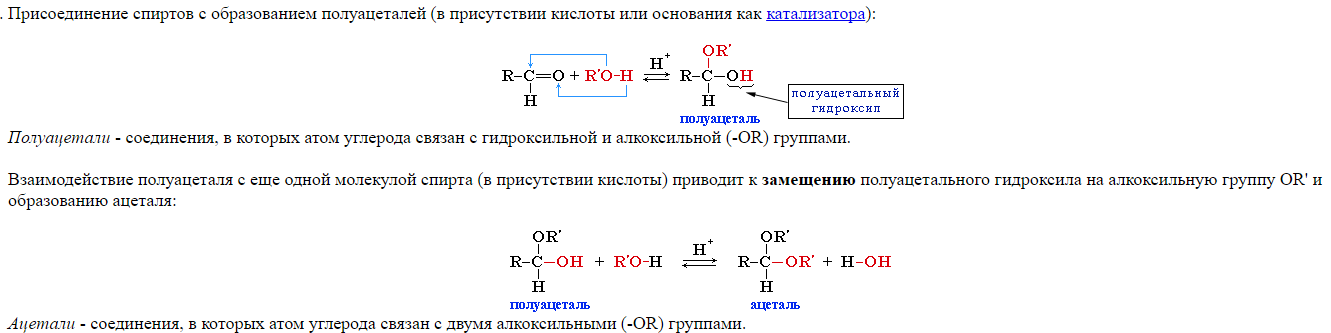
18) Альдегиды, особенности строения карбонильный группы. Химические свойства альдегидов: образование
ацеталей и полуацеталей, реакция диспропорционирования и альдольной конденсации, ОВР, образование оснований Шифра.
Альдегиды и кислородсодержащие органические соединения, содержа-щие карбонильную группу (-С=О).Общая
формула
карбонильных соединений: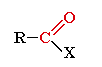
В альдегидах Х = Н (исключением является формальдегид (R = Х = H);
Строение карбонильной группы C=O
Свойства альдегидов определяются строением карбонильной группы >C=O.
Атомы углерода и кислорода в карбонильной группе находятся в состоянии sp2-гибридизации. Углерод своими sp2-гибридными орбиталями образует 3 s-связи (одна из них - связь С–О), которые располагаются в одной плоскости под углом около 120° друг к другу. Одна из трех sp2-орбиталей кислорода участвует в s-связи С–О, две другие содержат неподеленнные электронные пары.
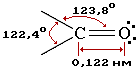
p-Связь образована р-электронами атомов углерода и кислорода.
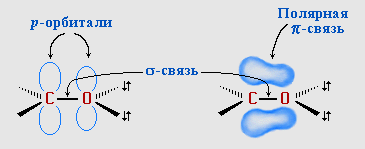
Связь С=О сильно поляризована. Электроны кратной связи С=О, в особенности более подвижные p-электроны, смещены к электроотрицательному атому кислорода, что приводит к появлению на нем частичного отрицательного заряда. Карбонильный углерод приобретает частичный положительный заряд.
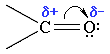
Поэтому углерод подвергается атаке нуклеофильными реагентами, а кислород - электрофильными, в том числе и протонами Н+.
В составе альдегидов имеется оксо-группа. В оксо-группе электронная плотность смещена в сторону более электроотрицательного кислорода и на атоме углерода этой группы возникает положительный заряд.Следовательно для альдегидов характерным является способность вступать в химические реакции, протекающие по механизму нуклеофильного присоединения
Альдегиды
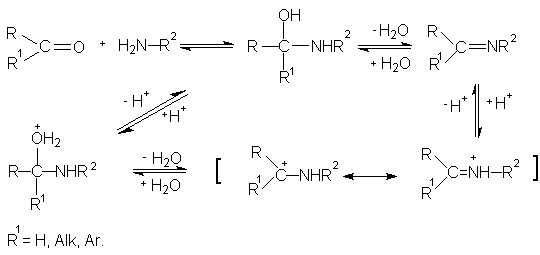
и кетоны реагируют с первичными аминами
с образованием иминов (оснований Шиффа,
азометинов).