Материал: Ekzamen-1
8)Сопряжение – перераспределение (выравнивание) электронной плотности в сопряженной системе, приводящее к стабилизации молекулы.Возможны два типа сопряжения π,π-сопряжение и р,π-сопряжение
-В π,π– сопряженной системе в сопряжении участвует две или более π – связи. π,π– сопряженная система может включать гетероатом (О,N). (При перекрывании четырёх рz-орбиталей происходит образование единого π-электронного облака, т.е.сопряжение двух двойных связей.)Бутадиен – 1,3, пропеналь – это π,π – сопряженная системы.(CH2=CH–CH=CH2CH2=CH–CH=O - бутадиен–1,3 пропеналь)
-В р,π– сопряженной системе π – связь должна быть отделена одной одинарной от р-негибридной орбитали гетероатомом (О,N),где Р-орбиталь гетероатома сопряжена с орбиталями π-связи.(В молекулах этих соединений осуществляется сопряжение двойной связи с р-орбиталью гетероатома.) К таким соединениям относятся галогениды, эфиры, ацетамиды, карбкатионы.
(СН2 = СН – О – СН3 - Винилметиловый эфир)
Сопряжение – энергетически выгодный процесс, поэтому делокализация электронной плотности сопровождается выделением энергии. Система переходит на более низкий энергетический уровень и становится более устойчивой.
Энергия, которая выделяется за счет сопряжения, называется энергией сопряжения (ΔЕ).
Чем длиннее цепь сопряжения, тем больше ΔЕ, тем устойчивее система.
1. Сопряжение. Сопряженные системы с открытой цепью
Сопряженная система представляет собой систему, в которой имеет место чередование простых и кратных связей или по-другому – система, в которой кратные связи находятся друг от друга на расстоянии одной одинарной связи. Такая цепь сопряженных связей называется цепью конъюгации .В сопряженных системах имеет место дополнительное перекрывание π-электронных облаков кратной связи. Двойная связь представляет собой сочетание σ-связи и π-связи. В алкенах электронная плотность π-связи охватывает только 2 атома и ее называют локализованной. Локализованные двойные связи часто встречаются в природных соединениях, например в ненасыщенных карбоновых кислотах.
В сопряженных системах происходит такое электронное взаимодействие, при котором электронная плотность в молекуле распределяется равномерно, т.е. образуется общая электронная плотность.
π,π-сопряжение (Н2С = СН – СН = СН2 Бутадиен-1,3 ) / р,π-сопряжение (Н2С = СН – Cl Хлорэтен)
2. Замкнутые сопряженные системы. Ароматичность.
Сопряженные системы с замкнутой цепью сопряжения – это арены, гетероциклические соединения и небензоидные ароматические структуры.Простейшие замкнутые сопряженные структуры – арены, родоначальник - бензол. (Каждая р-орбиталь в равной степени перекрывается с р-орбиталями соседних атомов. Наблюдается сопряжение, возникает единое замкнутое π – электронное облако, которое охватывает все шесть атомов С.)Такая замкнутая с. система называется ароматической. Бензол Все атомы углерода в бензольном цикле находятся в sр2- гибридизации, все связи С–С равны между собой, имеют длину 1,40 А° и занимают как бы промежуточное положение между простой (1,54 А°) и двойной (1,33 А°) связями, При этом каждый атом углерода образует три s- связи (одну связь С–Н и две s-связи С–С), лежащих в одной плоскости , т.е. у каждого атома углерода осталось по одному р-электрону, орбитали которых, за счет двукратного перекрывания друг с другом образуют замкнутую p-электронную систему, которая охватывает все атомы углерода.p-Электронная плотность в такой системе распределена равномерно. Замкнутый секстет электронов представляет собой связь, которая отличается от других типов, и ее часто называют ароматической.
Электронное строение молекулы бензола можно описать с помощью теории резонанса, согласно которой молекула бензола рассматривается как резонансный гибрид двух предельных (граничных структур).
9)
Ароматичность — особое свойство некоторых химических соединений, благодаря которому сопряженноекольцо ненасыщенных связей проявляет аномально высокую стабильность; большую чем та, которую можнобыло бы ожидать только при одном сопряжении.
К ароматическим системам относятся любые плоские замкнутые циклы, отвечающие критериям ароматичности.
Критерии ароматичности
1. Молекула имеет плоское циклическое строение.
2. Все атомы в цикле в состоянии sp2- гибридизации (следовательно s-скелет плоский и все рz-орбитали параллельны.
3. В молекуле существует делокализованная p-электронная система, содержащая 4n + 2 p-электрона , где n = 0,1,2, – натуральный ряд чисел. Это правило получило название правила Хюккеля, предложено в 1931 на основании метода молекулярных орбиталей).
Правило Хюккеля применимо не только для моноциклических p-электронных систем, но и для плоских конденсированных систем.
Нафталин (4n+2=10 p-эл-нов,n = 2) /Антрацен (4n+2=14 p-эл-нов,n = 3) /Фенантрен(4n+2=14 p-эл-нов,n = 3)
Однако н все замкнутые ароматические структуры являются ароматическими. Так, например, циклооктатетраен-1,3,5,7 не относится к ароматическим, т.к. не удовлетворяется правило Хюккеля, 4n + 2 = 8 p-электронов, n = 1,5.
10)Электронные эффекты - смещение электронной плотности в молекуле, ионе или радикале под влиянием заместителей. Заместителем считается любой атом (кроме водорода) или группа атомов, связанные с атомом углерода. Различают индуктивный (I) и мезомерный (M) эффекты заместителей.
Взаимное влияние, передающееся по цепи σ-связей, называется индуктивным эффектом (I)атома или группы, а передающееся по цепи π-связей -мезомерным эффектом или эффектом сопряжения (M).
Заместители проявляют отрицательный индуктивный эффект (-I), если они смещают к себе электронную плотность σ-связи от атома углерода сильнее, чем водород. Таким свойством обладают группы, содержащие полярные связи, и атомы более электроотрицательные, чем углерод:
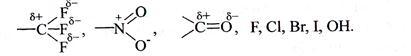
Заместители характеризуются положительным индуктивным эффектом (+I), если они отталкивают электронную плотность σ-связи к углероду. +I проявляют металлы I-III групп периодической системы и алкильные группы:
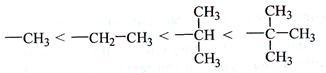
Положительный мезомерный эффект (+М) проявляют атомы азота, кислорода и галогенов, непосредственно связанные с ненасыщенными атомами углерода.
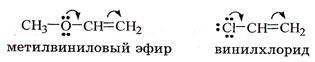
1.Индуктивный эффект — смещение электронной плотности по цепи σ-связей, которое обусловлено различиями в электроотрицательностях атомов.(Наличие в молекуле полярной σ-связи вызывает поляризацию ближайших двух–трех σ-связей и ведет к возникновению частичных зарядов δ+ (дельта плюс) или δ– (дельта минус) на соседних атомах)
Индуктивный эффект передаётся по цепи с затуханием, т. к. при образовании ϭ-связи выделяется большое количество энергии и она плохо поляризуется и поэтому индуктивный эффект проявляется в большей степени на одну две связи. Направление смещения электронной плотности всех ϭ-связей обозначают прямыми стрелками.→
Например: СH3δ+ <→CH2δ+<→CH2δ+<→Clδ-Э.О. Сl> Э.О. С / СH3δ+< →CH2δ+<→CH2δ+<→OHδ- Э.О. ОН > Э.О. С
Атом или группа атомов, смещающие электронную плотность ϭ-связи от атома углерода на себя называются электроноакцепторными заместителями и проявляют отрицательный индуктивный эффект(-I-эффект).
Ими являются галогены (Cl, Br, I), OH-, NH2-, COOH, COH, NO2, SO3H и др.
Атом или группа атомов, отдающие электронную плотность называются электронодонорными заместителями и проявляют положительный индуктивный эффект(+I-эффект).
+I-эффект проявляют алифатические углеводородные радикалы, СН3, С2Н5и др.
Индуктивный эффект проявляется и в случае, когда связанные атомы углерода различны по состоянию гибридизации. Например, в молекуле пропена группа СН3 проявляет +I-эффект, так как атом углерода в ней находится в sp3-гибридном состоянии, а атомы углерода при двойной связи в sp2-гибридном состоянии и проявляют большую электроотрицательность, поэтому проявляют -I-эффект и являются электроноакцепторами.(пропен-1)
2)Мезомерный эффект - смещение электронной плотности по цепи делокализованных (сопряженных) π-связей.
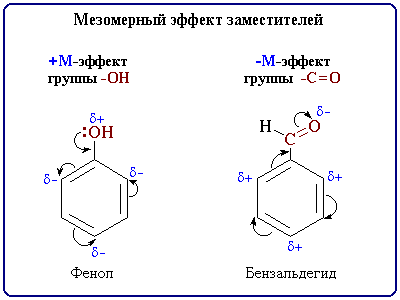
Этот эффект проявляют заместители, связанные с sp2- или sp-гибридизованным атомом. Благодаря подвижности π-электронов, М-эффект передается по цепи сопряжения без затухания. +М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся группы, которые содержат атомы с неподеленной парой электронов, способные к передаче этой пары электронов в общую систему сопряжения. +М-эффект характерен для групп -OH и -NH2. Так, в молекуле фенола C6H5OH группа -OH проявляет +М-эффект за счет участия одной из неподеленных электронных пар атома кислорода в системе сопряжения.
–М-эффект проявляют заместители с электроотрицательными атомами и смещающие электронную плотность на себя. –М-эффект характерен для групп -CH=O, -COOH, -NO2. Хотя эти группы имеют неподеленные электронные пары, пространственное расположение орбиталей с этими электронами не позволяет им вступать в систему сопряжения. Таким образом, в данном случае заместитель может лишь оттягивать электроны из общей системы сопряжения за счет своей более высокой электроотрицательности.
Направление смещения электронной плотности под влиянием М-эффекта обозначается изогнутыми стрелками.
11)Гомолитический разрыв связи — разрыв, когда каждому атому отходит по одному электрону. Характерен для обменного механизма образования ковалентной связи.
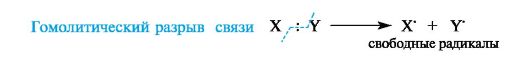
Гетеролитический разрыв связи — разрыв, когда в результате образуются положительно и отрицательно заряженные частицы, т.к. оба электрона из общей электронной пары остаются при одном из атомов. Характерен для донорно-акцепторного механизма образования ковалентной связи.
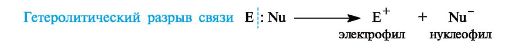
-Процесс, обратный образованию ковалентной связи по обменному механизму, в результате которого образуются два свободных радикала, называется гомолитическим разрывом связи.
-Процесс обратный образованию связи по донорно-акцепторному механизму называется гетеролитическим разрывом сввязи. При этом часто (но не всегда!!!) образуются заряженные частицы ионы.
Частица с неподеленной электронной парой называется нуклеофил, а частица с пустой орбиталью – электрофил.
12) Радикальные реагенты (радикалы) - свободные атомы или частицы с неспаренным электроном. Примеры радикальных реагентов: гидроксильные НОˑ, гидропероксильные HOOˑ, алкильные Rˑ радикалы, атомы галогенов Сˑ, Brˑ. Электрофильные реагенты (электрофилы) - частицы, образующие новую ковалентную связь за счет электронной пары реакционного партнера. Электрофильные частицы обозначаются символом Е+ или Е. Они могут нести положительный заряд - протон Н+, карбокатионы R3C+, ацилий-катионы R-C=O - или быть электронейтральными, например триоксид серы SO3.
Нуклеофильные реагенты (нуклеофилы) - частицы, образующие новую ковалентную связь с реакционным партнером, предоставляя для этого свою электронную пару. Нуклеофильные частицы обозначаются символами Nu или Nu и могут быть отрицательно заряженными - гидрид-ион Н-, гидроксид-ион НО- , алкоксид-ион RO- , карбанион R3C- , хлорид-ион Cl- или быть электронейтральными. В этом случае их нуклеофильность обусловлена р- или π-электронами (NH3, H2O, CH2=CH2, C6H6). -Термин «нуклеофил» применяется к частице, реагирующей с любым электрофильным реакционным партнером за исключением протона Н+.
-Взаимодействующие вещества разделяют на субстраты и реагенты. Такое распределение достаточно условно, но субстратом, как правило, выступает молекулы, которая поставляет атом углерода для образования новой связи. В зависимости от природы реагента (атакующей частицы) все реакции делятся на нуклеофильные, электрофильные и радикальные.
Нуклеофильные (И) - это реакции, в которых реагентом выступает нулкеофил (В-), имеющей отрицательный заряд и хотя бы одну неразделенную электронную пару. Эта пара электронов образует ковалентную связь с атомом, с которым они вступают в реакцию. Условно все нуклеофилы можно разделить на три группы: 1)Анионы:2)Соединения со свободными парами электронов:3)Ненасыщенные соединения с p-электронами: алкены, алкины, диены, арены.
Нуклеофльные реакции обозначаются символом N.
13)Классификация органических реакций по результату: замещения, присоединения, элиминирования, перегруппировки, овр.
РЕАКЦИИ ЗАМЕЩЕНИЯ - одни функциональные группы заменяются на другие.
Примеры:
C2H6 + Cl2 (на свету)→CH3CH2Cl + HCl хлорирование этана
CH3CH2Cl + KOH (водн. р-р) → CH3CH2OH + KCl щелочной гидролиз хлорэтана
реакции присоединения - реакции, в которых одни химические соединения присоединяются к кратным связям другого химического соединения, при этом другие продукты реакции не образуются:А + В→С
Примеры:
CH2=CH-CH3 + Br2 →CH2Br-CHBr-CH3 бромирование пропена
CH2=CH2 + H2O→CH3CH2OH гидратация этилена
К реакциям присоединения относятся также реакции полимеризации - это химический процесс соединения множества исходных мономеров в крупные молекулы полимера.
Например, образование полиэтилена: n CH2=CH2→(-CH2-CH2-) n
Реакции элиминирования - В реакции происходит отрыв атомов или атомных групп от молекулы исходного вещества при сохранении ее углеродного скелета.
Например:
· отщепление воды (при нагревании спирта с серной кислотой)
CH3-CH2OH→CH2=CH2 + H2O дегидратация этанола
· отщепление водорода от алкана (в присутствии катализатора)
CH3-CH3 →CH2=CH2 + H2 дегидрирование этана
Реакции перегруппировки - В органическом соединении происходит переход отдельных атомов или групп атомов от одного участка молекулы к другому без изменения ее качественного и количественного состава:
Например:
Окислительно-восстановительные реакции - реакции, в ходе которых меняется степень окисления атомов, входящих в молекулу.
пример: CH3-CH2-OH + O2 = CH3-C=O + H2O
4 CH3CH2HOH + 5 O2 = 6 H2O + 4 C2H4O2
14) Кислоты и основания по Бренстеду, их классификация.
Кислоты Бренстеда - ( протонные кислоты) - нейтральные молекулы или ионы, способные отдавать протон.
4 типа бренстедовских кислот:
S-H к-ты: тиолы.
O-H к-ты: карбоновые, фенолы, спирты.
N-H к-ты: амид, амины, имиды.
C-H к-ты:углеводороды и их производные.
В этом ряду сверху вниз кислотность уменьшается. Сила кислоты определяется стабильностью образующегося аниона. Чем стабильнее анион, тем сильнее кислота. Стабильность аниона зависит от делока-лизации (распределения) «отрицательного» заряда по всей частице (аниону). Чем больше делокализован «отрицптельный» заряд, тем стабильнее анион и сильнее кислота.
Делокализация заряда зависит:
1) от электроотрицательности (ЭО) гетероатома. Чем больше ЭО гетероатома, тем сильнее соответствующая кислота. Например: R-OH и R-NH2.
Спирты более сильные кислоты, чем амины, т. к. ЭО (0) ? 30(N);
2) от поляризуемости гетероатома. Чем больше поляризуемость гетероатома, тем сильнее соответствующая кислота. Например: R-SH и R-ОН.
Тиолы более сильные кислоты, чем спирты, т. к. атом S более поляризован, чем атом О;