Материал: Ekzamen-1
В настоящее время в органической химии общепринятой является систематическая номенклатура, разработанная Международным союзом чистой и прикладной химии (IUPAC). Наряду с ней сохранились и используются тривиальная и рациональная номенклатуры.
Тривиальная номенклатура состоит из исторически сложившихся названий, которые не отражают состава и строения вещества. Они являются случайными и отражают природный источник вещества (молочная кислота, мочевина, кофеин), характерные свойства (глицерин, гремучая кислота), способ получения (пировиноградная кислота, серный эфир), имя первооткрывателя (кетон Михлера, углеводород Чичибабина), область применения (аскорбиновая кислота). Преимуществом тривиальных названий являетсяих лаконичность, поэтому употребление некоторых из них разрешено правилами IUPAC.
Систематическая номенклатура является научной и отражает состав, химическое и пространственное строение соединения. Название соединения выражается при помощи сложного слова, составные части которого отражают определенные элементы строения молекулы вещества. В основе правил номенклатуры IUPAC лежат принципы заместительной номенклатуры, согласно которой молекулы соединений рассматриваются как производные углеводородов, в которых атомы водорода замещены на другие атомы или группы атомов. При построении названия в молекуле соединения выделяют следующие структурные элементы.
Родоначальная структура – главная цепь углеродная цепь или циклическая структура в карбо- и гетероциклах.
Углеводородный радикал – остаток формульного обозначения углеводорода со свободными валентностями (см. таблицу 2.2).
Характеристическая группа – функциональная группа, связанная с родоначальной структурой или входящая в ее состав (см. таблицу 2.3).
При составлении названия последовательно выполняют следующие правила.
Определяют старшую характеристическую группу и указывают ее обозначение в суффиксе.
Определяют родоначальную структуру по следующим критериям в порядке падения старшинства: а) содержит старшую характеристическую группу; б) содержит максимальное число характеристических групп; в) содержит максимальное число кратных связей; г) имеет максимальную длину. Родоначальную структуру обозначают в корне названия в соответствии с длиной цепи или размером цикла: С1 – “мет”, С2 – “эт”, С3 – “проп”, С4 – “бут”, С5 и далее – корни греческих числительных.
Определяют степень насыщенности и отражают ее в суффиксе: “ан” – нет кратных связей, “ен” – двойная связь, “ин” – тройная связь.
Устанавливают остальные заместители (углеводородные радикалы и младшие характеристические группы) и перечисляют их названия в префиксе в алфавитном порядке.
Устанавливают умножающие префиксы – “ди”, “три”, “тетра”, указывающие число одинаковых структурных элементов (при перечислении заместителей в алфавитном порядке не учитываются).
Проводят нумерацию родоначальной структуры так, чтобы старшая характеристическая группа имела наименьший порядковый номер. Локанты (цифры) ставят перед названием родоначальной структуры, перед префиксами и перед суффиксами.
3) Изомеризация — это специфическая реакция, во время которой наблюдается превращение структурных изомеров друг в друга. В качестве примера можно взять вещества из ряда алканов. Структурные виды изомерии алканов позволяют превращать некоторые вещества в изоалканы. Таким образом, в промышленности повышается октановое число топлива. Стоит упомянуть, что такие свойства имеют огромное значение для развития промышленности.
Структурная изомерия и ее разновидности
Структурная изомерия — это явление, при котором изомеры различаются между собой химическим строением. Здесь выделяют несколько отдельных видов
1. Изомерия углеродного скелета. Такая форма характерна для углеродов и связана с различным порядком связей между атомами углерода.
4) Пространственная изомерия: Конфигурационная и Конформационная.
Конформации:
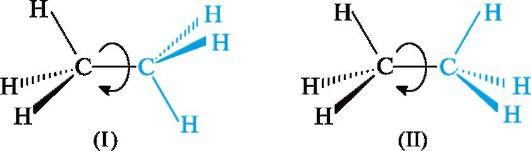
Вокруг простой связи С-С возможно свободное вращение, в результате которого молекула может принимать различные формы в пространстве. Это видно на стереохимических формулах этана (I) и (II), где отмеченные цветом группы СН3 расположены по-разному относительно другой группы СН3.
Поворот одной группы СН3 относительно другой происходит без нарушения конфигурации - изменяется лишь взаимное расположение в пространстве атомов водорода
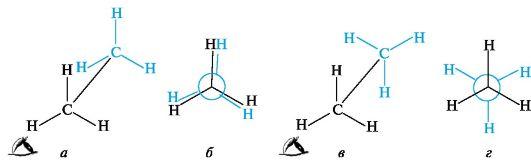
Конформации ациклических соединений
Простейшим соединением со связью С-С является этан; рассмотрим две из множества его конформаций. В одной из них (рис. 7, а) расстояние между атомами водорода двух групп СН3 наименьшее, поэтому находящиеся друг против друга связи С-Н отталкиваются. Это приводит к увеличению энергии молекулы, а, следовательно, к меньшей устойчивости этой конформации. При взгляде вдоль связи С-С видно, что три связи С-Н у каждого атома углерода попарно «заслоняют» друг друга. Такую конформацию называют заслоненной. В другой конформации этана, возникающей при повороте одной из групп СН3 на 60° (см. рис. 7, в), атомы водорода двух метильных групп максимально удалены друг от друга. При этом отталкивание электронов связей С-Н будет минимальным, энергия такой конформации также будет минимальной. Эту более устойчивую конформацию называют заторможенной. Разница в энергии обеих конформаций невелика и составляет ~12 кДж/моль; она определяет так называемый энергетический барьер вращения.
5) Симметрия молекул
Элементы симметрии представляют собой геометрические места, относительно которых осуществляются операции симметрии. При этом различают:
элементы симметрии 1 рода – оси симметрии (оси вращения);
элементы симметрии 2 рода – плоскости симметрии (зеркальные плоскости), центры симметрии (центры инверсии) и оси зеркального отражения.
Под термином операции симметрии понимают геометрические операции, осуществляемые на элементах симметрии и переводящие объект (молекулу) в неотличимую, эквивалентную или идентичную ориентацию.
Различают четыре основных операции симметрии:
вращение на угол 2π/n = 360°/n вокруг оси вращения;
отражение в плоскости симметрии;
инверсия (отражение в точке) в центре симметрии;
вращение с отражением вокруг оси зеркального отражения (вращение на угол 2π/n и отражение в плоскости, перпендикулярной к оси вращения).
Асимметрический атом — атом многовалентного элемента (напр., углерода, азота), к которому присоединены неодинаковые атомные группы или атомы других элементов.
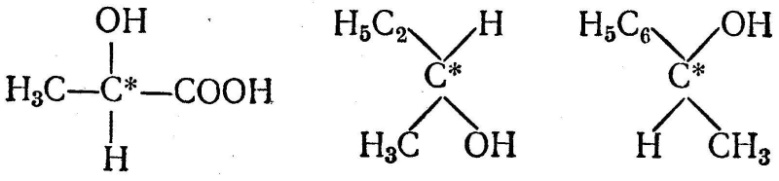 Примеры
ассиметричного атома.
Примеры
ассиметричного атома.
Стереоизомерами называются изомеры, различающиеся только расположением атомов и групп атомов в пространстве. Имеются органические молекулы, не обладающие плоскостью симметрии, и такие молекулы оказывается совместимыми со своим зеркальным изображением -это хиральность. Энантиомеры - ϶ᴛᴏ стереоизомеры, обладающие одинаковыми физическими (кроме знака вращения) и химическими свойствами и относящиеся друг к другу как предмет к своему зеркальному отражению.
6)
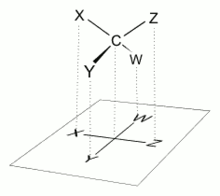
Проекция Фишера (проекционная
формула Фишера, формула
Фишера) —
способ изображения трёхмерной молекулы
в видеопроекции,
в которой вертикальные связи удаляются
за проекционную плоскость, а горизонтальные
связи выступают перед этой плоскостью.
2. Изомерия по положению функциональной группы. Это явление связано с различным положением функциональной группы или групп в молекуле. В качестве примера можно привести 4-хлорбутановую и 2-хлорбутановую кислоту.
3. Изомерия кратных связей. Кстати, сюда можно отнести самые распространенные виды изомерии алкенов. Изомеры различаются между собой положением ненасыщенной связи.
4. Изомерия функциональной группы. В этом случае общий состав вещества сохраняется, но свойства и характер самой функциональной группы изменяются. В качестве примера можно привести диметиловый эфир и этанол.
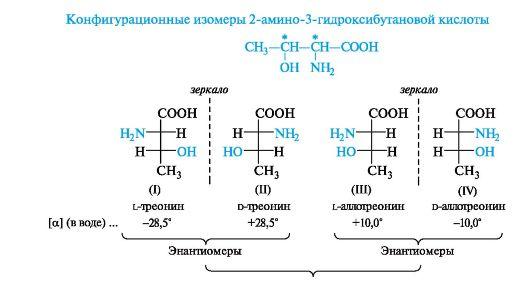
Структуры (I) и (II), соответствующие L- и D-треонину, а также (III) и (IV), соответствующие L- и D-аллотреонину (от греч. alios - другой), относятся друг к другу, как предмет и несовместимое с ним зеркальное отражение, т. е. они представляют собой пары энантиомеров. При сопоставлении структур (I) и (III), (I) и (IV), (II) и (III), (II) и (IV) видно, что в этих парах соединений у одного асимметрического центра конфигурация одинаковая, а у другого - противоположная. Такие пары стереоизомеров представляют собой диастереомеры. Подобные изомеры называют σ-диастереомерами, так как заместители в них связаны с центром хиральности σ-связями.
Аминокислоты и гидроксикислоты с двумя центрами хиральности относят к D- или L-ряду по конфигурации асимметрического атома с наименьшим номером.
Диастереомеры, в отличие от энантиомеров, различаются физическими и химическими свойствами. Например L-треонин, входящий в состав белков, и L-аллотреонин имеют разные значения удельного вращения (как показано выше).
σ-Диастереомеры. Многие биологически важные вещества содержат в молекуле более одного центра хиральности. При этом возрастает число конфигурационных изомеров, которое определяется как 2n, где n - число центров хиральности. Например, при наличии двух асимметрических атомов соединение может существовать в виде четырех стереоизомеров (22 = 4), составляющих две пары энантиомеров.
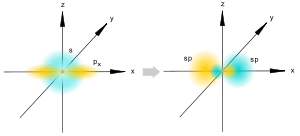
7) sp-Гибридизация.
sp-гибридизация
Происходит при смешивании одной s- и одной p-орбиталей. Образуются две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра центрального атома. Две оставшиеся негибридные p-орбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются не поделёнными парами электронов.
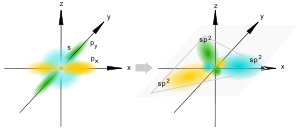
sp2-Гибридизация.
sp2-гибридизация
Происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей
 .
.
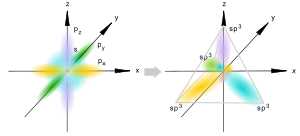
sp3-Гибридизация
sp3-гибридизация
Происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp3-гибридные орбитали. Могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.
Оси sp3-гибридных орбиталей направлены к вершинам тетраэдра, тогда как ядро центрального атома расположено в центре описанной сферы этого тетраэдра. Угол между любыми двумя осями приближённо равен 109°28'[3], что соответствует наименьшей энергии отталкивания электронов. Также sp3-орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов. Такое состояние характерно для атомов
углерода
в насыщенных углеводородах и соответственно
в алкильных радикалах .
разовании химических связей (отсутствуют неподелённые электронные пары)[4].
Основные характеристики:
Тип гибридизации |
Число гибридных орбиталей |
Геометрия |
Структура |
Примеры |
sp |
2 |
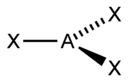
Линейная |
|
BeF2, CO2, NO2+ |
sp2 |
3 |
Треугольная |
|
BF3, NO3-, CO32- |
sp3 |
4 |
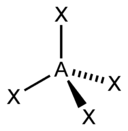
Тетраэдрическая |
|
CH4, ClO4-, SO42-, NH4+ |
dsp2 |
4 |
Плоскоквадратная |
|
[Ni(CN)4,](2-) [PdCl4]2- |
sp3d |
5 |
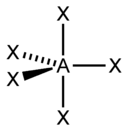
Гексаэдрическая |
|
PCl5, AsF5 |
sp3d2, d2sp3 |
6 |
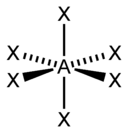
Октаэдрическая |
|
SF6, Fe(CN)63-, |