Материал: Ekzamen-1
[Ni(CO)4] – тетракарбонилникель
[Pt(NH3)2Cl2] – дихлородиамминплатина (II)
Комплексное соединение [Pt(NH3)2Cl2] внешней сферы не имеет и заряд комплекса равен 0.
2. По принадлежности комплексного соединения к определенному классу соединений:

Есть и вещества, не диссоциирующие на ионы, т.е. неэлектролиты
3. По природе лиганда:
- аквакомплексы (лигандом выступает вода: [Co(H2O)6]Cl2, [Al(H2O)6]Cl3 и др.),
- аммиакаты (лигандом выступает аммиак, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4 и др.),
- ацидокомплексы (анионы - кислоты). К ним относятся комплексные соли: K2[PtCl4], комплексные кислоты: H2[CoCl4], H2[SiF6].
- гидроксокомплексы (ОН), например: Na2[Zn(OH)4], Na2[Sn(OH)6] и др.
- карбонилы - комплексные соединения, в которых лигандами являются молекулы оксида углерода (II): [Fe(CO)5], [Ni(CO)4].
- комплексы с макроциклическими лигандами, внутри которых размещается центральный атом (хлорофилл, гемоглобин, цианокобаламин).
4. По внутренней структуре комплекса:
- моноядерные – если комплекс содержит только один атом металла --комплексообразователя (пример, PdCl4 – имеет один атом палладия);
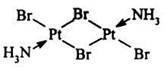
- многоядерные или полиядерные – если он содержит два или более атомов металла (комплекс платины [Pt2(NH3)2Cl4] – содержащий два атома платины.
Если полиядерные комплексы содержат атомы металла одинаковой химической природы, то они называются гомометаллическими: |
|
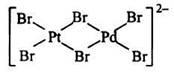
Если же в полиядерном комплексе имеются атомы металла-комплексообразователя разной химической природы, то такие комплексы называются гетерометаллическими. Так, из двух биядерных комплексов: |
|
Для комплексных соединений, содержащих во внутренней сфере различные лиганды, характерна геометрическая изомерия, когда при одинаковом составе внутренней сферы лиганды в ней располагаются по-разному относительно друг друга.
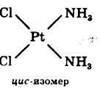
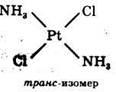
Геометрические изомеры комплексных соединений отличаются не только по физическим и химическим свойствам, но и биологической активностью. Цис-изомер Pt(NH3)2Cl2 имеет ярко выраженную противоопухолевую активность, а транс-изомер – нет.
Номенклатура комплексных соединений.
Название комплексных солей образуют по общему правилу: сначала называют анион, а затем – катион в родительном падеже
Названия комплексных соединений образуются аналогично названиям обычных солей с той лишь разницей, что указываются лиганды и степень окисления центрального атома. К названиям лигандов-анионов добавляют суффикс -о (сульфато-, хлоро-, бромо-, циано-, и т.д.). Наиболее важные лиганды-молекулы: Н2О - аква, NН3 - аммин, СО - карбонил.
Число монодентатных лигандов указывают греческими числительными: 1 - моно (часто не приводится), 2 - ди, 3 - три, 4 - тетра, 5 - пента, 6 - гекса. Для полидентатных лигандов (например, этилендиамин, оксалат) используют бис-, трис-, тетракис- и т.д.
Затем называют комплексообразователь, используя корень его латинского названия и окончание -ат (примеры: цинкат, хромат, феррат), после чего римскими цифрами указывают (в скобках) степень окисления комплексообразователя.
После обозначения состава внутренней сферы называют внешнюю сферу.
В названии нейтральных комплексных частиц комплексообразователь указывается в именительном падеже, а степень его не указывается, так как она однозначно определяется, исходя из электронейтральности комплекса.
Если присутствуют несколько лигандов, они перечисляются в алфавитном порядке и префиксы не изменяют этот порядок, например [CrCl2(H2O)4]+- тетрааквадихлорохром (III)-ион (хотя рекомендуют сначала указывать название отрицательно заряженных лигандов, а затем названия нейтральных молекул).
Примеры:
K3[Fe(CN)6] – гексацианоферрат (III) калия
(NH4)2[PtCl4(OH)2] – дигидроксотетрахлороплатинат (IV) аммония
[Сr(H2O)3F3] - трифторотриаквахром
[Сo(NH3)3Cl(NO2)2] - динитритохлоротриамминкобальт
[Pt(NH3)4Cl2]Cl2 - хлорид дихлоротетраамминплатины (IV)
[Li(H2O)4]NO3 - нитрат тетрааквалития
20. Понятие о хелатных соединениях. Хелатообразующие лиганды, примеры
Хелатные соединения - комплексные соединения, в которых лигандприсоединен к центральному атому металла посредством двух или большего числа связей. Характернаяособенность хелатных соединений - наличие циклических группировок атомов, включающих атом металла, как, напр., в гемоглобине, хлорофилле. Хелатные соединения используют в химической промышленности, напр. для разделения близких по свойствам металлов, в аналитической химии.
Органические хелатообразующие лиганды широко используются в аналитической практике как осадители ионов металлов. Растворимость хелатных комплексов этого типа зависит прежде всего от свойств лигандов, заряда, устойчивости и структуры образующегося комплекса. Предполагается, что в определении стереохимии значительная роль принадлежит лиганду, являющемуся партнером в образовании координационной связи. Координационное число иона металла по отношению к монодентатным лигандам определяется главным образомразмером лиганда и числом потенциальных донорных атомов. Детальная стереохимия для данного координационного числа в большинстве случаев зависит от требований иона металла (эффекты кристаллического поля) и в изменяющейся степени от стереохимии лиганда, хелатообразующих свойств и природы донорных атомов, принимающих участие в образовании связи. Группу атомов (молекулу или ион), которая может связываться с одним и тем же ионом металла несколькими из своих атомов, называют хелатообразующей или полидентатным лигандом. Известны хелатообразующие агенты, координирующиеся двумя, тремя, четырьмя, пятью, шестью и даже восемью донорными атомами чаще всего встречаются агенты с двумя донорными атомами. Такие полидентатные лиганды называют соответственно би-, три-, тетра-, пента- и гексадентатными.
21. Представление о строении гемопротеидов
ГЕМОПРОТЕИДЫ — сложные окрашенные белки, содержащие в качестве небелкового компонента гем. К гемопротеидам относятся гемоглобин, миоглобин, некоторые окислительные ферменты
Гемопротеиды, сложные белки, содержащие окрашенную простетическую группу - гем. Относятся к хромопротеидам. Кроме дыхательных пигментов - гемоглобина и миоглобина, Г. включают широко распространённые дыхательные ферменты - цитохромы, и окислительные ферменты тканей - пероксидазу, катализирующую окисление органических веществ перекисью водорода, катализу и леггемоглобин (легоглобин) - пигмент, обнаруженный в корневых клубеньках бобовых растений.
22. Сорбция. Понятия адсорбции и абсорбции. Физическая и химическая адсорбция. Зависимость величины адсорбции от различных факторов
Благодаря поверхностному натяжению жидкость при отсутствии внешних силовых воздействий принимает форму шара, отвечающую минимальной величине поверхности и, следовательно, наименьшему значению свободной поверхностной энергии. Одним из путей понижения свободной поверхностной энергии является сорбция.
Сорбция (от лат. sorbeo – поглощаю) − поглощение твёрдым телом или жидкостью вещества из окружающей среды. Поглощающее тело называется сорбентом, поглощаемое им вещество − сорбатом (или сорбтивом). Различают поглощение вещества всей массой жидкого сорбента – это абсорбция; поверхностным слоем твёрдого или жидкого сорбента − это адсорбция.
Абсорбция − поглощение веществ из газовой смеси жидкостями. В технике абсорбция обычно пользуется для извлечения из газовой смеси какого-либо компонента. Абсорбция улучшается с повышением давления и понижением температуры.
Адсорбция − процесс концентрирования вещества из объема фаз на границе их раздела.
Адсорбент – вещество, способное адсорбировать другое вещество. Адсорбтив – вещество, которое может адсорбироваться. Адсорбат – адсорбированное вещество.
Процесс адсорбции является избирательным и обратимым. Адсорбция из растворов на твердом теле (имеющая поверхность раздела) бывает двух видов:
Молекулярная – адсорбция из растворов молекул слабых электролитов.
Ионная – это адсорбция из растворов ионов.
Десорбция − удаление адсорбированного вещества с поверхности адсорбента. Десорбция обратна адсорбции и происходит при уменьшении концентрации адсорбируемого вещества в среде, окружающей адсорбент.
Различают два вида адсорбции – физическая и химическая адсорбция. Физическая адсорбция вызвана Ван – дер – ваальсовыми силами взаимодействия между молекулами адсорбата и адсорбента. Эти силы невелики и поэтому теплота физической адсорбции составляет ~ 10 – 30 кДж/моль. Химическая адсорбция, или хемосорбция, обязана химической связи, возникающей между адсорбатом и адсорбентом. При этом образуются поверхностные соединения. Теплота хемосорбции составляет ~ 100 – 400 кДж/моль, а сам процесс хемосорбции носит активационный характер. Молекулы адсорбата и адсорбента должны обладать энергией, которая превышает некоторое пороговое значение (энергия активации). Энергетические характеристики этих двух видов адсорбции и обуславливают их основные отличия