Материал: 2793
7
Нумерацию атомов углерода начинают с карбоксильной группы. Названия кетокислот образуют подобным образом. Обозначать следует только те атомы углеродной цепи, у которых находятся оксиили кетогруппы, т.е. только в радикале кислоты.
CH3–C–COOH |
2-оксопропановая кислота |
|
|| |
|
|
O |
|
|
HOOC – CH – CH – COOH |
||
| |
| |
2,3 – диоксибутандиовая кислота |
OH |
OH |
|
|
|
O |
5 4 3 |
2 |
1 ⁄⁄ |
CH3–CH–CH2–C–C–OH 4-метил-2-оксопентановая кислота
| ||
CH3 O
СH3– C – COOH
||
О2-оксопропановая кислота
Для некоторых соединений со смешанными функциями часто используется тривиальная номенклатура.
HO – CH2 – COOH |
гликолевая кислота (Т) |
|
CH3 – CH – COOH |
молочная кислота (Т) |
|
| |
|
|
OH |
|
|
CH – COOH |
|
глиоксалевая кислота (Т) |
|| |
|
|
O |
|
|
HOOC–CH2–CH–COOH |
яблочная кислота (Т) |
|
|
| |
|
|
OH |
|
HOOC – CH – CH – COOH |
винная кислота (Т) |
|
| |
| |
|
OH |
OH |
|
|
8 |
HOCH2 – CH – CH=O |
глицериновый альдегид (Т) |
| |
|
OH |
|
СH3 – C – COOH |
пировиноградная кислота (Т) |
|| |
|
O |
|
Относительная и абсолютная конфигурация и номенклатура оптических изомеров
Для соединений с асимметрическим атомов углерода (имеющим 4 разных заместителя) характерна оптическая изомерия. Оптические изомеры могут иметь относительную и абсолютную конфигурацию. Относительная конфигурация определяет принадлежность к D или L генетическому ряду.
При написании формул оптических изомеров функциональные группы располагаются следующим образом: вверху помещают главную функциональную группу, атомы углерода записывают сверху вниз, а слева и справа от атома углерода располагают другие группы. По положению старшего заместителя у асимметрического атома углерода, наиболее удаленного от главной функциональной группы определяют D или L конфигурацию. Если
старший заместитель находится справа, то это D |
изомер, если слева – то L. |
|
За эталон был принят глицериновый альдегид. Ниже приведены D или |
||
L конфигурация глицеринового альдегида: |
|
|
O |
|
O |
// |
|
// |
C |
C |
|
| H |
| |
H |
H –C – OH |
HO–C– H |
|
| |
| |
|
CH2OH |
CH2OH |
|
D – глицериновый альдегид |
L – глицериновый альдегид |
|
Если у последнего асимметрического атома углерода от главной функ- |
||
циональной группы расположение заместителей соответствует D- |
||
глицериновому альдегиду, то оптический изомер |
относят к D-ряду. Если |
|
соответствует L-глицериновому альдегиду, то относят к L-ряду, например: |
||
COOH |
COOH |
|
| |
| |
|
H– C – Br |
H– C – Br |
|
| |
| |
|
H– C – OH |
HO – C – H |
|
| |
| |
|
COOH |
COOH |
|
D – бромяблочная кислота |
L –бромяблочная кислота |
|
9
Углеводы. Моносахариды
Простые углеводы, не подвергающиеся гидролизу, иначе называются моносахаридами или монозами, а также гликозами. Для моносахаридов характерно общее окончание – ОЗА. В зависимости от количества атомов углерода моносахариды делятся на триозы (С3Н5О3), тетрозы (С4Н6О4), пентозы (С5Н10О5), гексозы (С5Н12О5) и т.д. Моносахариды представляют собой многоатомные оксиальдегиды (альдегидоспирты) или оксикетоны (кетоноспирты). Моносахариды, содержащиеся в оксикарбонильной форме альдегидную или кетонную группу, называют соответственно альдозами или кетозами. В зависимости от числа углеродных атомов различают альдогексозы, кетогексозы, альдопентозы и т.д. Например:
⁄⁄ |
O |
CH2–OH |
CH2OH |
|
| |
| |
|
C |
C=О |
C=O |
|
|
H |
| |
| |
H–C–OH |
H– C –OH |
H–C–OH |
|
| |
|
| |
| |
H–C–OH |
H– C –OH |
H–C–OH |
|
| |
|
| |
| |
CH2OH |
CH2OH |
H–C–OH |
|
|
|
|
| |
|
|
|
CH2OH |
альдотетроза |
кетопентоза |
кетогексоза |
|
Пространственное строение моносахаридов выражают проекционными формулами (формулы Фишера). Наиболее распространенные моносахариды – гексозы:
O |
O |
O |
CH2OH |
// |
// |
// |
| |
С |
C |
C |
C=O |
| H |
| H |
| H |
| |
H–C–OH |
HO–C–H |
H–C–OH |
HO–C–H |
| |
| |
| |
| |
HO–C–H |
HO–C–H |
HO–C–H |
H–C–OH |
| |
| |
| |
| |
H–C–OH |
H–C–OH |
HO–C–H |
H–C–OH |
| |
| |
| |
| |
H–C–OH |
H–C–OH |
H–C–OH |
CH2OH |
| |
| |
| |
|
CH2OH |
CH2OH |
CH2OH |
|
D-глюкоза |
D-манноза |
D-галактоза |
D-фруктоза |
|
|
10 |
|
|
|
Пентозы: |
|
H |
O |
O |
O |
\ |
// |
// |
// |
C |
|
C |
C |
| |
|
| H |
| H |
H–C–OH |
HO–C–H |
H–C–OH |
|
| |
|
| |
| |
HO–C–H |
H–C–OH |
H–C–OH |
|
| |
|
| |
| |
H–C–OH |
H–C–OH |
H–C–OH |
|
| |
|
| |
| |
CH2OH |
CH2OH |
CH2OH |
|
D- ксилоза |
D- арабиноза |
D-рибоза |
|
Приведены тривиальные названия моноз. Кроме открытой (оксикарбонильной) формы моносахариды могут существовать в виде циклических полуацетальных форм.
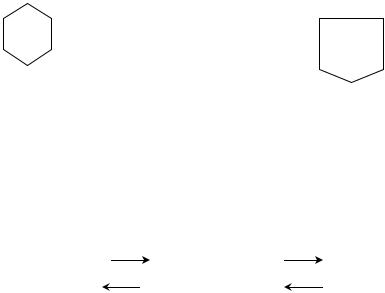
Образование полуацетальной формы в альдозах происходит при взаимодействии альдегидной группы со спиртной группой 5-го или 4-го атома углерода. При этом образуется кислотосодержащие кольцо (цикл), а кислород карбонильной группы образует гидроксил (полуацетальный, гликозидный). Шестичленное кольцо с кислородом носит название пираноза. Пятичленное
– фураноза. Эти названия происходят от названий соответствующих гетероциклических соединений.
|
|
СН2 |
|
|
|
|
|
|
|
|
|
|
|||||||
HC |
|
|
|
|
СH |
|
HC |
|
|
|
CH |
||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|||||||||||||||||
НС |
|
|
|
|
СН пиран |
|
|
|
|
|
|
|
фуран |
||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
О |
|
HC |
|
|
|
CH |
||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||
ОН |
Н |
⁄⁄ |
О |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
С–––––– |
|
|
C |
|
|
|
|
CH2OH |
|||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| Н |
| |
|
|
|
|
|||||
Н–C–ОН |
|
|
Н–C–OН |
|
НО–C |
|
|
|
|||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
HO–C–H |
|
|
HO–C–H |
|
HO–C–H |
|
|||||||||||||
|
|
||||||||||||||||||
| |
|
|
|
О |
| |
|
| |
|
|
|
|
||||||||
|
|
|
|
||||||||||||||||
H–C–OH |
|
|
H–C–OH |
|
H–C–OH О |
||||||||||||||
|
|
||||||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H–C–––––– |
|
|
H–C–OH |
|
H–C |
|
|
||||||||||||
|
|
|
|
|
|||||||||||||||
| |
|
|
|
|
|
|
|
|
| |
|
| |
|
|
|
|
||||
CH2ОН |
CH2OH |
|
|
|
CH2OH |
||||||||||||||
полуацетальная |
альдогексоза |
полуацетальная форма |
форма альдозы |
оксикарбонильная |
альдозы (фураноза) |
(пираноза) |
(альдоза) |
|
11
Полуацетальные формы кетоз также имеют либо шестичленное, либо пятичленное кислородосодержащие кольцо. Шестичленное кольцо (пираноза) образуется в результате взаимодействия кетонной группы при втором атоме углерода со спиртовой группой при шестом атоме углерода, а пятичленное (фураноза) – за счет взаимодействия со спиртовой группой 5-го углерода:
|
|
CH2OH |
|
CH2OH |
|
CH2OH |
||||||||||
HO |
|
|
|
|
|
|
|
|
С==O |
HO |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||||
HO |
|
|
|
H |
|
HO |
|
|
|
Н |
Н |
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
Н |
|
|
|
OH О |
Н |
|
|
|
OH |
H |
|
|
OH |
|
||
|
|
|
|
|
|
|
|
|||||||||
Н |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
Н |
|
|
|
OH |
H |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
CH2OH |
|
CH2OH |
||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
||||||||||||
полуацетальная |
кетоза |
|
полуацетальная |
|||||||||||||
(пиранозная) |
фруктоза |
|
(фуранозная) |
|||||||||||||
форма кетозы |
оксикарбонильная форма |
|
форма кетозы |
|||||||||||||
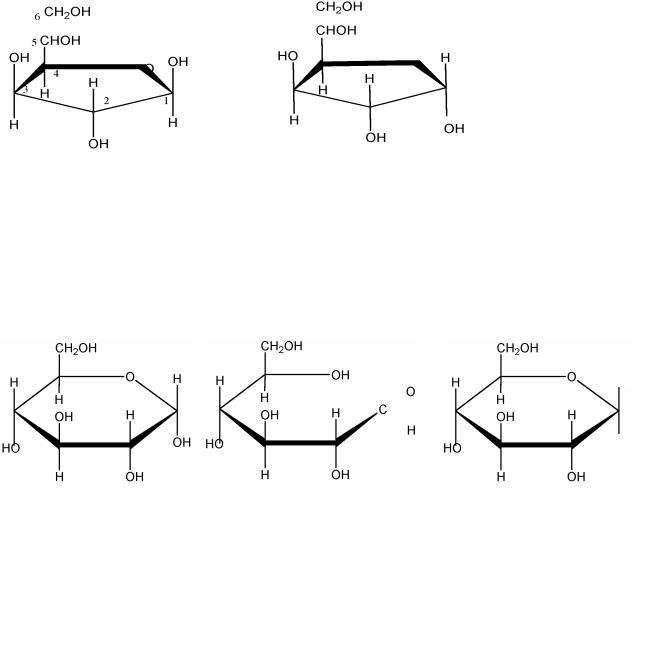
По предложению английского химика Хеуорса, полуацетальные формы моносахаридов изображают в виде перспективных форм. Углеродные атомы в этих формулах нумеруют так же, как и в оксикарбонильных. Атомы и группы при асимметричных углеродах, которые у Фишера пишут слева, в перспективных формулах ориентированы вверх от плоскости кольца, а группы, расположенные справа, в перспективных формулах направлены вниз.
ОН
Н
α-D глюкопираноза |
D-глюкоза (оксикарбонильная форма) |
β-D глюкопираноза |
О |
|
О |
|
|
|
β-D –глюкофураноза |
α-D -глюкофураноза |