Материал: 2002
16
Спиртовая группа содержится в спиртах, карбонильная - в альдегидах и кетонах, карбоксильная - в карбоновых кислотах.
3.1АААААА. АААААА. ААААААА ААААА
Взависимости от количества гидроксильных групп спирты разделяются на одноатомные, двухатомные, трехатомные и т.д. Особо важное значение имеют одноатомные спирты и некоторые двух- и трехатомные.
Наиболее употребительная номенклатура спиртов – рациональная и международная.
По тривиальной номенклатуре названия спиртов образуются от названий соответствующих радикалов:
CH3OH |
CH3–CH2–OH |
метиловый спирт |
этиловый спирт |
По международной номенклатуре названия спиртов производятся от названий углеводородов с присоединением окончания "ол", в конце ставится цифра, обозначающая номер атома углерода, при котором стоит гидроксильная группа.
|
CH3 |
CH3–CH2–CH2–OH |
| |
пропанол-1 |
CH3–C–CH3 |
|
| |
|
OH |
|
2-метилпропанол-2 |
Надо обратить особое внимание на умение правильно называть спирты по международной номенклатуре. Следует учесть, что для фенолов, ароматических спиртов, альдегидов и кислот очень употребительны тривиальные названия, но применяется и международная номенклатура.
Для спиртов характерна изомерия углеводородного скелета и изомерия положения гидроксила (спирты первичные, вторичные, третичные).
При рассмотрении физических свойств, следует обратить внимание на аномалии в температурах кипения спиртов, зависящие от их ассоциации, вызванной водородными связями. В связи с этим необходимо усвоить понятие "водородная связь".
Спирты отличаются амфотерными свойствами, т.е. они взаимодействуют с сильными кислотами и щелочными металлами.
Обратите особое внимание на реакции образования и свойства сложных и простых эфиров как веществ, имеющих широкое применение. Учесть, что для спиртов важными являются реакции окисления. Они протекают различно для первичных, вторичных и третичных спиртов и используются для
17
их идентификации (установления строения). Следует внимательно рассмотреть свойства, основные способы получения и применения метилового, этилового, пропиловых и высших жирных спиртов. Необходимо также знать свойства и применение аллилового спирта, этиленгликоля и глицерина.
Ароматические соединения с гидроксилом, стоящим у бензольного кольца, называются фенолами, у нафталинового кольца - нафтолами.Они вступают во все реакции, характерные для спиртов. Кроме того, эти вещества отличаются значительно более кислыми свойствами по сравнению с алифатическими спиртами. Так, например, они реагируют со щелочами, давая феноляты. Необходимо также учесть способность водородов ароматических колец фенолов и нафтолов вступать в реакции электрофильного замещения (галогенирования, нитрования, сульфирования и др.). При этом гидроксил действует как ориентант первого рода.
Следует обратить особое внимание на простые эфиры и эпоксиды, являющиеся мономерами для получения важного класса полимеров - эпоксидных смол, из которых получают клей превосходного качества, каучук и другие ценные продукты.
Контрольные вопросы к теме "Спирты. Фенолы. Простые эфиры"
71. В чем различия в структуре и свойствах первичных, вторичных, третичных спиртов? Напишите формулы спиртов: бутанол-1, пентанол-2, 2-метилпентанол-2 и реакции их окисления. Назовите полученные соединения.
72.Напишите основные химические реакции, в которые вступают спирты на примере изопропилового спирта.
73.Напишите изомерные спирты состава C4H10O и назовите их. Какие из этих спиртов окисляются до альдегидов?
74.Какие спирты получаются при гидратации следующих углеводородов: 2-метилпентен-2, изобутилен; бутен-1? Что такое простые эфиры?
75.Напишите структурные формулы изомерных простых эфиров C5H12O. Назовите спирты, из которых получаются эти эфиры; напишите реакции их получения.
76.Что такое реакция этерификации? Напишите уравнение реакции получения изопропилпропионата.
77.Напишите уравнения реакций, в которых может вступать этиленгликоль.
78.Химические свойства трехатомных спиртов.
79.В чем различие фенолов и спиртов? Напишите реакции фенольного гидроксила на примере одного из изомерных метилфенолов.
80.Напишите реакции замещения в ароматическом ядре фенола. Каковы правила замещения в ароматическом ядре?
18
3.2 ААААААААА А АААААА
Общеупотребительные названия альдегидов происходят от названия предельных кислот, в которые они превращаются при окислении. Для составления названия по международной номенклатуре к названию углеводорода с тем же числом углеродных атомов прибавляется окончание "аль" или "ал":
H–C=O |
CH3–C=O |
| |
| |
H |
H |
метаналь |
этаналь |
Названия кетонов по рациональной номенклатуре производят от названий радикалов, входящих в их молекулу, с добавлением окончания "кетон":
CH3–C=O |
CH 3–C=O |
| |
| |
CH3 |
C2H5 |
диметилкетон |
метилэтилкетон |
ацетон |
|
По международной номенклатуре названия кетонов производят, прибавляя к названию соответствующего углеводорода окончание "он".
Двойная связь углерод-кислород вследствие большой разницы в электроотрицательности и наличия подвижной π-связи сильно поляризована. Карбонил, в свою очередь, сильно влияет на соседние углеводородные радикалы, особенно на метильные и метиленовые.
Следует учесть, что взаимное влияние остальных групп в карбонильных соединениях делает их очень подвижными, способными к реакциям присоединения, замещения, конденсации, полимеризации. Обратите внимание на различия в реакционноспособности альдегидов и кетонов.
Контрольные вопросы к теме "Альдегиды и кетоны"
81.Химические свойства альдегидов. Напишите реакции присоединения а) водорода, б) синильной кислоты, в) этилового спирта к бутаналю.
82.Различия в строении и химических свойствах альдегидов и кетонов покажите на примере пропаналя и пропанона.
83.Напишите изомерные карбонильные соединения состава C5H10O назовите по международной номенклатуре.
84.Напишите формулы следующих непредельных альдегидов и кетонов:
а) пропенал, б) 3-бутеналь. Напишите реакции а) присоединения брома и б) полимеризации для пропеналя.
85.Напишите структурную формулу соединения С4Н8О, которое при окислении дает кислоту С3Н7СООН, а при восстановлении изобутиловый спирт. Напишите эти реакции.
19
86.Определите строение соединения С5Н10О, если известно, что оно не реагирует с аммиачным раствором оксида серебра, а при гидрировании образует пентанол-3. Напишите уравнения реакций.
87.Осуществите следующие превращения; назовите все соединения и реакции
O
C2H6→ C2H5Cl → C2H5OH → CН3–С → CH3COOH
Н
88.Из соответствующих спиртов получите пентаналь и пентанон-3.
89.Химические свойства формальдегида. Как используется он в деревообработке?
90.Химические свойства уксусного альдегида?
3.3 АААААААААА ААААААА. ААААААА ААААА
Для органических кислот применяется не только исторически сложившаяся тривиальная номенклатура, но и рациональная (углерод и окончание "карбоновая", например:CH3–СООН метанкарбоновая), и международная (к окончанию соответствующего углеводорода добавляется окончание "овая": C2H3COOH – этановая кислота).
Изомерия карбоновых кислот обусловлена изомерией углеводородных
радикалов, входящих в структуру кислоты. |
O |
В карбоновых кислотах, содержащих карбоксил C |
, увеличивается |
|
ОH |
влияние кислорода на свойства органического соединения. Следует провести аналогию со спиртами. Показать взаимное влияние карбонильной и гидроксильной групп и вытекающие из этого следствия. Рассмотрите кислотные свойства карбоновых кислот, их способность к образованию галоидоангидридов и ангидридов кислот, сложных эфиров, амидов и нитрилов кислот. Обратите внимание на способы получения муравьиной, уксусной и высших кислот.
Соседство ароматического кольца увеличивает кислотные свойства ароматических кислот. Обратите внимание на практическое применение двухосновных (фталевых) кислот, их роль для получения синтетических полиэфиров.
Необходимо внимательно изучить свойства и методы получения важнейших производных карбоновых кислот - галоидоангидридов кислот, ангидридов кислот, сложных эфиров минеральных кислот, сложных эфиров карбоновых кислот, нитрилов кислот, а также иметь понятие о жирах, мылах и синтетических моющих средствах.
Что касается двухосновных кислот, то в этом разделе следует обратить внимание на практически важные кислоты - щавелевую, малоновую, а также на производные угольной кислоты фосген и карбамид (мочевину).
20
Контрольные вопросы к теме "Карбоновые кислоты. Сложные эфиры"
91.Напишите структурные формулы изомерных кислот C4H10O2, назовите по международной номенклатуре.
92.Химические свойства одноосновных карбоновых кислот покажите на примере пропановой кислоты.
93.Химические свойства дикарбоновых кислот. Напишите уравнения реакций щавелевой кислоты по одной и двум карбоксильным группам.
94.Реакции этерификации карбоновых кислот. Напишите уравнение получения сложных кислых и средних эфиров пропандикарбоновой кислоты.
95.Что такое производные кислот? Напишите их общие формулы и формулы производных уксусной кислоты.
96.Выведите формулы изомерных ароматических кислот состава C8H6O4, назовите. Для одной из этих кислот напишите уравнения этерификации метиловым спиртом.
97.Малеиновая и фумаровая кислоты. Малеиновый ангидрид, получение. Напишите уравнения гидрирования и этерификации малеиновой кислоты.
98.Чем отличаются простые эфиры от сложных? Напишите формулы простых и сложных эфиров на основе пропанола-2 и уксусной кислоты. Как применяются эфиры?
99.В чем различие между жирами и маслами? Напишите уравнения реакций триолеина а) с бромом, б) водородом. В чем значение этих реакций?
100.Составьте уравнения реакций по схеме, назовите все соединения и реакции.
OO
C2H2 → CH3–C → CH3–C → CH3–CO–OC2H5
HH
3.4АААААААААА АААААААА
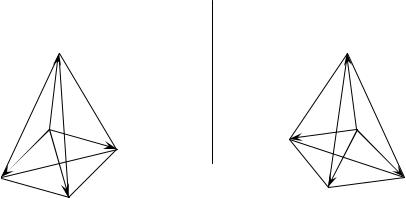
Одним из видов пространственной изомерии (стереоизомерии) является оптическая или зеркальная. Она возникает, если в молекуле содержится асимметрический атом углерода, т.е. атом, имеющий четыре различных заместителя. Например, в глицериновом альдегиде второй атом углерода асимметрический и молекула его может существовать в виде двух зеркальных противоположных изомеров
О |
О |
С |
С |
Н |
Н |
ОН |
НО |
Н |
Н |
СН2ОН |
СН2ОН |
|