Материал: 1082
U, кДж/моль |
|
|
|
|
|
|
|
|
|
170 |
|
|
|
|
|
|
|
|
|
155 |
|
|
|
|
|
|
|
|
Ц/З=100/0 |
140 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
125 |
|
|
|
|
|
|
|
|
Ц/З=60/40 |
110 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
95 |
|
|
|
|
|
|
|
|
|
80 |
|
|
|
|
|
|
|
|
|
20 |
40 |
60 |
80 |
100 |
120 |
140 |
160 |
180 |
200 |
|
|
|
|
|
|
|
|
Т, 0С |
|
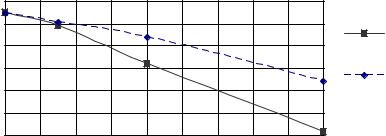
Рис. 6.8. Зависимость энергии активации от темпера- |
|||||||||
туры окружающего воздуха при фиксированной ско- |
|||||||||
рости вращения роторов дезинтегратора =16,67 с-1 |
|||||||||
Кроме того, наглядно продемонстрирована суть коэффициента перенапряжения D, т.к. знание сути данного коэффициента объясняет явления неравномерности распределения тепловой энергии между атомами твердого тела, порождаемой хаотичностью теплового движения.
Необходимо отметить, что с повышением коэффициента D возрастает наличие в твердом теле определенного числа атомов с повышенной энергией, позволяющей развиваться процессам, которые были бы немыслимы, если бы энергия была распределена равномерно и все атомы обладали бы средней, сравнительно низкой энергией.
Данные обстоятельства говорят о том, что величина энергии активации напрямую зависит от физико-механических свойств измельчаемого материала, а также режимных параметров дезинтеграторной установки.
Из вышеизложенного следует, что энергия активации является важным показателем процесса механической активации, связывающим физикомеханические характеристики обрабатываемого материала и технические параметры мельницы с конечными свойствами получаемого продукта. Учитывая, что отношение энергии активации U к средней тепловой энергии, приходящейся на одну степень свободы атомов тела, определяет скорость развития процесса, в данном случае для минеральных вяжущих понижение энергии активации в данном соотношении указывает на такие изменения физико-механических свойств последнего, как повышение сроков схватывания, набора прочности и т.д. Поэтому в зависимости от того, какие свойства готового материала необходимо получить, задается энергия активации процесса механоактивации получаемого материала.
Как было показано, по абсолютному значению U, обусловленному межатомным взаимодействием, можно судить о механизме процесса и участии в нем межатомных перегруппировок и разрывов межатомных связей, в этой связи очень важным является обстоятельство, что определенные из
механических испытаний величины U0 для различных твердых тел оказались близкими к начальной энергии активации распада межатомных связей, определяемых независимыми методами (не из механических испытаний), т.е. энергия активации U различных физико-химических процессов сходна по своему численному значению.
Это вносит ясность в картину разрушения тела, позволяя отождествить ее с процессом последовательного распада межатомных связей.
Предположим, что адекватность зависимости (6.15) можно проверить путем исследования кинетики механоактивационных процессов в обрабатываемом материале. В качестве последнего возьмем дифференциальнотермический анализ смесей, произведенный на высокотемпературном дериватографе МОМ 1000-1500 с помощью прибора "Derivatograph Q- 15000" /24/. Помимо адекватности формулы (6.15), дифференциальнотермический анализ смесей определяет эффективность механоактивации.
Суть метода, позволяющего определять параметры уравнения кинетики процесса декарбонизации, сводится к следующему: из-за сложности процессов термического разложения твердых веществ трудно найти количественное описание, адекватное конкретным физико-химическим превращениям в образце. Поэтому эти процессы описывают формальными уравнениями, в качестве которых обычно используют уравнение классической формальной химической кинетики:
|
d |
K(1 1)n , |
(6.18) |
||
|
|
||||
|
d |
|
|||
где 1 – степень превращения компонента, масс. доли; |
– время, мин; К |
||||
– константа скорости реакции; n – порядок реакции. |
|
||||
Зависимость константы скорости реакции К от энергии активации U |
|||||
(кДж/моль) можно выразить по уравнениям Аррениуса |
|
||||
|
K zexp( |
U |
), |
(6.19) |
|
|
|
||||
|
|
|
RT |
|
|
где z – предэкспоненциальный множитель, число столкновений молекул в секунду в единице объема; R – универсальная газовая постоянная, кДж/(моль.К); Т – абсолютная температура, К.
Как следует из уравнения Аррениуса, в которое U входит в качестве показателя степени, даже небольшое уменьшение энергии активации приводит к значительному возрастанию скорости реакции.
Температура в образце изменяется по линейному закону:
q |
dT |
const, |
(6.20) |
|
d |
||||
|
|
|
где q – скорость изменения температуры. Таким образом,

d 1 |
|
z |
exp( |
U |
)(1 1)n . |
(6.21) |
dT |
|
|
||||
|
q |
RT |
|
|||
В работе Н.Л. Глинки предложен интегральный метод определения кинетических параметров уравнения, описывающего неизотермический процесс потери массы образцов.
Уравнение (6.21) записывается в виде
|
|
d 1 |
|
|
|
z |
|
U |
|
|
1 |
exp( C)dC , |
|||||||
|
(1 1) |
n |
|
|
|
|
|
2 |
|||||||||||
|
|
|
|
q R |
|
|
C |
|
|
|
|
||||||||
где |
|
|
|
|
|
U |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
C |
. |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Интегрирование даст |
|
|
|
|
RT |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
q(a) |
da |
|
|
|
z |
|
|
U |
|
1 |
exp( C)dC . |
||||||||
(1 1)n |
|
q |
|
|
R |
C2 |
|||||||||||||
e x
Величина интеграла p(x) x2 dx.
Тогда уравнение (6.19) принимает вид
z U q( 1) R q p(x)
и после логарифмирования
z U
lg lgq( 1) lg p(x) B.
R q
(6.22)
(6.23)
(6.24)
(6.25)
(6.26)
Величина q( 1) может быть определена по экспериментальным данным для любого заданного n. Энергию активации определяют из условия постоянства разности
lg q( 1 |
) lg p( x ) B |
const. |
(6.27) |
|||||
В качестве критерия правильности выбора величины В рассматривает- |
||||||||
ся дисперсия данной величины: |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
D |
|
|
(Bi |
B)2 |
|
|
||
|
|
|
. |
|
(6.28) |
|||
|
|
|
|
|||||
N
В качестве наполнителя к цементу в данном исследовании использована зола-унос ТЭЦ-2 г. Омска.
Необходимо отметить, что скорость реакции декарбонизации существенно зависит от размера зерен известняка и повышается с понижением их размера. Для сырьевых смесей влияние на процесс диссоциации карбоната Са оказывает и реакционная способность остальных сырьевых компонентов. Так, например, известно, что глинистые минералы на 90 – 1300С уменьшают температуру диссоциации СаСО3.
Для расчета параметров кинетического уравнения неизотермического процесса декарбонизации используем данные прецизионного дифференци- ально-термического анализа по методике, описанной выше.
Полученные расчетом на ЭВМ данные представлены в табл. 6.4 и на рис. 6.9, а дериватограмма – на рис. 6.10.
В каждом случае точное содержание карбоната кальция в исследуемых смесях рассчитывается по суммарным потерям массы при съемке дериватограмм. Расхождения по потерям при прокалывании каждого из видов смеси не превышает 0,3 %, что доказывает постоянство их химического состава.
Необходимо отметить, что полученное значение начальной ( =0) энергии активации процесса декарбонизации исследуемых смесей совпадает с данными табл. 6.1.
180 |
|
|
|
|
|
|
U, кДж/моль |
|
|
|
|
|
|
170 |
|
|
|
|
|
|
160 |
|
|
|
|
|
Ц/З=100/0 |
|
|
|
|
|
|
|
150 |
|
|
|
|
|
Ц/З=60/40 |
140 |
|
|
|
|
|
|
130 |
|
|
|
|
|
|
0 |
10 |
20 |
30 |
40 |
50 |
, с-1 |
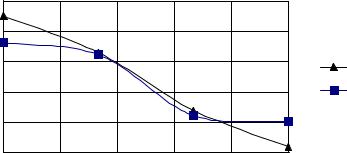
Рис. 6.9. Зависимость энергии активации |
|
|
||||
от скорости вращения роторов дезинтегратора |
|
|||||
Сравнение теплот эндотермического процесса декарбонизации для исследуемых смесей различной степени механической обработки показывает, что с увеличением скорости измельчения уменьшается значение энтальпии диссоциации. Поскольку тепловой эффект определялся по площади ДТА – кривой, невозможно разделить собственный эндоэффект декарбонизации и возможные экзоэффекты реакций взаимодействия химически активного оксида кальция с другими компонентами сырьевой смеси. С увеличением длительности обработки смеси, а также с добавлением в вяжущее золы, кроме уменьшения величины эндотермического пика разложения карбоната, происходит снижение температуры декарбонизации.
Анализ уравнения формальной неизотермической кинетики (6.18) показывает, что с повышением энергии активации от 130 до 180 кДж/моль при постоянных значениях остальных параметров скорость изменения степени декарбонизации при увеличении температуры уменьшается, т.е. чем меньше энергия активации, тем быстрее идет химический процесс (рис. 6.11). Можно предположить, что уменьшение затрат внешнего тепла на процесс декарбонизации вызвано появлением источника энергии в смеси,
причем интенсивность такого источника по мере увеличения нагрузки измельчения возрастает.
|
Термодинамические и кинетические параметры |
Таблица 6.4 |
||||||
|
|
|||||||
|
процесса декарбонизации механоактивированных смесей |
|||||||
Состав |
Скорость |
Энергия |
Поря- |
Предэкс- |
|
<Т>, 0С |
Ндек, |
К 1000к = |
смеси |
вращения |
актива- |
док |
понен- |
|
|
кДж/м |
zexp(- |
Ц/З |
роторов, |
ции U, |
реак- |
циальный |
|
|
оль |
U0/RT) |
|
, с-1 |
кДж/моль |
ции |
множитель |
|
|
|
|
|
|
|
n |
z |
|
|
|
|
10 |
|
|
0, |
. |
6 |
74 |
17 |
1,0.10 |
0/0 |
0 |
175,0 |
6 |
1,310 |
|
0…960 |
7,4 |
-3 |
10 |
|
|
0, |
. |
5 |
73 |
16 |
1,4.10 |
0/0 |
16,67 |
163,0 |
4 |
4,610 |
|
0…920 |
7,4 |
-3 |
10 |
|
|
0, |
. |
4 |
72 |
14 |
1,9.10 |
0/0 |
33,33 |
142,4 |
1 |
5,210 |
|
0…910 |
8,0 |
-3 |
10 |
|
|
0, |
. |
4 |
72 |
13 |
2,3.10 |
0/0 |
50,00 |
130,7 |
0 |
1,510 |
|
0…900 |
4,1 |
-3 |
60/ |
|
|
0, |
. |
5 |
73 |
15 |
1,2.10 |
40 |
0 |
166,3 |
4 |
6,010 |
|
0…930 |
6,5 |
-3 |
60/ |
|
|
0, |
. |
5 |
73 |
14 |
1,4.10 |
40 |
16,67 |
160,2 |
3 |
3,310 |
|
0…920 |
5,0 |
-3 |
60/ |
|
|
0, |
. |
4 |
72 |
13 |
2,0.10 |
40 |
33,33 |
144,1 |
1 |
6,810 |
|
0…920 |
0,3 |
-3 |
60/ |
|
|
0, |
. |
4 |
72 |
12 |
2,2.10 |
40 |
50,00 |
138,3 |
1 |
3,610 |
|
0…920 |
6,8 |
-3 |
Предэкспоненциальный коэффициент z можно рассматривать как меру интенсивности процесса. Чем больше z, тем больше скорость диссоциации известняка изменяется в сторону, определяемую параметрами U, n.
Наибольшее влияние на кинетику процесса декарбонизации на стадии, лимитируемой химической реакцией, оказывает параметр n. Отрицательное его значение означает, что процесс диссоциации карбоната Са ускоряется с увеличением степени диссоциации. Другими словами, образующийся в ходе реакции оксид Са инициирует процесс дальнейшего разложения карбоната Са, что равносильно, а образующийся оксид Са интенсивно связывается с другими компонентами смеси и тем самым удаляется из зоны реакции. Положительное же значение показателя n означает самоторможение процесса декарбонизации. Абсолютное значение n характеризует интенсивность просмотренных процессов.
Из данных табл. 6.4 явствует прямая связь между термодинамическимиН, U и кинетическими n, z параметрами процесса, что доказывает правильность сделанных выводов.