Материал: 1010-pochvovedenie-2013-7
856 |
|
|
МАКАРОВ и др. |
|
|
|
|
I |
|
II |
|
% |
АЛП |
|
ГКЛ |
АЛП |
ГКЛ |
80 |
|
|
|
80 |
|
60 |
|
|
|
60 |
|
А 40 |
|
|
|
40 |
|
20 |
|
|
|
20 |
|
0 |
|
|
|
0 |
|
% |
|
|
|
|
|
100 |
|
|
|
|
|
80 |
|
|
|
80 |
|
60 |
|
|
|
60 |
|
Б |
|
|
|
|
|
40 |
|
|
|
40 |
|
20 |
|
|
|
20 |
|
0 |
|
|
|
0 |
|
15N$NH Cl |
15N$NH Cl |
15N$NH Cl |
15N$NH Cl |
||
|
4 |
|
4 |
4 |
4 |
|
15N$глицин |
|
15N$глицин |
15N$глицин |
15N$глицин |
|
1 |
2 |
3 |
|
|
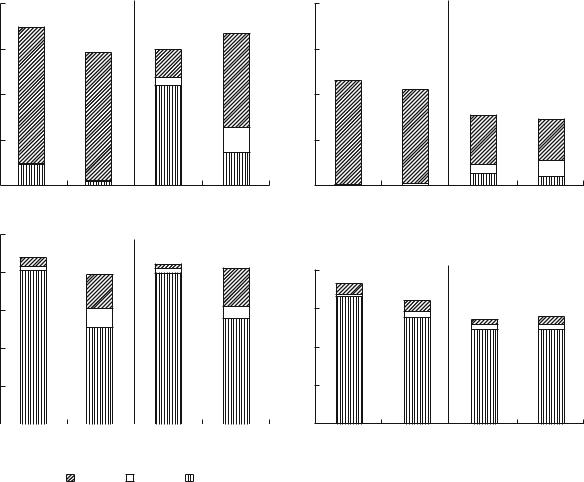
Распределение изотопной метки 15N, внесенной в составе NH4Cl и глицина, между лабильными фракциями азота че$ |
|||||
рез сутки (I) и через 15 суток (II) после внесения в свежие (А) и предварительно высушенные (Б) образцы почв. Обо$ |
|||||
значения: 1 – N микр, 2 – N орг, 3 – N$NH4+.
чия по азотному статусу: в бедной лабильными соединениями почве АЛП процессы трансформа$ ции азотсодержащих соединений протекают сла$ бее (менее интенсивно). Та же закономерность была показана ранее при проведении полевых инкубационных экспериментов и последующем анализе воздушно$сухих образцов почв [1, 6, 21].
Механизм мобилизации N орг во второй поло$ вине инкубации не вполне ясен, однако этот про$ цесс наблюдался как в почве АЛП, так и ГКЛ (в последнем случае происходила также мобилиза$ ция C орг). Из микробных показателей при инку$ бации свежих образцов горно$луговых почв за$ метное изменение затронуло лишь C микр в поч$ ве ГКЛ, концентрация которого увеличилась к концу эксперимента.
Высушивание изученных горно$луговых почв не только сильно изменило исходные их свой$ ства, но и принципиально повлияло на протека$ ние процессов микробной трансформации соеди$ нений N и C после увлажнения. В процессе инку$ бации предварительно высушивавшихся почв АЛП и ГКЛ происходило резкое изменение кон$ центраций всех изученных фракций N и C. Со$ держание N минеральных соединений возраста$ ло, а C орг и N орг уменьшалось (табл. 1, 2). Это свидетельствует об активной микробной транс$ формации лабильных органических соединений, поступивших в почву в результате гибели микро$ организмов при ее высушивании. Эти соедине$ ния подвергались интенсивной минерализации и менее интенсивной иммобилизации. Оба процес$ са протекали активнее в почве ГКЛ. При этом ми$ нерализация органических соединений N и C и
ПОЧВОВЕДЕНИЕ № 7 2013
ВЛИЯНИЕ ВЫСУШИВАНИЯ ОБРАЗЦОВ ГОРНО$ЛУГОВЫХ АЛЬПИЙСКИХ ПОЧВ |
857 |
их микробная иммобилизация были более актив$ ными в первой половине эксперимента, тогда как нитрификация – во второй половине. Несмотря на иммобилизацию N и C, концентрации N микр и C микр к концу эксперимента были в 1.5–2 раза меньше исходных значений, характерных для естественных горно$луговых почв.
Р а с п р е д е л е н и е и з о т о п н о й м е т к и 1 5 N м е ж д у р а з н ы м и а з о т н ы м и п у л а $ м и. Изотопная метка 15N, внесенная в образцы свежей почвы АЛП в составе NH4Cl и глицина, уже через сутки обнаруживалась в виде этих со$ единений лишь в небольшом количестве. Так, в
форме N$NH4+ оставалось всего около 10% 15N, внесенного в составе аммония, а в форме N орг – менее 1% 15N, внесенного в составе глицина. Еще
около 2% 15N глицина оказалось в составе N$NH4+. Основное же количество 15N, внесенного как в неорганической, так и в органической формах, вошло в состав N микр (рисунок). Всего же с ла$ бильными фракциями экстрагировалось 60–70% исходно добавленного в почву 15N. С учетом ко$ эффициента пересчета, учитывающего неполно$ ту экстракции N микр из хлороформированных образцов почвы [12], с микробной биомассой должно быть связано и все остальное количество 15N, которое не экстрагировалось 0.05 М K2SO4. Полученные результаты свидетельствуют, что ак$ тивность микробного сообщества почвы АЛП ли$ митирована доступностью N. Появление в почве небольшого, но сопоставимого с исходным со$
держанием (почти 100% N$NH4+ и около 50% N орг), дополнительного количества элемента в доступном виде, независимо от формы соедине$ ния, сопровождается его быстрой иммобилиза$ цией микроорганизмами. Аналогичные результа$ ты были получены в экспериментах с внесением изотопной метки 15N в тундровые почвы, где так$ же наблюдалась быстрая иммобилизация мик$ робной биомассой большей части внесенного N [15, 28].
В экспериментах с образцами свежей почвы ГКЛ изотопная метка 15N распределялась иным образом. Через сутки после ее внесения в составе
NH4Cl около 45% 15N оставалось в форме N$NH4+ и около 3.5% оказалось в форме N орг, а при вне$ сении глицина 11% 15N обнаруживалось в форме
N орг и 14% в виде N$NH4+. Таким образом, из со$ става NH4Cl микроорганизмы за сутки поглотили
чуть более половины внесенного 15N, а из состава глицина не поглощенным осталось около 25% 15N, который почти поровну распределился меж$
ду N$NH4+ и N орг (рисунок). Присутствие зна$ чительного количества изотопной метки в фор$
ме N$NH4+ при ее внесении в составе глицина
свидетельствует о достаточно активном процессе его минерализации. Полученные результаты сви$ детельствует, что микробное сообщество в почве ГКЛ в гораздо меньшей степени лимитировано доступностью N. В этой почве на долю добавлен$ ного 15N приходилось лишь около 20% от исход$
ного содержания N$NH4+ и N орг, изотопная мет$ ка медленнее иммобилизовалась микроорганиз$ мами, и заметнее проявлялось предпочтительное поглощение ими азота в органической форме по сравнению с минеральной. Еще меньшая ско$ рость микробной иммобилизации N показана для почв высокогорий Северной Америки, где за трое суток после внесения изотопа 15N в почву лишь 5% его было включено в состав N микр [19].
Распределение изотопа 15N в предварительно высушивавшихся образцах почв через сутки по$ сле внесения метки принципиально отличалось от его распределения в свежих образцах. В обеих почвах около 80% 15N, внесенного в составе
NH4Cl, обнаруживалось в форме N$NH4+. Из со$
става глицина также большое количество 15N (около 60%) не было поглощено микроорганиз$ мами, но и в этом случае преобладающая часть
15N (около 50%) оказалась в составе N$NH4+, сви$ детельствуя об активной минерализации амино$ кислоты (рисунок). Слабое закрепление 15N в со$ ставе микробной биомассы и активная минера$ лизация глицина свидетельствовали, что в высушенных почвах микробное сообщество не бы$ ло лимитировано доступностью азота. Хотя высу$ шенные образцы почв АЛП и ГКЛ заметно отлича$
лись по содержанию N$NH4+ и N орг (табл. 1), а вне$ сенный 15N составлял разные доли от лабильного N, перераспределение 15N между рассматривае$ мыми фракциями было сходным. Подобно образ$ цам свежей почвы ГКЛ, в высушенных образцах почв наблюдалась преимущественная микробная иммобилизация N из состава аминокислоты по сравнению с NH4Cl.
В свежих образцах почвы АЛП через 8 и 15 суток
после внесения изотопной метки в составе N$NH4+ и N орг обнаруживалось менее 1% 15N. Основное количество изотопа по$прежнему обнаружива$ лось в составе N микр, хотя его общая экстрагиру$ емость уменьшилась (рисунок), свидетельствуя о закреплении части 15N в составе органического вещества почвы или же в форме необменно$фик$
сированного NH4+. В почве ГКЛ в те же сроки ин$
кубирования в составе N$NH4+ оставалось около 5%, а в составе N орг – 5–10% 15N, то есть обмен изотопа между разными пулами происходил бо$ лее активно. Кроме того, экстрагируемость 15N из почвы ГКЛ к концу эксперимента заметно умень$ шилась по сравнению с почвой АЛП, что говорит
ПОЧВОВЕДЕНИЕ № 7 2013
858 |
МАКАРОВ и др. |
о более быстрой физико$химической иммобили$ зации N, а может быть и о частичной его потере в результате денитрификации. В высушивавшихся образцах почв АЛП и ГКЛ к концу эксперимента
в составе NH4+ сохранялось около половины вне$ сенного 15N, тогда как на долю N орг и N микр приходилось менее 10% (рисунок). Так же, как и в образцах свежей почвы, в ходе эксперимента с высушенными образцами экстрагируемость 15N уменьшилась.
ЗАКЛЮЧЕНИЕ
При высушивании образцов горно$луговых почв в них происходит гибель значительной части микроорганизмов, что способствует обогащению пулов N и C их лабильными соединениями. На
фоне изменения концентраций NH4+, N орг, N микр, C орг и C микр сохраняется различие почв разных биогеоценозов по степени обога$ щенности этими соединениями. Относительная разница в интенсивности процессов минерализа$ ции органических соединений N и нитрификации также сохраняется, однако более высокие показате$ ли активности этих процессов, определяемые при инкубировании предварительно высушивавшихся почв, не соответствуют естественному функциони$ рованию высокогорных почв. Кроме того, даже 15$дневное инкубирование при температуре 15°C предварительно высушенных образцов почв не приводит к восстановлению исходных запасов микробной биомассы. Таким образом, анализ вы$ сушенных образцов горно$луговых альпийских почв не отражает реальные концентрации в них лабильных соединений N и C и не позволяет су$ дить об активности происходящих процессов микробной трансформации органического веще$ ства. Однако при высушивании образцов почв со$ храняются относительные различия в концентра$ циях и активностях, существующие между есте$ ственными почвами.
СПИСОК ЛИТЕРАТУРЫ
1.Булатникова И.В., Макаров М.И., Малышева Т.И., Волков А.В. Минерализация органических соеди$ нений азота и нитрификация в горно$луговых аль$ пийских почвах Северо$Западного Кавказа // Вестн. Моск. ун$та. Сер. 17, почвоведение. 2003. № 2. С. 8–14.
2.Гришина Л.А., Онипченко В.Г., Макаров М.И., Ванясин В.А. Изменения свойств горно$луговых альпийских почв Северо$Западного Кавказа в раз$ личных экологических условиях // Почвоведение. 1993. № 4. С. 5–12.
3.Даденко Е.В., Казеев К.Ш., Колесников С.И., Вальков В.Ф. Изменение ферментативной актив$ ности при хранении почвенных образцов // Поч$ воведение. 2009. № 12. С. 1481–1486.
4.Кизилова А.К., Степанов А.Л., Макаров М.И. Био$ логическая активность горно$луговых альпийских почв Тебердинского заповедника // Почвоведе$ ние. 2006. № 1. С. 77–80.
5.Макаров М.И. Органические соединения фосфора в высокогорных почвах северо$западного Кавказа // Почвоведение. 1998. № 7. С. 854–863.
6.Макаров М.И., Леошкина Н.А., Ермак А.А., Малышева Т.И. Сезонная динамика доступности азота в горно$луговых альпийских почвах // Поч$ воведение. 2010. № 8. С. 969–978.
7.Онипченко В.Г. Фитомасса альпийских сообществ Северо$Западного Кавказа // Бюл. Моск. о$ва ис$ пытателей природы. Отд. биол. 1990. Т. 95. Вып. 6. С. 52–62.
8.Онипченко В.Г., Вертелина О.С., Макаров М.И.
Пространственная гетерогенность высокогорных фитоценозов и свойств почвы // Почвоведение. 1998. № 6. С. 689–695.
9.Практикум по агрохимии / Под ред. В.Г. Минеева. М.: Изд$во Моск. ун$та, 1989.
10.Практикум по почвоведению / Под ред. И.С. Кау$ ричева. М.: Колос, 1980.
11.Birch H.F. The effect of soil drying on humus decom$ position and nitrogen availability // Plant and Soil. 1958. V. 10. P. 9–31.
12.Brooks P.C., Landman A., Pruden G., Jenkinson D.S.
Chloroform fumigation and release of soil nitrogen: a rapid direct extraction method to measure microbial biomass nitrogen // Soil Biol. Biochem. 1985. V. 17. P. 837–842.
13.Dorich R.A., Nelson D.W. Evaluation of manual cadmi$ um reduction methods for determination of nitrate in potassium chloride extracts of soils // Soil Sci. Soc. Am. J. 1984. V. 48. P. 72–75.
14.Fierer N., Schimel J.P. Effects of drying$rewetting fre$ quency on soil carbon and nitrogen transformations // Soil Biol. Biochem. 2002. V. 34. P. 777–787.
15.Grogan P., Michelsen A., Ambus P., Jonasson S. Freeze$ thaw regime effects on carbon and nitrogen dynamics in sub$arctic heath tundra mesocosms // Soil Biol. Bio$ chem. 2004. V. 36. P. 641–654.
16.Holmes R.M., McClelland J.M., Sigman D.M., Fry B., Petersen B.J. Measuring 15N$NH4+ in marine, estuarine and fresh waters: An adaptation of the ammonia diffu$ sion method for samples with low ammonium concen$ trations // Marine Chemistry. 1998. V. 60. P. 235–243.
17.Kandeler E. Ammonium // Methods in soil biology. Berlin, Heidelberg: Springer$Verlag, 1996. P. 406–408.
18.Kirkham D., Bartholomew W.V. Equations for following nutrient transformations in soil, utilizing tracer data // Soil Sci. Soc. Am. Proc. 1954. V. 18. P. 33–34.
19.Lipson D.A., Monson R.K. Plant$microbe competition for soil amino acids in the alpine tundra: effects of freeze$thaw and dry$rewet events // Oecologia. 1998. V. 113. P. 406–414.
20.Lorenz N., Lee Y.*B., Dick L.K., Dick R. Impact of soil storage on soil microbial biomass, total DNA yield, en$ zyme activities and fatty acid microbial biomarkers // Materials of the World Congress of Soil Science. Phila$ delphia, USA. 2006. P. 659–660.
ПОЧВОВЕДЕНИЕ № 7 2013
ВЛИЯНИЕ ВЫСУШИВАНИЯ ОБРАЗЦОВ ГОРНО$ЛУГОВЫХ АЛЬПИЙСКИХ ПОЧВ |
859 |
21.Makarov M.I., Glaser B., Zech W., Malysheva T.I., Bu* latnikova I.V., Volkov A.V. Nitrogen dynamics in alpine ecosystems of the northern Caucasus // Plant and Soil. 2003. V. 256. P. 389–402.
22.Makarov M.I., Malysheva T.I., Cornelissen J.H.C., van Logtestijn R.S.P., Glasser B. Consistent patterns of 15N distribution through soil profiles in diverse alpine and tundra ecosystems // Soil Biol. Biochem. 2008. V. 40. P. 1082–1089.
23.Methods in soil biology / Eds.: F. Schinner et al. Berlin etc.: Springer$Verlag, 1996.
24.Mikha M.M., Rice C.W., Milliken G.A. Carbon and ni$ trogen mineralization as affected by drying and wetting circles // Soil Biol. Biochem. 2005. V. 37. P. 339–347.
25.Onipchenko V.G., Makarov M.I., van der Maarel E. In$ fluence of alpine plants on soil nutrient concentrations in a monoculture experiment // Folia geobotanica. 2001. V. 36. P. 225–241.
26.Ross D.J. Effects of storage on dehydrogenase activities of soils // Soil Biol. Biochem. 1970. V. 2. P. 55–61.
27.Schimel J.P., Bennett J. Nitrogen mineralization: chal$ lenges of a changing paradigm // Ecology. 2004. V. 85.
P.591–602.
28.Schimel J.P., Chapin F.S. III. Tundra plant uptake of amino acid and NH4+ nitrogen in situ: plants compete well for amino acid N // Ecology. 1996. V. 77. P. 2142– 2147.
29.Schmidt I.K., Jonasson S., Shaver G.R., Michelsen A., Nordin A. Mineralization and distribution of nutrients in plants and microbes in four arctic ecosystems: re$ sponses to warming // Plant and Soil. 2002. V. 242.
P.93–106.
30.Soil sampling and methods of analysis / Ed. M.R. Cart$ er. Boca Raton etc.: Lewis Publishers, 1993.
31.Vance E.D., Brookes P.C., Jenkinson D.S. An extraction method for measuring soil microbial biomass C // Soil Biol. Biochem. 1987. V. 19. P. 703–707.
32.Xiang S.*R., Doyle A., Holden P.A., Schimel J.P. Drying and rewetting effects on C and N mineralization and microbial activity in surface and subsurface California grassland soils // Soil Biol. Biochem. 2008. V. 40.
P.2281–2289.
ПОЧВОВЕДЕНИЕ № 7 2013

ПОЧВОВЕДЕНИЕ, 2013, № 7, с. 860–866
БИОЛОГИЯ
ПОЧВ
УДК 631.46:58.051
ЧИСЛЕННОСТЬ И СТРУКТУРА КОМПЛЕКСОВ ПОЧВЕННЫХ АКТИНОМИЦЕТОВ В РАЙОНЕ ВОЗМОЖНОГО ВЛИЯНИЯ ХИМИЧЕСКИ ОПАСНОГО ОБЪЕКТА
© 2013 г. И. Г. Широких1, 2, Е. В. Товстик1, Е. В. Дабах2, Т. Я. Ашихмина2
1 НИИСХ Северо Востока им. Н.В. Рудницкого, 610007, Киров, ул. Ленина, 166а 2 Институт биологии Коми НЦ УрО РАН и ВятГГУ, 610002, Киров, ул. Свободы, 122
e mail: irgenal@mail.ru
Поступила в редакцию: 08.10.2012 г.
Рассмотрены численность, разнообразие и структура комплексов актиномицетов в ряду сопряжен ных почв подзоны южной тайги вблизи полигона хранения и уничтожения химического оружия “Марадыковский”. Показаны количественные и качественные различия актиномицетных ком плексов, обусловленные как естественными условиями формирования – кислотностью и грануло метрическим составом почвы, характером растительности, так и удаленностью от объекта, опреде ляющей степень техногенного воздействия на почву. Отличия в структуре комплексов почвенных актиномицетов вблизи объекта заключались в изменении структуры доминирования, частоты встречаемости и относительного обилия представителей родов Streptomyces и Micromonospora, сокра щении или, напротив, расширении видового и родового разнообразия мицелиальных прокариот.
Ключевые слова: почвы, биодиагностика, уничтожение химического оружия, техногенное воздей ствие.
DOI: 10.7868/S0032180X13070101
ВВЕДЕНИЕ
Объекты хранения и уничтожения химическо го оружия относятся к числу объектов повышен ной техногенной опасности для природных ком плексов и экосистем [1]. Поскольку в результате их производственной деятельности возможно по ступление в природную среду токсических про дуктов в количествах, находящихся за пределами возможности их обнаружения инструментальны ми методами анализа, контроль загрязнения поч венного покрова в зоне влияния объекта, наряду с физико химическими показателями, должен вклю чать методы биодиагностики – выявление реакций на воздействие комплекса ксенобиотиков со сторо ны биологических систем. Почвенные микроб ные комплексы в силу большого разнообразия биохимических функций и высокой чувствитель ности к изменениям среды перспективны в био индикации возникающих нарушений и последу ющей биоремедиации экосистем [2, 15–17].
Неотъемлемой частью микробного комплекса почвы являются актиномицеты, составляющие четвертую часть от общего количества бактерий, вырастающих на традиционно используемых пи тательных средах при посеве из разведений поч венных суспензий [6]. Техногенные воздействия,
как правило, вызывают изменение структуры комплекса почвенных актиномицетов [10], кото рая определяется составом и численностью ти пичных родов и видов и величиной видового спектра, специфичных для каждого типа биогео ценозов. Накопление данных, характеризующих актиномицетные комплексы в различных экоси стемах, позволяет перейти к выявлению влияния на них различных видов техногенных воздей ствий [4, 5, 7, 8].
Поскольку почвенный покров районов разме щения объектов хранения и уничтожения хими ческого оружия, как правило, неоднороден, про цесс сопоставления получаемой информации, не всегда дает возможность выявить те биологиче ские эффекты, которые вызваны техногенным воздействием. Для более корректной интерпрета ции получаемой в процессе мониторинга инфор мации необходимо разграничение изменчивости почвенного микробного комплекса, обусловлен ной естественными и техногенными причинами.
Целью работы было сравнительное изучение комплексов актиномицетов в ряду сопряженных подзолистых и дерново подзолистых почв лес ных и луговых фитоценозов, расположенных в зоне возможного влияния объекта хранения и
860