Материал: Задачи по биохимии
10.вопрос
Макроэргические соединения:
А) Макроэргические соединения – органические соединения живых клеток, содержащие богатые энергией, или макроэргические связи. Эти соединения образуются в результате фото- и хемосинтеза и биологического окисления. К ним относятся, например, вещества, при гидролизе которых высвобождается энергии в 2—4 раза больше, чем при гидролизе других веществ. К макроэргическим соединениям относятся аденозинтрифосфорная кислота (АТФ), аденозиндифосфорная кислота (АДФ), а также пирофосфат (H4P2O7), полифосфаты (полимеры метафосфорной кислоты — (НРО3)n * Н2О) и ряд других соединений. Самое важное макроэргическое соединение — АТФ. Используя энергию, заключенную в макроэргических связях АТФ, при действии ферментов, переносящих фосфатные группы, можно получить другие макроэргические соединения, например, ГТФ (гуанозинтрифосфорная кислота), ФЕП (фосфоенолпировиноградная кислота) и др. Образуется АТФ в процессах биологического окисления и при фотосинтезе.
Макроэргические связи — это ковалентные связи, которые гидролизуются с выделением значительного количества энергии: 30 кДж/моль и более (свободная энергия гидролиза).Вообще термин «макроэргическая связь» используется исключительно для связей, энергия которых используется в метаболизме и не указывает на истинную величину энергии связейОбычно это относится к макроэргическим молекулам — биологическим молекулам, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды карбоновой и фосфорной кислот, а также других слабых кислот. Примеры макроэргических соединений — молекулы АТФ, ГТФ и НАД. В АТФ имеются 2 макроэргические связи.
Б)
К макроэргическим соединениям относятся,
главным образом, аденозинтрифосфорная
кислота (АТФ) и вещества, способные
образовывать АТФ в ферментативных
реакциях переноса преимущественно
фосфатных групп, а также нуклеозидтри-
(или ди) -фосфорные кислоты, пирофосфорная
и полифосфорная кислоты, креатинфосфорная,
фосфопировиноградная, дифосфоглицериновая
кислоты, ацетил- и сукцинилкоферменты
А, аминоацильные производные адениловой
и рибонуклеиновых кислот и другие.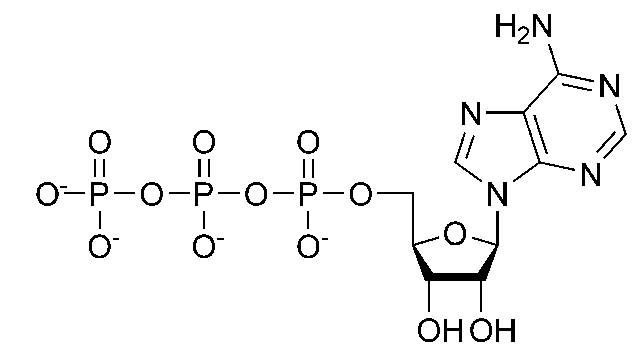 Аденозинтрифосфорная кислота (АТФ)
Аденозинтрифосфорная кислота (АТФ)
Энергия, которая выделяется при распаде макроэргических соединений и за счет которой может быть совершена та или иная работа, используется не только для химического синтеза. Она может служить в организме для теплообразования, свечения, накопления электричества, выполнения механической работы и т. п. При этом химическая энергия преобразуется в тепловую, лучистую, электрическую, механическую и пр. Принципиально важно то, что преобразование химической энергии в другие ее виды протекает в организме при обязательном участии соединений с макроэргическими связями, в частности АТФ. В молекуле АТФ происходит трансформация стабильной энергии макроэргических межфосфатных химических связей в подвижную энергию возбуждения электронов пуриновой части молекулы; это и есть, вероятно, первый этап преобразования энергии в организме. Именно поэтому АТФ занимает центральное место в энергетическом обмене живой материи.
В) В организме АТФ синтезируется путём фосфорилирования АДФ:
АДФ + H3PO4 + энергия → АТФ + H2O.
Фосфорилирование АДФ возможно тремя способами: субстратное фосфорилирование и окислительное фосфорилирование, (используя энергию окисляющихся веществ) и фотофосфорилирование в процессе фотосинтеза у растений. Основная масса АТФ образуется на мембранах митохондрий в ходе окислительного фосфорилирования H-зависимой АТФ-синтазой. Субстратное фосфорилирование АТФ не требует участия мембранных ферментов, оно происходит в цитоплазме в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений.
Реакции фосфорилирования АДФ и последующего использования АТФ в качестве источника энергии образуют циклический процесс, составляющий суть энергетического обмена.
11. ЦПЭ в митохондриях
А) Дыхательная цепь переноса электронов (ЭТЦ)— система структурно и функционально связанных трансмембранных белков и переносчиков электронов. ЭТЦ запасает энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН2 молекулярным кислородом (в случае аэробного дыхания) или иными веществами (в случае анаэробного) в форме трансмембранного протонного потенциала за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану.
Комплексы дыхательной цепи
-Комплекс I (НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 2 протона и 2 электрона из матрикса в межмембранное пространство митохондрии.
-Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
-Комплекс III (Цитохром bc1 комплекс) переносит электроны с убихинона на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинон передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинона и перекачиваются комплексом.
-Комплекс IV (Цитохромоксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a3, которые, помимо гема, содержат ионы меди.
Кислород, поступающий в митохондрии из крови, связывается с атомом железа в геме цитохрома a3 в форме молекулы O2. Каждый из атомов кислорода присоединяет по два электрона и два протона и превращается в молекулу воды.
Б) ЦПЭ локализуется на внутренней мембране митохондрий.
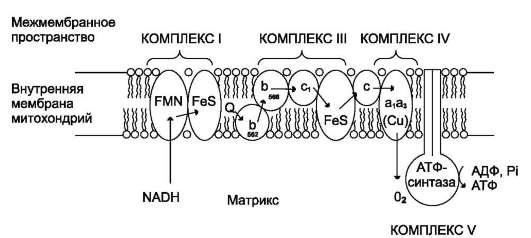
В) В интактной (неповрежденной) митохондриальной мембране перенос электронов в дыхательной цепи и фосфорилирование тесно сопряжены между собой.
Так, например, выключение фосфорилирования по исчерпании АДФ либо неорганического фосфата сопровождается торможением дыхания (эффект дыхательного контроля). Большое число повреждающих митохондриальную мембрану воздействий нарушает сопряжение между окислением и фосфорилированием, разрешая идти переносу электронов и в отсутствие синтеза АТФ (эффект разобщения).
В настоящее время наиболее признанной гипотезой, объясняющей синтез АТФ, является хемиосмотическая гипотеза.
Хемиосмотическая гипотеза сформулированна английским биохимиком Питером Митчеллом.
Согласно этой гипотезе, цепь переноса электронов можно представить себе как насос, перекачивающий ионы Н+. Энергия, высвобождаемая при переносе электронов, используется для перемещения ионов Н+ из митохондриального матрикса наружу, что приводит к возникновению электрохимического Н+ градиента с более высокой концентрацией ионов Н+ в наружной водной фазе. Этот же процесс ведет к появлению трансмембранного электрического потенциала - наружная сторона мембраны оказывается электроположительной. Ионы Н+ из окружающей Среды вновь устремляются внутрь, т.е. в митохондриальный матрикс, на этот раз по электрохимическому градиенту. Этот переход ионов Н+ из зоны с более высокой в зону с более низкой их концентрацией сопровождается выделением свободной энергии, за счет которой синтезируется АТФ.
Электрохимический Н+ градиет с более высокой концентрацией Н+ на наружной мембране.
Трансмембранный электрический потенциал - наружная мембрана заряжена положительно, а внутренняя - отрицательно.
Ионы Н+ из окружающей среды по электрохимическому градиенту идут внутрь митохондрии и этот процесс сопровождается выделением свободной энергии, которая идет на синтез АТФ.
13. Ингибиторы можно разделить на 3 группы: ингибиторы собственно дыхательной цепи, ингибиторы окислительного фосфорилирования и разобщители окислительного фосфорилирования.
Ингибиторы, блокирующие дыхательную цепь, по-видимому, действуют в трех местах. Одно из них ингибируется барбитуратами (например, амобарбиталом), а также антибиотиком пиерицидином А и ротеноном. Эти ингибиторы препятствуют окислению субстратов, которые поставляют восстановительные эквиваленты в дыхательную цепь при участии NAD-зависимых дегидрогеназ, — примером таких субстратов является гидроксибутират.
Димеркапрол и антимицин А ингибируют дыхательную цепь на участке между цитохромом b и цитохромом с. Классические яды окись углерода и цианид — ингибируют цитохромоксидазу. Карбоксин и TTFA (теноилтрифторацегон) специфически ингибируют переход восстановительных эквивалентов от сукцинатдегидрогеназы на кофермент Q, а малонат является конкурентным ингибитором сукцинатдегидрогеназы.
Антибиотик олигомицин полностью блокирует окисление и фосфорилирование в интактных митохондриях. Однако если вместе с олигомицином добавить к системе разобщитель динитрофенол, то окисление протекает, но без фосфорилирования. Это означает, что олигомицин не действует непосредственно на дыхательную цепь, а подавляет стадию фосфорилирования .
Атрактилознд ингибирует окислительное фосфорилирование, блокируя транспорт адениновых нуклеотидов через внутреннюю митохондриальную мембрану. Он ингибирует транспорт ADP в митохондрии и выход АТР из митохондрий .
Разобщители нарушают систему сопряжения процессов окисления в дыхательной цепи и фосфорилирования. В этих условиях процесс дыхания происходит неконтролируемым образом, поскольку концентрации ADP или Р, не являются лимитирующими.
Чаще всего в качестве разобщителя используют 2,4-динитрофенол; аналогичное действие оказывает ряд других соединений: динитрокрезол, пентахлорфенол, СССР (карбонилцианид-л-хлорфенилгидразон). Последний по эффективности в 100 раз превосходит динитрофенол.
Ингибиторы I комплекса — барбитураты, ротенон, пиерицидин
Ингибитор II комплекса — малонат.
Ингибитор III комплекса — антимицин А, миксотиазол, стигматтелин
Ингибиторы IV комплекса — сероводород, цианиды, угарный газ, оксид азота.
14 Разобщители тканевого дыхания (динитроортокрезол)
Известны вещества, способные разобщать процессы биологического окисления и фосфорилирования. Такими свойствами обладают, как правило, липофильные соединения, содержащие фенольную группу в молекуле и являющиеся слабыми органическими кислотами. Наиболее известными и широко используемыми в хозяйственной деятельности представителями группы являются 2,4-динитрофенол (ДНФ), динитро-о-крезол (ДНОК), пентахлорфенол. При авариях на промышленных объектах и других чрезвычайных ситуациях эти вещества могут стать причиной массового поражения людей.
In vitro разобщители тканевого дыхания стимулируют скорость потребления кислорода митохондриями и индуцируют активность АТФазы. In vivo в результате их действия значительно активируются процессы биологического окисления и потребления кислорода тканями, однако содержание АТФ и других макроэргов в клетках при этом снижается. Развиваются типичные для отравления веществами общеядовитого действия признаки интоксикации. Образующаяся в ходе окисления субстратов энергия рассеивается в форме тепла, температура тела отравленного резко повышается, что является характерным признаком острого отравления разобщителями тканевого дыхания.
Биологическая роль свободного, или нефосфорилирующего, окисления.
Биологический смысл нефосфорилирующего — свободного — окисления можно видеть в многочисленных реакциях окисления, не связанных с лимоннокислым циклом и переносом водорода и электронов по дыхательной цепи. Сюда относятся, например, все внемитохондриальные процессы окисления, окислительное удаление токсически действующих веществ и многие акты регуляции количественного содержания биологически активных соединений (некоторых аминокислот, биогенных аминов, адреналина, гистидина, серотонина и т. д., альдегидов и пр.) путем более или менее интенсивного их окисления. Соотношение свободного и фосфорилирующего окисления является также одним из путей терморегуляции у человека и теплокровных животных 15 Окисли́тельное декарбоксили́рование пирува́та — биохимический процесс, заключающийся в отщеплении одной молекулы углекислого газа (СО2) от молекулы пирувата и присоединения к декарбоксилированному пирувату кофермента А (СоА) с образованием ацетил-СоА; является промежуточным этапом между гликолизом и циклом трикарбоновых кислот. Декарбоксилирование пирувата осуществляет сложный пируватдегидрогеназный комплекс (PDH), включающий в себя 3 фермента и 2 вспомогательных белка, а для его функционирования необходимы 5 кофакторов (СоА, NAD+, тиаминпирофосфат (ТРР),FAD и липоевая кислота (липоат)). Суммарное уравнение окислительного декарбоксилирования пирувата таково[1]:
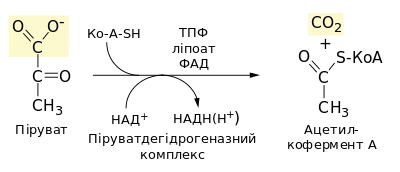
Компоненты
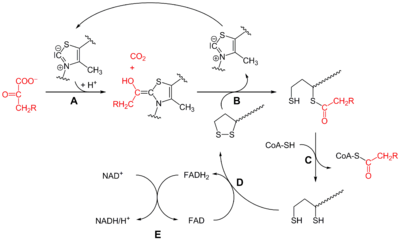
Работа пируватдегидрогеназного комплекса
Пируватдегидрогеназный комплекс включает в себя 3 фермента, 3 кофактора (простетическая группа,связанная с апоферментом прочно ковалентно), 2 кофермента (простетическая группа, связанная сапоферментом непрочно нековалентно):
-
Е1 — пируватдегидрогеназа декарбоксилирующая.
-
Кофактором является активная форма витамина В1 — тиаминпирофосфат.
Е2 — дигидролипоилацетилтрансфераза.
-
Кофактором является витаминоподобное вещество — липоевая кислота, которая присоединив 2 атомаводорода может превращаться в дигидролипоил.
-
Коферментом является активная форма пантотеновой кислоты — НS-КоА, она принимает ацетильныйостаток от липоевой кислоты.
Е3 — дигидролипоилдегидрогеназа .
-
Кофактором является флавинадениндинуклеотид (ФАД) — активная форма витамина В2.
-
Коферментом является активная форма витамина PP — никотинамидадениндинуклеотид (НАД+).
Регуляция
«По механизму обратной связи» ингибируют работу пируватдегидрогеназного комплекса конечные продуктыокислительного декарбоксилирования — ацетил-КоА, НАДН.Н+, а также АТФ. Увеличивает активностькомплекса пируват.
Также имеется регуляция со стороны гормонов: Инсулин увеличивает активность комплекса, глюкагон —снижает.
16.
Цикл трикарбоновых кислот — это ключевой этап дыхания всех клеток, использующих кислород, центр пересечения множества метаболических путей в организме, промежуточный этап между гликолизом и электронтранспортной цепью. Кроме значительной энергетической роли циклу отводится также и существенная пластическая функция.
Главная роль ЦТК — образование большого количества АТФ. Значения ЦТК :
1) главный источник АТФ. Энергию для образования большого количества АТФ дает полный распад Ацетил-КоА до СО2 и Н2О;
2) универсальный терминальный этап катаболизма веществ всех классов;
3) играет важную роль в процессах анаболизма (промежуточные продукты ЦТК): а) из цитрата ——>синтез жирных кислот; б) из a-кетоглутарата и ЩУК (щавеливо-уксусная кислота) ——> синтез аминокислот; в) из ЩУК ——> синтез углеводов; г) из Сукцинил-КоА ——> синтез гема гемоглобина.
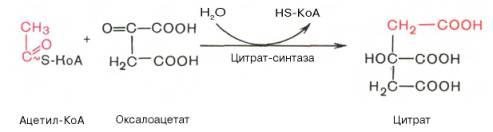
Данный цикл происходит в матриксе митохондрий и состоит из восьми последовательных реакций.
1.
2.
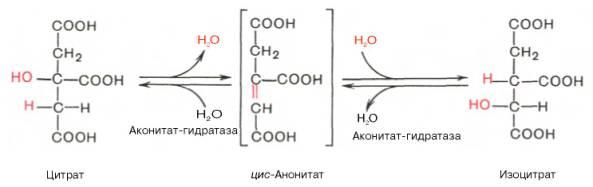
3.
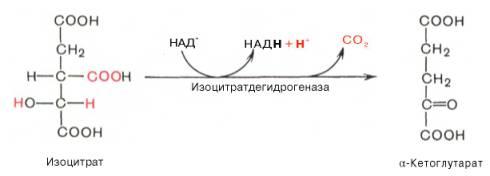
4.
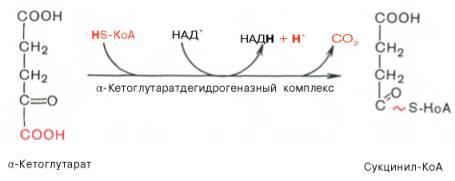
5.
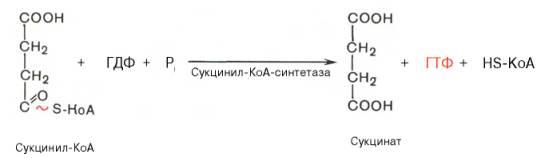
6.
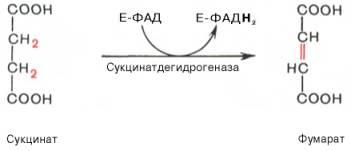
7.
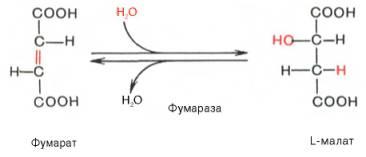
8.

Главным и основным регулятором ЦТК является оксалоацетат, а точнее его доступность. Наличие оксалоацетата вовлекает в ЦТК ацетил-SKoA и запускает процесс.
17.
Переваривание углеводов
Переваривание это процесс гидролиза веществ до их ассимилируемых форм. Переваривание бывает: 1). Внутриклеточное (в лизосомах); 2). Внеклеточное (в ЖКТ): а). полостное (дистантное); б). пристеночное (контактное).
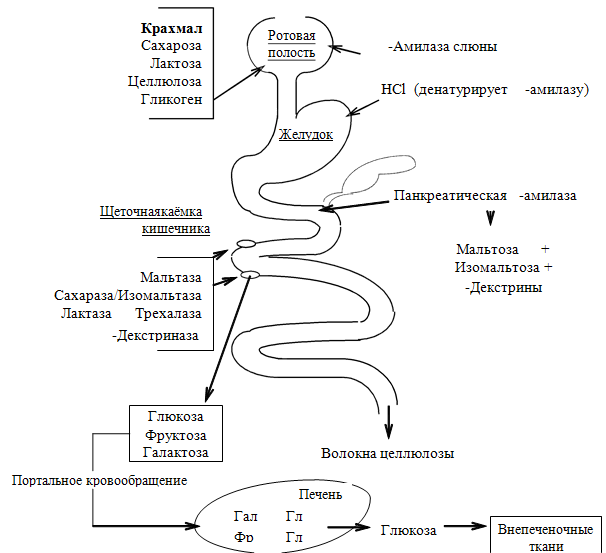
Переваривание углеводов в ротовой полости (полостное)
В ротовой полости пища измельчается при пережёвывании и смачивается слюной. Слюна состоит на 99% из воды и обычно имеет рН 6,8. В слюне присутствует эндогликозидаза α-амилаза (α-1,4-гликозидаза),расщепляющая в крахмале внутренние α-1,4-гликозидные связи с образованием крупных фрагментов — декстринов и небольшого количества мальтозы и изомальтозы. Необходим ион Cl-.
Переваривание углеводов в желудке (полостное)
Действие амилазы слюны прекращается в кислой среде (рН <4) содержимого желудка, однако, внутри пищевого комка активность амилазы может некоторое время сохраняться. Желудочный сок не содержит ферментов, расщепляющих углеводы, в нем возможен лишь незначительный кислотный гидролиз гликозидных связей.
Переваривание углеводов в тонком кишечнике (полостное и пристеночное)
В двенадцатиперстной кишке кислое содержимое желудка нейтрализуется соком поджелудочной железы (рН 7,5—8,0 за счет бикарбонатов). С соком поджелудочной железы в кишечник поступает панкреатическая α-амилаза. Эта эндогликозидаза гидролизует внутренние α-1,4-гликозидные связи в крахмале и декстринах с образованием мальтозы (2 остатка глюкозы, связанные α-1,4-гликозидной связью), изомальтозы (2 остатка глюкозы, связанные α-1,6-гликозидной связью) и олигосахаридов, содержащих 3—8 остатков глюкозы, связанных α-1,4- и α-1,6-гликозидными связями.
Переваривание мальтозы, изомальтозы и олигосахаридов происходит под действием специфических ферментов - экзогликозидаз, образующих ферментативные комплексы. Эти комплексы находятся на поверхности эпителиальных клеток тонкого кишечника и осуществляют пристеночное пищеварение.
-
Сахаразо-изомальтазный комплекс состоит из 2 пептидов, имеет доменное строение. Из первого пептида образован цитоплазматический, трансмембранный (фиксирует комплекс на мембране энтероцитов) и связывающий домены и изомальтазная субъединица. Из второго - сахаразная субъединица. Сахаразная субъединица гидролизует α-1,2-гликозидные связи в сахарозе, изомальтазная субъединица - α-1,6-гликозидные связи в изомальтозе, α-1,4-гликозидные связи в мальтозе и мальтотриозе. Комплекса много в тощей кишке, меньше в проксимальнойи дистальной частях кишечника.
-
Гликоамилазный комплекс, содержит две каталитические субъединицы, имеющие небольшие различия в субстратной специфичности. Гидролизует α-1,4-гликозидные связи в олигосахаридах (с восстанавливающего конца) и в мальтозе. Наибольшая активность в нижних отделах тонкого кишечника.
-
β-Гликозидазный комплекс (лактаза) гликопротеин, гидролизует β-1,4-гликозидные связи в лактозе. Активность лактазы зависит от возраста. У плода она особенно повышена в поздние сроки беременности и сохраняется на высоком уровне до 5-7-летнего возраста. Затем активность лактазы снижается, составляя у взрослых 10% от уровня активности, характерного для детей.
-
Трегалаза гликозидазный комплекс, гидролизует α-1,1-гликозидные связи между глюкозами в трегалозе — дисахариде грибов.
Переваривание углеводов заканчивается образованием моносахаридов – в основном глюкозы, меньше образуется фруктозы и галактозы, еще меньше – маннозы, ксилозы и арабинозы.
Всасывание углеводов
Моносахариды всасываются эпителиальными клетками тощей и подвздошной кишок. Транспорт моносахаридов в клетки слизистой оболочки кишечника может осуществляться путём диффузии (рибоза, ксилоза, арабиноза), облегчённой диффузии с помощью белков переносчиков (фруктоза, галактоза, глюкоза), и путем вторично-активного транспорта (галактоза, глюкоза). Вторично-активный транспорт галактозы и глюкозы из просвета кишечника в энтероцит осуществляется симпортом с Na+. Через белок-переносчик Na+ двигается по градиенту своей концентрации и переносит с собой углеводы против их градиента концентраций. Градиент концентрации Na+ создаётся Nа+/К+-АТФ-азой.
При низкой концентрации глюкозы в просвете кишечника она транспортируется в энтероцит только активным транспортом, при высокой концентрации - активным транспортом и облегчённой диффузией. Скорость всасывания: галактоза > глюкоза > фруктоза > другие моносахариды. Моносахариды выходят из энтероцитов в направлении кровеносного капилляра с помощью облегченной диффузии через белки-переносчики.
Нарушение переваривания и всасывания углеводов
Недостаточное переваривание и всасывание переваренных продуктов называют мальабсорбцией. В основе мальабсорбции углеводов могут быть причины двух типов:
1). Наследственные и приобретенные дефекты ферментов, участвующих в переваривании. Известны наследственные дефекты лактазы, α-амилазы, сахаразно-изомальтазного комплекса. Без лечения эти патологии сопровождаются хроническим дисбактериозом и нарушениями физического развития ребёнка.
Приобретённые нарушения переваривания могут наблюдаться при кишечных заболеваниях, например гастритах, колитах, энтеритах, после операций на ЖКТ.
Дефицит лактазы у взрослых людей может быть связан со снижением экспрессии гена лактазы, что проявляться непереносимостью молока - наблюдается рвота, диарея, спазмы и боли в животе, метеоризм.
2). Нарушение всасывания моносахаридов в кишечнике.
Нарушения всасывания могут быть следствием дефекта какого-либо компонента, участвующего в системе транспорта моносахаридов через мембрану. Описаны патологии, связанные с дефектом натрийзависимого белка переносчика глюкозы.
Синдром мальабсорбции сопровождается осмотической диареей, усилением перистальтики, спазмами, болями, а также метеоризмом. Диарею вызывают нерасщеплённые дисахариды или невсосавшиеся моносахариды в дистальных отделах кишечника, а также органические кислоты, образованные микроорганизмами при неполном расщеплении углеводов.
18. Биологическая роль, синтез и распад гликогена. Особенности распада гликогена в печени и скелетных мышцах.
Многие ткани синтезируют в качестве резервной формы глюкозы гликоген. Синтез и распад гликогена обеспечивают постоянство концентрации глюкозы в крови и создают депо для её использования тканями по мере необходимости.
Синтез гликогена. Глюкоза, поступающая в клетку, фосфорилируется при участии АТФ (реакция 1). Затем глюкозо-6-фосфат в ходе обратимой реакции превращается в глюкозо-1 -фосфат (реакция 2) под действием фермента фосфоглюкомутазы. Реакция 3 - стадия образования уридинди-фосфатглюкозы из УТФ и глюкозо-1-фосфата. Фермент, катализирующий эту реакцию, назван по обратной реакции: УДФ-глюкопирофосфорилаза. Однако в клетке обратная реакция не протекает, потому что образовавшийся в ходе прямой реакции пирофосфат очень быстро расщепляется пирофосфатазой на 2 молекулы фосфата. Образованная УДФ-глюкоза далее используется как донор остатка глюкозы при синтезе гликогена (реакция 4). Эту реакцию катализирует фермент гликогенсинтаза (глюкозилтрансфераза). Так как гликоген в клетке никогда не расщепляется полностью, синтез гликогена осуществляется путём удлинения уже имеющейся молекулы полисахарида, называемой "затравка", или "праймер". К "затравке" последовательно присоединяются молекулы глюкозы. Строением молекулы "затравки" как бы предопределяется тип связи, который возникает в реакции трансгли-козилирования. Таким образом, синтезируется полисахарид, аналогичный по строению с "затравочным". В состав "затравки" может входить белок гликогенин, в котором к ОН-группе одного из тирозиновых остатков присоединена олигосахаридная цепочка (примерно 8 остатков глюкозы). Глюкозные остатки переносятся гликогенсинтазой на нередуцирующий конец олигосахарида и связываются α-1,4-гликозидными связями. По окончании синтеза гликогенин остаётся включённым в гранулу гликогена. Разветвлённая структура гликогена образуется при участии амило-1,4 →1,6-глюкозилтрансферазы, называемой ферментом "ветвления"