Материал: Задачи по биохимии
В настоящее время обнаружены 14 человеческих Gla-белков, играющих ключевые роли в регулировании следующих физиологических процессов:
-
свёртывание крови (протромбин (фактор II), факторы VII, IX, X, белок C, белок S и белок Z). [2]
-
метаболизм костей (остеокальцин, также названный Gla-белком кости, и матрицей gla белка (MGP)). [3]
-
сосудистая биология. [4]
Некоторые бактерии, такие как кишечная палочка, найденная в толстом кишечнике, способны синтезировать витамин K2 , но не витамин K1.)[5]
В этих бактериях витамин K2 служит переносчиком электронов в процессе, называемым анаэробным дыханием. Например, такие молекулы, как лактаты, формиаты или NADH, являющиеся донорами электронов, с помощью фермента передают два электрона K2. Витамин K2 в свою очередь передает эти электроны молекулам — акцепторам электронов, таким как фумараты или нитраты, которые, соответственно, восстанавливаются до сукцинатов или нитритов. В результате таких реакций синтезируется клеточный источник энергии АТФ, подобно тому, как он синтезируется в эукариотических клетках с аэробным дыханием. Кишечная палочка способна осуществлять как аэробное, так и анаэробное дыхание, в котором участвуют интермедиаты менахиноны.
-
Вит.Д3(холекальциферол)
-
Витамин D в обеих формах (холекальциферол и эргокальциферол) является на самом деле провитамином. Для активации холекальциферол сначала должен превратиться в печени в 25-гидрокси-холекальциферол (сокращенно 25(HO)D), а затем в почках — в 1,25-дигидрокси-холекальциферол (кальцитриол).
-
Оценка адекватности обеспечения конкретного человека витамином D вызывает споры в научном сообществе. Наиболее полезным и универсальным лабораторным показателем в настоящее время считается концентрация 25-гидрокси-холекальциферола в сыворотке крови[3]. Её минимальное значение, обеспечивающее оптимальное здоровье костей у большинства людей в популяции, составляет 20 нг/мл (50 нмоль/л)[1].
-
Авитаминоз витамина D играет основную роль в развитии рахита у детей. Долговременный дефицит витамина D может приводить к увеличению заболеваемости раком[10], увеличивает вероятность развития остеопороза. В последнее время опубликованы результаты исследований, увязывающих недостаток витамина с ослаблением иммунитета, повышенным риском развития сердечно-сосудистых заболеваний[5].
-
Переизбыток
Гипервитаминоз витамина D может вызывать нарушения метаболизма кальция, приводящие к гиперкальциемии и гиперкальциурии. При длительном лечении эргокальциферолом или холекальциферолом гиперкальциемия обычно обусловлена накоплением провитамина D3, но может быть вызвана одновременным избыточным потреблением пищевых продуктов, содержащих много кальция, например молочных продуктов[11].
-
Вит. F( арахидоновая, линолевая, линоленовая к-ты)
Незаменимые жирные кислоты важны для сердечно-сосудистой системы: препятствует развитию атеросклероза, улучшает кровообращение, обладает кардиопротекторным и антиаритмическим действием. Полиненасыщенные жирные кислоты уменьшают воспалительные процессы в организме, улучшают питание тканей[13]. Суточная потребность человека оценивается в 5-10 грамм[9].
Витамин F в организме требуется для следующих процессов.
Формирование мембран и стенок клеток
Из полиненасыщенных жирных кислот в организме образуется эндогенный «хороший» холестерин, являющийся основой всех клеточных стенок и оболочек любых тканей. При его недостатке развивается ломкость кровеносных сосудов, возникают геморрагические явления, ухудшается работа нервной системы.
Синтез жиров
Многие липиды, необходимые для синтетических и энергетических процессов в организме, образуются именно из витамина F, поэтому без него немыслимы процессы регенерации тканей, запасание полезных веществ, работа печени, поддержание нормального состояния кожи и волос.
Производство простагландинов
Посредством простагландинов витамин F оказывает поддержку все нервной системе, ведь именно эти вещества являются медиаторами в различных реакциях возбуждения и торможения мускулов и нервных центров.
Усвоение кальция и фосфора
И как следствие — поддержка развития и функционирования костной ткани.
Поддержка сперматогенеза
И семенная жидкость, и сами сперматозоиды для производства требуют разных жирных кислот. При их недостатке синтез половых продуктов замедляется, и могут развиваться различные нарушения в половой сфере.
Помощь иммунной системе
При участии витамина F происходит производство некоторых антител. К тому же, жирные кислоты позволяют бороться с воспалениями и уменьшать их влияние на общее состояние всего тела. При воспалениях витамин F способствует уменьшению количества гистамина в крови, что уменьшает очаг воспаления и ускоряет его снятие.
Восстановление повреждённых тканей
Особенно это заметно при открытых ранах и других повреждениях наружных покровов тела. При достаточном количестве витамина F в организме их заживление происходит значительно быстрее.
Связи же витамина F с другими веществами в организме так широки, что его недостаток отражается обычно организованно на всех системах органов.
Наиболее явными проявлениями недостатка витамина F являются различные повреждения кожных покровов. Это может быть экзема, перхоть, шелушение кожи, различные высыпания, прыщи, утолщение эпидермиса. При этом же развивается ломкость ногтей и волос, может начаться облысение.
Маленькие дети при недостатке витамина F в рационе сильно отстают в росте и психическом развитии. Параллельно у них увеличивается потребность в воде, но при этом увеличения количества выделяемой мочи не происходит, зато становится жидким стул.
У мужчин при недостатке витамина F начинаются различные сексуальные расстройства и понижается выработка спермы.
Хронический дефицит витамина F в рационе приводит к развитию нервных расстройств. Появляется депрессия, головные боли, возможно нарушение координации движений.
И главным последствием постоянного недостатка витамина являются нарушения в работе кровеносных сосудов. Их стенки становятся тонкими и ломкими, часто возникают кровоизлияния разного масштаба, ухудшается их проницаемость. Вероятность развития атеросклероза при недостатке витамина F повышается в разы.
Признаки гипервитаминоза витамина F у человека не выявляются даже при длительном поступлении избыточного количества его в организм. Чрезмерный прием может привести к увеличению веса тела. Не стоит злоупотреблять омега-3 жирными кислотами, т.к. у них есть свойство разжижать кровь и они могут быть причиной кровотечений. Гипервитаминоз витамина F проявляется болями в желудке, изжогой, кожно-аллергическими высыпаниями и связан с передозировкой ненасыщенных жирных кислот.
-
7. Процесс, начинающийся от пирувата, называется общим путем катаболизма и в свою очередь включает:
-
окислительное декарбоксилирование пирувата
-
цитратный цикл.
Окислительное декарбоксилирование пировиноградной кислоты
Суммарный результат многостадийной реакции выглядит следующим образом:
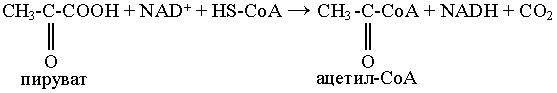
Реакция катализируется тремя ферментами, работающими в определенной последовательности и объединенными в пируватдегидрогеназный комплекс.
Цитратный цикл
Цитратный цикл (цикл Кребса, цикл трикарбоновых кислот) - это система реакций, приводящая к полному окислению двухуглеродного ацетильного фрагмента, имеющего различное происхождение. Цитратный цикл является общим конечным путем окисления белков, жиров и углеводов. Все реакции цитратного цикла, как и окислительного декарбоксилирования пирувата, локализованы в митохондриях. В ходе одного полного цикла происходит:
-
полное окисление ацетильного остатка до двух молекул СО2;
-
образование трех молекул восстановленного NAD+ и одной молекулы FADH2;
-
образование одной молекулы GTP в результате субстратного фосфорилирования.
Реакции цитратного цикла, ферменты и их характеристика приведена на рисунке:
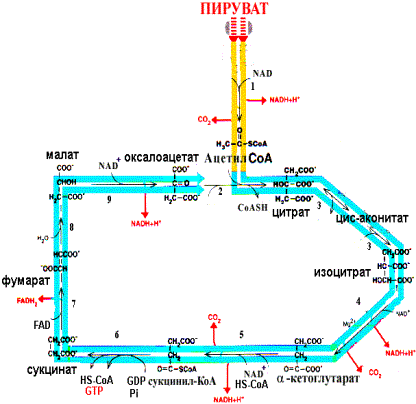
Схема цитратного цикла; ферменты: 1- пируватдегидрогеназный комплекс, 2- цитратсинтаза, 3- аконитаза, 4- изоцитратдегидрогеназа, 5- -кетоглутаратдегидрогеназный комплекс, 6- сукцинил-КоА-тиокиназа, 7- сукцинатдегидрогеназа, 8- фумараза, 9- малатдегидрогеназа
Специфические
пути катаболизма.
Простые метаболиты подвергаются
специфическим реакциям расщепления, в
результате которых образуется либо
пировиноградная кислота, либо ацетил
- СоА. Причем ацетил - СоА может образоваться
из пирувата в результате окислительного
декарбоксилирования. Могут также
образоваться другие соединения,
непосредственно включающиеся в цитратный
цикл.
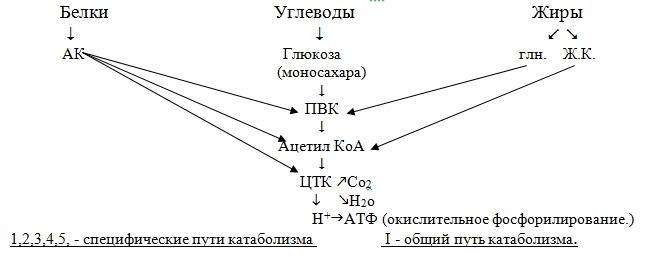
Существует четыре этапа распада У, Ж, Б: I этап - Распад полимеров до мономеров: Белки до АК, Углеводы домоносахаров, Липиды до жирных кислот и глицерина. Процесс распада в основ гидролитический, освобождающаяся при этом в небольшом количестве энергия превращается в тепло. II этап - Мономеры подвергаются дальнейшему распаду по своим специфическим путям (1, 2, 3, 4, 5, 6) в результате чего все продукты переваривания пищи превращаются в ПВК и ацетил КоА. В ПВК превращаются все моносахара, глицерин, некоторые АК. Затем путем окислительного декарбоксилирования ПВК превращается в ацетил КоА. Минуя образование ПВК в ацетил КоА превращаются жирные кислоты и некоторые АК. Далее ацетил КоА вступает в реакции окисления в лимоннокислом цикле ( цикле трикарбоновых кислот (ЦТК)) Кребса. Образование ацетил КоА и реакции ЦТК (I и II этапы) относятся к общему пути катаболизма. Некоторы АК вступают в общий путь катаболизма на промежуточных стадиях ЦТК. III этап - Окисление ацетил КоА и др. метаболитов (α-кетоглутарат, щавелевоуксусная кислота (ЩУК)) в ЦТК. Этот этап сопровождается образованием восстановленных форм НАД ∙Н2 и ФАД∙Н2 IV этап - Через дыхательную цепь происходит перенос ℮‾ от восстановленных форм НАД ∙Н2 и ФАД∙Н2 на кислород. В результате образуется конечный продукт Н2О.
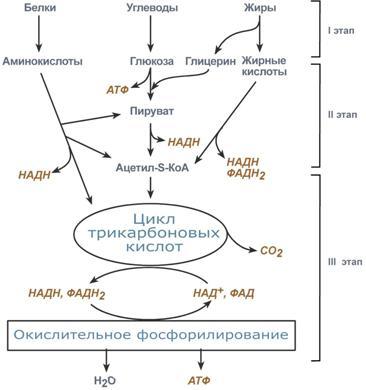
8 Вопрос
Биологическое окисление - это совокупность реакций окисления, протекающих во всех живых клетках. Оно проходит 3 способами:
1.отщепление атомов Н+
2.присоединение кислорода
3.перенос электронов
Тканевое дыхание - это разновидность биологического окисления. В процессе тканевого дыхания в организме вырабатывается АТФ.
Тканевое дыхание - это процесс расщепления органических веществ с выделением энергии в виде АТФ, что сопровождается поглощением кислорода, выделением СО2 и образованием воды.
Расщепление органических веществ в организме проходит в 3 стадии:
1 и 2 стадия – это специфические пути превращения органических веществ, Ш стадия -–общая, объдиняет все пути превращения органических веществ. В ней образуется наибольшее количество энергии.
Биологические виды энергии. Энергетические превращения в живой клетке подразделяют на две группы: локализованные в мембранах и протекающие в цитоплазме. В каждом случае для «оплаты» энергетических затрат используется своя «валюта»: в мембране это ΔμН+ или ΔμNa+, а в цитоплазме – АТФ, креатинфосфат и другие макроэргические соединения. Непосредственным источником АТФ являются процессы субстратного и окислительного фосфорилирования. Процессы субстратного фосфорилирования наблюдаются при гликолизе и на одной из стадий цикла трикарбоновых кислот (реакция сукцинил-КоА —> сукцинат). Генерация ΔμН+ и ΔμNa , используемых дляокислительного фосфорилирования, осуществляется в процессе транспорта электронов в дыхательной цепи энергосопрягающих мембран.Энергия разности потенциалов на сопрягающих мембранах может обратимо превращаться в энергию АТФ. Эти процессы катализируются Н+-АТФ-синтазой в мембранах, генерирующих протонный потенциал, или Na+-АТФ-синтазой (Na+-АТФазой) в «натриевых мембранах» алкалофиль-ных бактерий, поддерживающих ΔμNa+ [Скулачев В.П., 1989]. Cвет или энергия субстратов дыхания утилизируется ферментами фотосинтетической или дыхательной редокс-цепи (у галобактерий – бактериородопси-ном). Генерируемый потенциал используется для совершения полезной работы, в частности для образования АТФ. Будучи макроэргическим соединением, АТФ выполнняет функцию аккумулирования биологической энергии и ее последующего использования для выполнения клеточных функций. «Макроэргичность» АТФ объясняется рядом особенностей его молекулы. Это прежде всего высокая плотность зарядов, сконцентрированная в «хвосте» молекулы, обеспечивающая легкость диссоциациитерминального фосфата при водном гидролизе. Продукты этого гидролиза представляют собой АДФ и неорганический фосфат и далее – АМФ и неорганический фосфат. Это обеспечивает высокую величину свободной энергиигидролиза терминального фосфата АТФ в водной среде.
Все окислительно-восстановительные реакции, протекающие в клетках катализируются ферментами класса- оксидоредуктаза.
Типы реакций в процессах биологического окисления:
-
Реакции связанные с передачей субстратом, который окисляется(SH2), АКЦЕПТОРУ (А), водорода (протонов и электронов): SH2 + A S + AH2
Реакции такого типа- дегидрирование, а ферменты которые их катализируют- дегидрогеназы. Коферменты дегидрогеназ, которые исполняют функцию акцепторов восстановительных эквивалентов:
-никотинамид (пиридиновые) коферменты- нуклеотиды НАДФ+ и НАД+
-флавиновые коферменты- нуклеотиды ФАД и ФМН
В зависимости от химической природы акцептора, с которым взаимодействуют дегидрогеназы, реакции дегидрирования делят на классы:
-
Реакции дегидрирования, в которых акцептор- химическое соединение(R):
SH2 + R S + RH2
-
Реакции дегидрирования, в которых как акцептор используется кислород:
SH2 + O2 S + H2 O2
Ферменты, катализирующие эти реакции- аэробные дегидрогеназы, или оксидазы; в результате их образуется перекись водорода.
-
Реакции, которые происходят с передачей от субстрата к акцептору электронов:
Se– + A S + Ae–
Реакции такого типа катализируются цитохромами дыхательной цепи митохондрий.
-
Реакции, в основе которых – присоединение к субстрату, который окисляется, 1 или 2 атомов кислорода. Такие реакции- оксигеназные, ферменты- оксигеназы. В зависимости от количества атомов кислорода, оксигеназные реакции делят на:
- монооксигеназные SH + 1/2 O2 ====S–OH
- диоксигеназные S + O2===SO2
Монооксигеназные реакции катализируются цитохромом Р- 450 и лежат в основе окислительного гидроксилирования многих гидрофобных субстратов экзогенного и эндогенного происхождения ( микросомальное окисление). К диоксигеназным реакциям пренадлежат реакции переокисного окисления липидов.