Материал: Задачи по биохимии
19.
Гликолиз — это сложный ферментативный процесс расщепления глюкозы до двух молекул пирувата (аэробный гликолиз) или двух молекул лактата (анаэробный гликолиз, протекающий без потребления кислорода).
Биологическая роль гликолиза: 1. Генерирование АТФ. Гликолиз — единственный процесс в клетках, продуцирующий АТФ без потребления кислорода. Клетки, имеющие мало или не имеющие вообще митохондрий, получают АТФ только в ходе гликолиза. Значение гликолиза для эритроцитов. Гликолиз — единственный процесс, продуцирующий АТФ в эритроцитах и поддерживающий их целостность и функции. 2. Является источником углеводородных радикалов для процессов биосинтеза в клетках Уравнения реакций
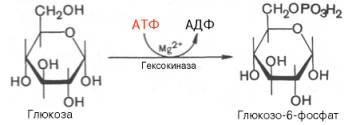
1.
2.
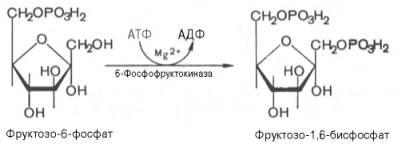
3.
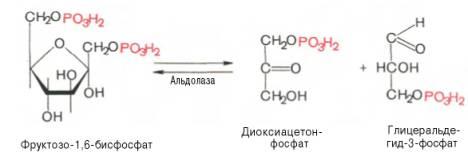
4.
5.
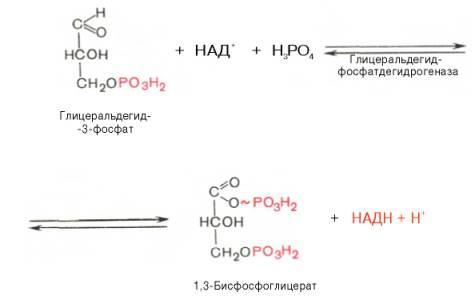
6.
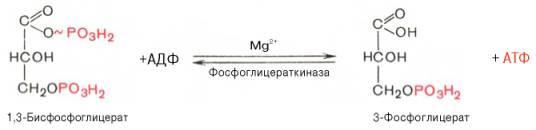
7.
8.

9.
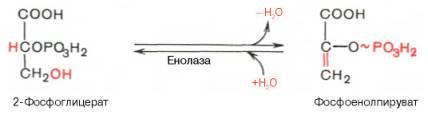
10.
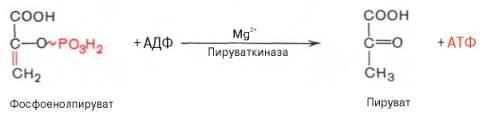
11.

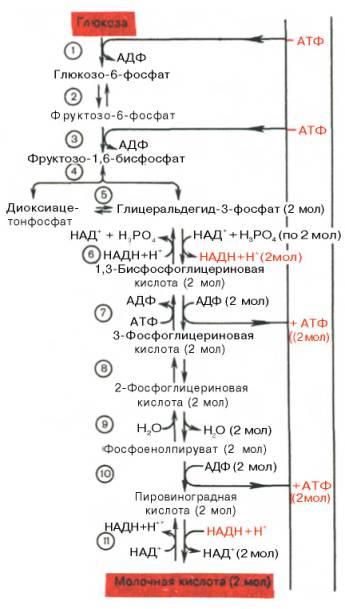
20. Биологическая роль аэробного окисления глюкозы, его основные этапы и расчет энергии окисления глюкозы в аэробных условиях.
Аэробным называется окисление биологических субстратов с выделением энергии, протекающее при использовании кислорода в качестве конечного акцептора водорода в дыхательной цепи. В качестве доноров водорода выступают восстановленные формы коферментов (НАДН, ФАДН2 и НАДФН), образующиеся в промежуточных реакциях окисления субстратов.
Аэробное дихотомическое окисление глюкозы является основным путём катаболизма глюкозы в организме человека и может происходить во всех органах и тканях. В результате этих реакций глюкоза расщепляется до СО2 и Н2О, а выделяющаяся энергия аккумулируется в АТФ.
1. Аэробный путь окисления глюкозы и его энергетика.
Аэробный путь окисления глюкозы происходит в 3 этапа:
1. окисление молекулы глюкозы до 2 молекул пирувата;
2. окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетил-КоА);
3. реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с образованием 12 АТФ.
1-ый этап. Окисление молекулы глюкозы до 2 молекул пирувата - это первые 10 реакций гликолиза. Суммарная реакция 1 этапа: Глюкоза + 2 НАД+ + 2 АДФ ^ 2 пирувата + 2 НАДН + Н+ + 2 АТФ
2-ой этап. Окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетил-КоА) происходит в матриксе митохондрий и осуществляется мультиферментным комплексом пируватдегидрогеназой. В его состав входят 3 фермента и 5 коферментов:
1. Пируватдекарбоксилаза - кофермент тиаминпирофосфат (активная форма витамина В1).
2. Дегидролипоилацетилтрансфераза - кофермента: в активном центре - липоевая кислота (витаминоподобное вещество), из матрикса митохондрий используется Коэнзим А (КоА~8Н).
3. Дигидролипоилдегидрогеназа - коферменты: в активном центре - ФАД, из матрикса митохондрий используется - НАД.
Суммарная реакция: 2 Пируват + 2 НАД+ + КоА ^ 2 ацетил-КоА + 2 НАДН + Н+
Каждый восстановленный НАД в митохондриях отдает протоны и электроны в полную ц.п.э., где образуется 2 х 3 АТФ = 6 АТФ. Таким образом, ценность второго этапа - 6 АТФ. Эти реакции происходят только в аэробных условиях!
3-ий этап. Реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с образованием 12 АТФ. Следовательно, энергетический выход третьего этапа (в расчете на молекулу глюкозы) - 2 х 12 АТФ = 24 АТФ
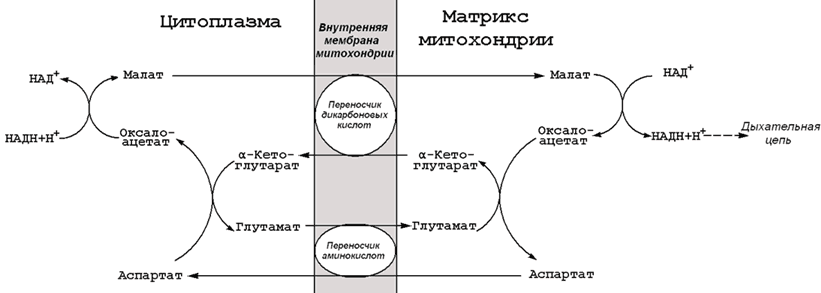
2. Челночные механизмы переноса НАДН из цитозоля в матрикс митохондрий.
Образующийся в ходе аэробного окисления каждый НАДН отдает протоны и электроны в митохондриальную цепь переноса электронов с помощью челночных механизмов (см. наглядный материал): малат-аспартатного. В случае малат-аспартатного челнока митохондриальным акцептором протонов и электронов является НАД+. При работе малат-аспартатного челнока в результате реакций окислительного фосфорилирования, сопряженного с цепью переноса электронов, образуется 3 АТФ (в полной ц.п.э.) . Следовательно, в результате первого этапа окисления глюкозы образуется 2 АТФ (7-ая и 10-ая реакции гликолиза -субстратное фосфорилирование) + 2 х [3 (или 2)] АТФ при окислении каждого НАДН в ц.п.э. = 8 (или 6) АТФ.
3. Энергетическая ценность аэробного окисления глюкозы:
1 этап - 8 (6) АТФ
2 этап - 6 АТФ
3 этап - 24 АТФ Итого: 38 (36) АТФ
(разница в 2 АТФ зависит от челнока, который переносит протоны и электроны из цитозоля от НАДН, образованного в 6-ой реакции гликолиза в митохондрии в ц.п.э.).
Аэробное окисление глюкозы является главным источником энергии для большинства клеток организма.
22
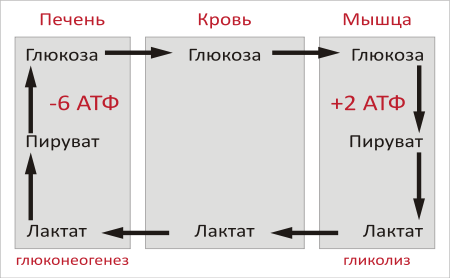
Глюкозо-лактатный цикл (цикл Кори) – это циклический процесс, объединяющий реакции глюконеогенеза и реакции анаэробного гликолиза. Глюконеогенез происходит в печени, субстратом для синтеза глюкозы является лактат, поступающий в основном из эритроцитов или мышечной ткани. В эритроцитах молочная кислота образуется непрерывно, так как для них анаэробный гликолиз является единственным способом образования энергии. В скелетных мышцах высокое накопление молочной кислоты (лактата) является следствием гликолиза при интенсивной работе. Убрать молочную кислоту можно только одним способом – превратить ее в пировиноградную кислоту. Клеточная мембрана высоко проницаема для лактата и он движется по градиенту концентрации наружу, малая часть молочной кислоты выводится с мочой, большая часть лактата крови захватывается гепатоцитами, окисляется в пировиноградную кислоту и вступает на путь глюконеогенеза. Глюкоза, образованная в печени используется самим гепатоцитом или возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена.
23.
Регуляторный «эффект Пастера» - торможение гликолиза дыханием - объясняется энергозависимой конкуренцией за АДФ и фосфат между системами фосфорилирования в дыхательной цепи(окислительное фосфорилирование) и на уровне субстрата(субстратное фосфорилирование). Хорошо известно, что факультативно анаэробные клетки, растущие в анаэробных условиях, потребляют сравнительно очень большие количества глюкозы (и образуют большие количества продуктов брожения). Если же ввести в среду кислород, то клетки начнут немедленно его поглощать и уровень потребления глюкозы резко снизится. Это снижение скорости гликолитического расщепления глюкозы с началом дыхания и носит название эффекта Пастера.
Эффект Пастера обусловлен подавлением активности фермента фосфофруктокиназы, который катализирует реакцию, лимитирующую общую скорость гликолиза, а именно фосфорилирование фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата. Фосфофруктокиназа представляет собой поливалентно регулируемый аллостерический фермент, который активируется АДФ и подавляется АТФ и цитратом. Знание аллостерических свойств фосфофруктокиназы позволяет сделать следующий вывод: если аэробно растущие дрожжевые клетки лишить кислорода и приостановить таким образом окислительное фосфорилирование, то в клетке снизится соотношение концентраций АТФ/АМФ, что приведет к повышению активности фермента и соответственно к ускорению реакции. Таким образом, снижение активности фосфофруктокиназы связано с ускорением образования АТФ и началом функционирования ЦТК при переходе к аэробному окислению глюкозы.
Регуляторный «эффект Кребтри» - торможение дыхания гликолизом - явление, обратное «эффекту Пастера», также объясняется энергозависимыми конкурентными взаимоотношениями систем окислительного и субстратного фосфорилирования за АДФ и фосфат. Одна из точек зрения состоит в том, что эффект Кребтри обусловлен активацией гликолиза высокими концентрациями глюкозы, что приводит к избытку продуктов гликолиза, которые, главным образом в виде ацетата, экскретируются в среду. Другая точка зрения заключается в том, что
можно моделировать, применяя довольно низкие (миллимолярные) концентрации глюкозы, регистрируя при этом явление «дыхательного контроля» у бактерий. Обе точки зрения сходятся в одном - в основе механизма эффекта Кребтри лежит регуляторная способность факультативных анаэробов модулировать в широких пределах поток через гликолиз, чтобы компенсировать при необходимости нефункционирующий ЦТК усилением субстратного фосфорилирования и по той же причине иметь механизм сброса избытка продуктов гликолиза при анаэробиозе.
24.
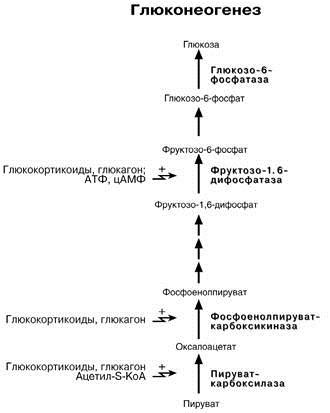
Открытие пути прямого окисления углеводов, или, как его называют,пентозофосфатного цикла, принадлежит О. Варбургу, Ф. Липману, Ф. Дикенсу и В.А. Энгельгарду. Расхождение путей окисления углеводов – классического (цикл трикарбоновых кислот, или цикл Кребса) и пентозофосфатного – начинается со стадии образования гексозомонофосфата. Если глюкозо-6-фосфат изомеризуется во фруктозо-6-фосфат, который фосфорилируется второй раз и превращается во фруктозо-1,6-бисфосфат, то в этом случае дальнейший распад углеводов происходит по обычному гликолитическому пути с образованием пировиноградной кислоты, которая, окисляясь до ацетил-КоА, затем «сгорает» в цикле Кребса.
Если второго фосфорилирования гексозо-6-монофосфата не происходит, то фосфорилированная глюкоза может подвергаться прямому окислению до фосфопентоз. В норме доля пентозофосфатного пути в количественном превращении глюкозы обычно невелика, варьирует у разных организмов и зависит от типа ткани и ее функционального состояния.
У млекопитающих активность пентозофосфатного цикла относительно высока впечени, надпочечниках, эмбриональной ткани и молочной железе в период лактации. Значение этого пути в обмене веществ велико. Он поставляет восстановленный НАДФН, необходимый для биосинтеза жирных кислот,холестерина и т.д. За счет пентозофосфатного цикла примерно на 50% покрывается потребность организма в НАДФН.
Другая функция пентозофосфатного цикла заключается в том, что он поставляет пентозофосфаты для синтеза нуклеиновых кислот и многихкоферментов. При ряде патологических состояний удельный вес пенто-зофосфатного пути окисления глюкозы возрастает. Механизм реакцийпентозофосфатного цикла достаточно расшифрован.
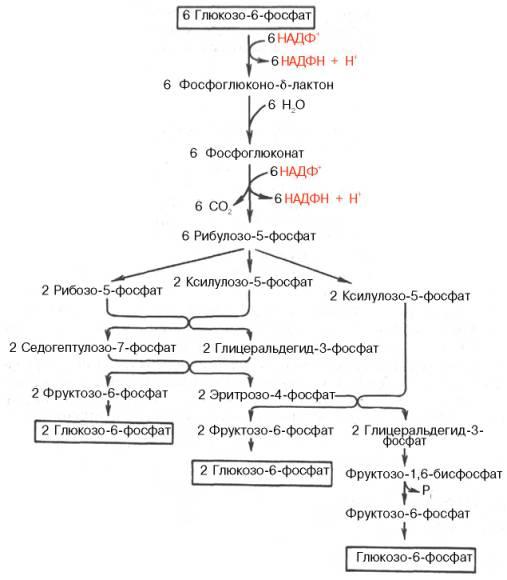
Пентозофосфатный цикл начинается с окисления глюкозо-6-фосфата и последующего окислительногодекарбоксилирования продукта (в результате от гексозофосфата отщепляется первый атом углерода). Это первая, так называемая окислительная, стадия пентозофосфатного цикла. Вторая стадия включает неокислительные превращения пентозофосфатов с образованием исходного глюкозо-6-фосфата (рис. 10.12). Реакции пен-тозофосфатного цикла протекают в цитозоле клетки.
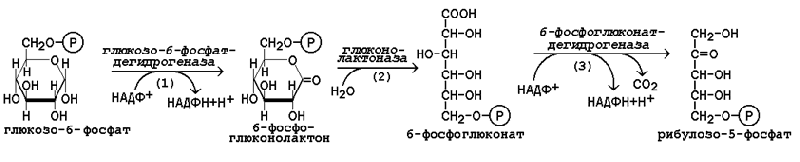
Первая реакция – дегидрирование глюкозо-6-фосфата при участии фермента глюкозо-6-фосфатдегидрогеназы икофермента НАДФ+. Образовавшийся в ходе реакции 6-фосфоглюконо-δ-лактон – соединение нестабильное и с большой скоростью гидролизуется либо спонтанно, либо с помощью фермента 6-фосфоглюконолактоназы с образованием 6-фос-фоглюконовой кислоты (6-фосфоглюконат):
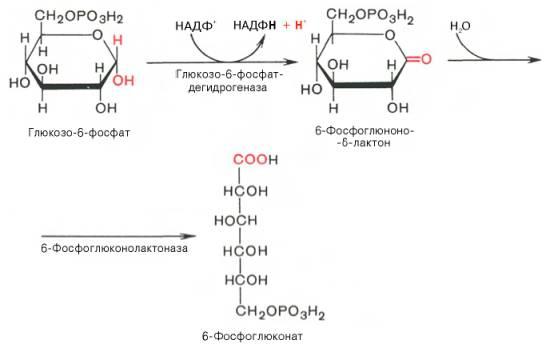
Во второй – окислительной – реакции, катализируемой 6-фосфоглюко-натдегидрогеназой (декарбоксилирующей), 6-фосфоглюконат дегидрируется и декарбоксилируется. В результате образуется фосфорилированная кетопентоза – D-рибулозо-5-фосфат и еще 1 молекула НАДФН:
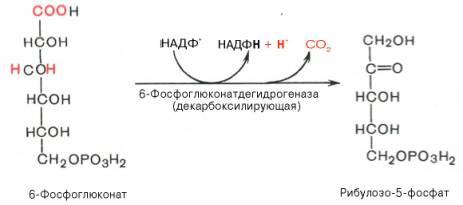
Под действием соответствующей эпимеразы из рибулозо-5-фосфата может образоваться другая фосфопентоза – ксилулозо-5-фосфат. Кроме того, рибулозо-5-фосфат под влиянием особой изомеразы легко превращается в рибозо-5-фосфат. Между этими формами пентозофосфатов устанавливается состояние подвижного равновесия:
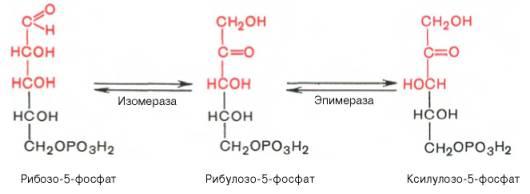
При определенных условиях пентозофосфатный путь на этом этапе может быть завершен. Однако при других условиях наступает так называемый неокислительный этап (стадия) пентозофосфатного цикла. Реакции этого этапа не связаны с использованием кислорода и протекают в анаэробных условиях. При этом образуются вещества, характерные для первой стадии гликолиза (фруктозо-6-фосфат, фруктозо-1,6-бисфосфат, фосфотрио-зы), а другие – специфические для пентозофосфатного пути (седогептулозо-7-фосфат, пентозо-5-фосфаты, эритрозо-4-фосфат).
Основными реакциями неокислительной стадии пентозофосфатного цикла являются транскетолазная и трансальдолазная. Эти реакции катализируют превращение изомерных пентозо-5-фосфатов:
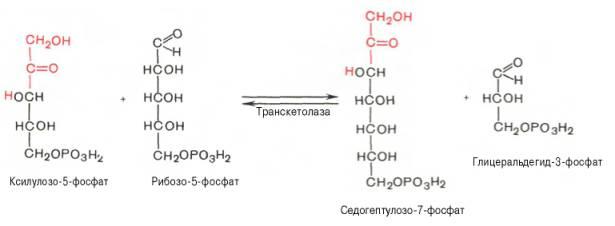
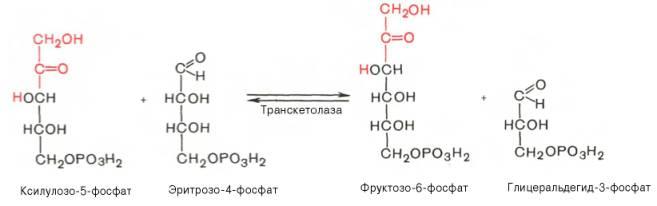
Коферментом в транскетолазной реакции служит ТПФ, играющий роль промежуточного переносчика гликольальдегидной группы от ксилулозо-5-фосфата к рибозо-5-фосфату. В результате образуется семиуглеродныймоносахарид седогептулозо-7-фосфат и глицеральдегид-3-фосфат.
Транскетолазная реакция в пентозном цикле встречается дважды, второй раз – при образовании фруктозо-6-фосфата и триозофосфата в результате взаимодействия второй молекулы ксилулозо-5-фосфата с эритрозо-4-фосфатом:
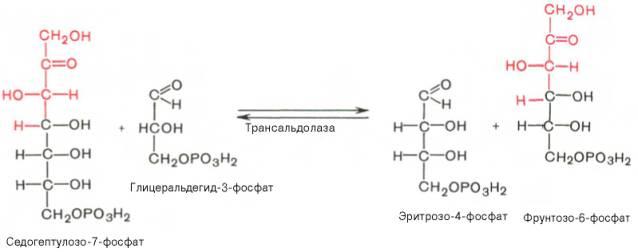
Фермент трансальдолаза катализирует перенос остатка диоксиацетона (но не свободного диоксиацетона) от седогептулозо-7-фосфата на гли-церальдегид-3-фосфат:
 Шесть молекул глюкозо-6-фосфата,
вступая в пентозофосфатный
цикл,
образуют 6 молекул рибулозо-5-фосфата
и 6молекул СО2,
после чего из 6 молекул рибулозо-5-фосфата
снова регенерируется 5 молекул глюко-зо-6-фосфата
(см. рис. 10.12). Однако это не означает,
что молекула глюкозо-6-фосфата,
вступающая в цикл, полностью окисляется.
Все 6 молекул СО2 образуются
из С-1-атомов 6 молекул глюкозо-6-фосфата.
Шесть молекул глюкозо-6-фосфата,
вступая в пентозофосфатный
цикл,
образуют 6 молекул рибулозо-5-фосфата
и 6молекул СО2,
после чего из 6 молекул рибулозо-5-фосфата
снова регенерируется 5 молекул глюко-зо-6-фосфата
(см. рис. 10.12). Однако это не означает,
что молекула глюкозо-6-фосфата,
вступающая в цикл, полностью окисляется.
Все 6 молекул СО2 образуются
из С-1-атомов 6 молекул глюкозо-6-фосфата.
Валовое уравнение окислительной и неокислительной стадий пенто-зофосфатного цикла можно представить в следующем виде:
![]() или
или
![]()
Образовавшийся НАДФН используется в цитозоле на восстановительные синтезы и, как правило, не участвует в окислительном фосфори-лировании, протекающем в митохондриях.
В последние годы появились работы, которые дают основание предполагать, что в некоторых тканях схема пентозофосфатного превращения углеводов сложнее, чем это представлено на рис. 10.12. Согласно этой более полной схеме пентозофосфатного пути, первые этапы превращения совпадают с прежней схемой, однако после первой транскетолазной реакции начинаются некоторые отклонения (рис. 10.13).
Считают, что пентозофосфатный путь и гликолиз, протекающие в цитозоле, взаимосвязаны и способны переключаться друг на друга в зависимости от соотношения концентраций промежуточных продуктов, образовавшихся в клетке
Биологическая роль Как отмечалось выше, пентозофосфатный путь имеется у животных, растений и микроорганизмов. У всех клеток этот путь служит для образования восстановленного NADPH, который используется как донор водорода в реакциях восстановления и гидроксилирования[en], а также обеспечивает клетки рибозо-5-фосфатом[13]. Хотя NADPH образуется также при окислении малата до пирувата и углекислого газа, а также при дегидрировании изоцитрата, в большинстве случаев потребности клеток в восстановительных эквивалентах удовлетворяются именно за счёт пентозофосфатного пути[3]. Впрочем, в некоторых случаях образование рибозо-5-фосфата является единственным назначением пентозофосфатного пути[4]. Рибозо-5-фосфат служит предшественником 5-фосфорибозил-1-пирофосфата (PRPP), который участвует в биосинтезе нуклеотидов и нуклеиновых кислот, аминокислот гистидина и триптофана. Другой интермедиат пентозофосфатного пути, эритрозо-4-фосфат, конденсируясь сфосфоенолпируватом, даёт начало общей части пути биосинтеза триптофана, фенилаланина и тирозина[14].
Пентозофосфатный путь может функционировать в печени, жировой ткани, молочной железе при лактации, семенниках[3], коре надпочечников, эритроцитах. В этих тканях и органах активно протекают реакции гидроксилирования и восстановления, например, при синтезе жирных кислот[en], холестерола, обезвреживания ксенобиотиков в печени и активных форм кислорода в эритроцитах и других тканях, поэтому у них велика потребность в восстановительных эквивалентах, в том числе,
25.
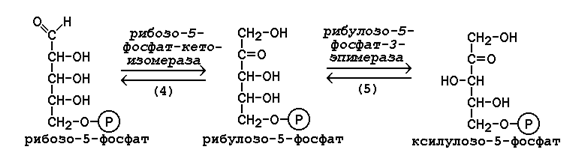
![]()
![]()
Посредством пентозофосфатного пути может происходить полное окисление глюкозо-6-фосфата до шести молекул СО2. Все эти молекулы образуются из С-1-атомов шести молекул глюкозо-6-фосфата, а из образовавшихся при этом шести молекул рибулозо-5-фосфата снова регенерируются пять молекул глюкозо-6-фосфата:
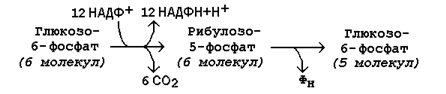
![]()
Таким образом, полное окисление 1 молекулы глюкозы в пентозофосфатном пути сопровождается восстановлением 12 молекул НАДФ.