Материал: Задачи по биохимии
Пантотеновая кислота участвует в метаболизме жирных кислот. Она нормализует липидный обмен и активирует окислительно-восстановительные процессы в организме.
Пантотеновая кислота (витамин В5) оказывает мощный репаративный эффект на слизистые. Повышенные дозы пантотеновой кислоты, наоборот, тормозит секреторную функцию желудка. Также пантотеновая кислота стимулирует перистальтику кишечника.[1]
Пантотеновая кислота оказывает значительное гиполипидемическое действие, обусловленное, по-видимому, ингибированием биосинтеза основных классов липидов, формирующих в печени липопротеины низкой и очень низкой плотности.
Дефицит: Недостаток пантотеновой кислоты в организме приводит к нарушениям обмена веществ, на основе которых развиваются дерматиты, депигментация и потеря волос, шерсти или перьев, прекращение роста, истощение, изменения в надпочечниках и нервной системе, а также расстройства координации движений, функций сердца и почек, желудка, кишечника.
При недостатке в организме пантотеновой кислоты в желудке образуется избыток соляной кислоты, что может стать причиной развития язвенно-эрозийных заболеваний желудочно-кишечного тракта. [1]
Причиной дефицита витамина могут быть малое содержание в пище белков, жиров, витамина С, витаминов группы В, заболевания тонкого кишечника с синдромом мальабсорбции, а также длительное применение многих антибиотиков и сульфаниламидов.
Симптомы гиповитаминоза:
-
усталость
-
депрессия
-
расстройство сна
-
повышенная утомляемость
-
головные боли
-
тошнота
-
мышечные боли
-
жжение, покалывание, онемение пальцев ног
-
жгучие, мучительные боли в нижних конечностях, преимущественно по ночам
-
покраснение кожи стоп
-
диспепсические расстройства
-
язвы 12-перстной кишки
При пантотеновой недостаточности снижается сопротивляемость организма к инфекции, часто возникают острые респираторные заболевания.
-
Биотин(вит.Н, В7)
Входит в состав ферментов, регулирующих белковый и жировой баланс, обладает высокой активностью. Участвует в синтезе глюкокиназы — фермента, регулирующего обмен сахаров.
Является коферментом различных ферментов, в том числе и транскарбоксилаз. Участвует в синтезе пуриновых нуклеотидов. Является источником серы, которая принимает участие в синтезе коллагена[1]. С участием биотина протекают реакции активирования и переноса СО2.
Дефицит: При недостатке биотина наблюдаются:
-
поражения кожи рук и ног
-
сухость и нездоровый оттенок кожи
-
бледный гладкий язык
-
сонливость, депрессия
-
болезненность и слабость мышц
-
гипотония
-
высокий уровень холестерина и сахара в крови
-
анемия
-
потеря аппетита и тошнота
-
ухудшение состояния волос
-
замедляется рост.
-
А,Е,К,Д3,F
-
Вит. А(ретинол)
Ретиналь является компонентом родопсина — основного зрительного пигмента. В форме ретиноевой кислоты витамин стимулирует рост и развитие. Ретинол является структурным компонентом клеточных мембран, обеспечивает антиоксидантную защиту организма. Дефицит: Недостаток витамина A может произойти из-за первичной или вторичной недостаточности. Первичный дефицит витамина A возникает среди детей и взрослых, которые не потребляют нужное количество каротиноидов из фруктов и овощей или витамина A из животных и молочных продуктов. Ранний отказ от грудного вскармливания может также увеличить риск дефицита витамина A[21].
Вторичный дефицит витамина A связан с хроническим нарушением всасывания липидов, желчеобразования и хроническому воздействию окислителей, таких как сигаретный дым, и хронический алкоголизм. Витамин A — жирорастворимый витамин, и зависит от мицеллярной солюбилизации для дисперсии в тонком кишечнике, что приводит к плохому использованию витамина A при низком содержании жиров. Дефицит цинка также может ухудшать всасывание, транспорт и метаболизм витамина A, поскольку он необходим для синтеза транспортных белков и в качестве кофактора для превращения ретинола в ретиналь. В недоедающих популяциях общее низкое употребление витамина A и цинка усиливают выраженность дефицита витамина A. Исследование, проведённое в Буркина-Фасо, показало значительное снижение заболеваемости малярией среди детей младшего возраста при использовании комбинации витамина A и цинка[22].
Наиболее ранним симптомом гиповитаминоза является куриная слепота — резкое снижение темновой адаптации. Характерными являются поражения эпителиальных тканей: кожи (фолликулярный гиперкератоз), слизистых оболочек кишечника (вплоть до образования язв), бронхов (частые бронхиты), мочеполовой системы (лёгкое инфицирование). Дерматиты сопровождаются патологической пролиферацией, кератинизацией и слущиванием эпителия. Десквамация эпителия слёзных каналов может приводить к их закупорке и уменьшению смачивания роговицы глаза — она высыхает (ксерофтальмия) и размягчается (кератомаляция) с образованием язв и «бельма». Поражение роговицы может развиваться очень быстро, так как нарушение защитных свойств эпителия приводит к вторичным инфекциям. При недостатке витамина также начинается отставание в росте[2].
Надлежащее обеспечение, но не избыток витамина A, особенно важен для беременных и кормящих женщин для нормального развития плода и в грудное молоко[21][23]. Недостатки не могут быть компенсированы послеродовой добавкой[24].
Метаболическая активность витамина ингибируется при употреблении алкоголя во время беременности и характеризуется такой же тератогенностью, что и материнский дефицит витамина A[25].
Гипервитаминоз
Доза витамина A 25 000 МЕ/кг вызывает острое отравление, а ежедневное употребление дозы 4000 МЕ/кг в течение 6—15 месяцев вызывает хроническое отравление[26].
Для гипервитаминоза характерны следующие симптомы: воспаление роговицы глаза, потеря аппетита, тошнота, увеличение печени, боли в суставах. Хроническое отравление витамином A наблюдается при регулярном употреблении высоких доз витамина, больших количеств рыбьего жира[2]. При избыточном употреблении каротинов возможно пожелтение ладоней, подошв стоп и слизистых, однако даже в крайних случаях симптомов интоксикации не наблюдается. У животных более чем 100-кратное увеличение дозировки β-каротина приводило к прооксидантному эффекту. Этого не наблюдалось в присутствии витаминов E и C, которые защищают молекулу от окислительной деструкции[2].
Случаи острого отравления со смертельным исходом возможны при употреблении в пищу печени акулы, белого медведя, морских животных, хаски[2][27][28][29]. Европейцы начали сталкиваться с этим по крайней мере с 1597 года, когда Геррит де Веер и его люди серьёзно заболели после того, как съели печень белого медведя[30].
Острая форма отравления проявляется в виде судорог, паралича. При хронической форме передозировки повышается внутричерепное давление, что сопровождается головной болью, тошнотой, рвотой. Одновременно возникает отёчность жёлтого пятна и связанные с этим нарушения зрения. Проявляются геморрагии, а также признаки гепато- и нефротоксического действия больших доз витамина A. Могут происходить спонтанные переломы костей[31]. Избыток витамина A может вызвать врождённые дефекты и поэтому не должен превышать рекомендуемой дневной нормы[32].
Для ликвидации гипервитаминоза назначают маннит, снижающий внутричерепное давление и ликвидирующий симптомы менингизма, глюкокортикоиды, ускоряющие метаболизм витамина в печени и стабилизирующие мембраны лизосом в печени и почках. Витамин E тоже стабилизирует клеточные мембраны. Большие дозы витамина A нельзя назначать беременным (особенно на ранних стадиях беременности) и даже за полгода до беременности, так как очень велика опасность возникновения тератогенного эффекта[4].
-
Вит. Е(токол)
-
Витамин Е поступает в желудочно-кишечный тракт в составе масел, гидролиз которых липазой и эстеразой приводит к высвобождению витамина. Затем он всасывается и в составе хиломикронов поступает в лимфатическую систему, а затем в кровь. В печени витамин связывается с токоферолсвязывающими белками, причем наибольшим сродством обладает RRR-α-токоферол. Другие токоферолы выделяются из печени с желчными кислотами. Эти белки доставляют витамин в кровь в составе ЛПОНП. В плазме крови происходит обмен токоферолом между ЛПОНП и другими липопротеинами крови. Обмен между фракциями липопротеинов (особенно между ЛПНП и ЛПВП) и эритроцитами обеспечивает равновесие концентраций токоферола в крови[1].
-
Витамин поступает в экстрапеченочные ткани в составе ЛПНП, которые захватываются соответствующими рецепторами. Кроме такого рецепторно-опосредованного механизма имеется и другой, зависящий от активности липопротеинлипазы: фермент высвобождает токоферол из хиломикронов и ЛПОНП, после чего витамин поступает в ткани путем пассивной диффузии. Благодаря пассивной диффузии через клеточную мембрану концентрация RRR-a-токоферола увеличивается во всех тканях организма, особенно в мозге. Структурная организация фосфолипидов в клеточных мембранах способна узнавать хиральную форму RRR-a-токоферола, благодаря чему витамин задерживается в мембране, где и выполняет свою функцию (синтетические токоферолы в составе мембраны обеспечивают меньшую её защиту от оксидативного стресса)[1].
-
Не всосавшиеся в кишечнике токоферолы выводятся с калом. Продукты метаболизма витамина — токофериновая кислота и её водорастворимые глюкурониды — выводятся с мочой.[1]
Витамин Е является универсальным протектором клеточных мембран от окислительного повреждения. Он занимает такое положение в мембране, которое препятствует контакту кислорода с ненасыщенными липидами мембран (образование гидрофобных комплексов). Это защищает биомембраны от их перекисной деструкции. Антиоксидантные свойства токоферола обусловлены также способностью подвижного гидроксила хроманового ядра его молекулы непосредственно взаимодействовать со свободными радикалами кислорода (О2·, НО·, НО2·), свободными радикалами ненасыщенных жирных кислот (RO·, RO2·) и перекисями жирных кислот. Мембраностабилизируюшее действие витамина проявляется и в его свойстве предохранять от окисления SH-группы мембранных белков. Его антиоксидантное действие заключается также в способности защищать от окисления двойные связи в молекулах каротина и витамина А. Витамин Е (совместно с аскорбатом) способствует включению селена в состав активного центра глутатионпероксидазы, тем самым он активизирует ферментативную антиоксидантную защиту (глутатионпероксидаза обезвреживает гидропероксиды липидов)[1].
Токоферол является не только антиоксидантом, но и актигипоксантом, что объясняется его способностью стабилизировать митохондриальную мембрану и экономить потребление кислорода клетками. Следует отметить, что из всех клеточных органелл митохондрии наиболее чувствительны к повреждению, так как в них содержится больше всего легко окисляющихся ненасыщенных липидов. Вследствие мембраностабилизируюшего эффекта витамина Е в митохондриях увеличивается сопряженность окислительного фосфорилирования, образование АТФ и креатинфосфата. Важно также отметить, что витамин контролирует биосинтез убихинона — компонента дыхательной цепи и главного антиоксиданта митохондрий[1].
Окисленная форма витамина может реагировать с донорами водорода (например, с аскорбиновой кислотой) и таким образом вновь переходит в восстановленную форму[7].
Так как окисленные формы в организме восстанавливаются, то их обычно не находят in vivo. In vitro были найдены следующие продукты окисления[7]:
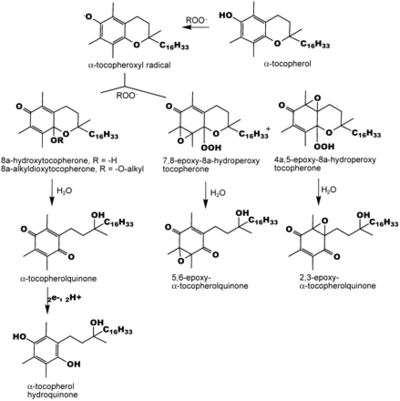
Токотриенолы проявляют сильные нейропротекторные, антиоксидантные свойства, снижают риск заболевания раком. Микромолярные количества токотриенолов уменьшают активность 3-гидрокси-3-метилглютарил-кофермент А редуктазы, отвечающей за синтез холестерина, таким образом снижая его уровень в организме[8].
Токоферол контролирует синтез нуклеиновых кислот (на уровне транскрипции), К0 энзима Q, миозиновой АТФ-азы (необходимой для сокращения) кальциевой АТФ-азы (необходимой для захвата кальция в саркоплазматический ретикулум при расслаблении), каталазы и пероксидазы (участвующих в ликвидации перекисей), а также гема (таким образом увеличивая эритропоэз), входящего в состав цитохромов (P-450, цитохром-С-редуктазы), гемоглобина и миоглобина. Под его влиянием происходит синтез следующих белков: коллагена в подкожной клетчатке и костях, сократительных белков в скелетных, гладких мышцах и миокарде, белков слизистых оболочек и плаценты, ферментов печени, креатинфосфокиназы, вазопрессиназы и гонадотропных гормонов[1][9].
Витамин Е обладает способностью угнетать активность фосфолипазы А2 лизосом, разрушающей фосфолипиды мембран. Повреждение мембран лизосом приводит к выходу в цитозоль протеолитических ферментов, которые и повреждают клетку.
Витамин Е является эффективным иммуномодулятором, способствующим укреплению иммунозащитных сил организма[1].
Гиповитаминоз
Недостаточность токоферола — весьма распространенное явление, особенно у людей, проживающих на загрязненных радионуклидами территориях, а также подвергающихся воздействию химических токсикантов. Глубокий гиповитаминоз встречается редко — преимущественно у недоношенных детей (проявляется гемолитической анемией)[1].
При Е-витаминной недостаточности наблюдается частичный гемолиз эритроцитов, в них снижается активность ферментов антиоксидантной защиты. Повышение проницаемости мембран всех клеток и субклеточных структур, накопление в них продуктов ПОЛ — главное проявление гиповитаминоза. Именно этим обстоятельством объясняется разнообразие симптомов недостаточности токоферола — от мышечной дистрофии и бесплодия вплоть до некроза печени и размягчения участков мозга, особенно мозжечка. Увеличение активности выходящих из поврежденных тканей ферментов в сыворотке крови (креатинфосфокиназы, аланинаминотрансферазы и других) и увеличение содержания в ней продуктов ПОЛ наблюдается уже на ранних стадиях Е-гиповитаминоза[1].
При недостатке витамина Е у младенцев и маленьких детей с мальабсорбцией атаксия протекает намного быстрее, чем у взрослых. Это означает, что нервной системе необходимо достаточное количество витамина для нормального развития[7].
Дефицит витамина Е в организме сопровождается снижением содержания иммуноглобулинов Е. После его введения нормализуется численность Т- и В-лимфоцитов в периферической крови и восстанавливается функциональная активность Т-клеток[1].
Гипервитаминоз
Витамин нетоксичен при значительных (10—20-кратных к суточной потребности) и длительных превышениях его дозировки, что обусловлено ограничением способности специфических токоферолсвязывающих белков печени включать витамин в состав ЛПОНП. Его избыток выводится из организма с желчью. В некоторых случаях длительный прием мегадоз токоферола (более 1 г в сутки) может привести к гипертриглицеридемии и повышению кровяного давления[1].
Основные осложнения при гипервитаминозе связаны с[9]:
-
чрезмерным угнетением свободнорадикальных реакций в нейтрофилах и других фагоцитах (нарушение переваривания захваченных микроорганизмов, что может проявится сепсисом у очень недоношенных детей);
-
прямым токсическим действием на нейтрофилы, тромбоциты, эпителий кишечника, клетки печени и почек;
-
угнетением активности витамин K-зависимой карбоксилазы.
Возможная клиника отравления α-токоферолом: сепсис, некротизирующий энтероколит, гепатомегалия, гипербилирубинемия (более 20 мг/дл), азотемия (более 40 мг/дл), тромбоцитопения (менее 50-60 тыс./мкл), симптомы почечной недостаточности, кровоизлияния в сетчатую оболочку глаз или мозг, асцит[9].
При внутривенном введении витамина Е на месте инъекции возникает отёк, эритрема, кальцификация мягких тканей[9].
-
Вит.К(филлохинон)
-
Дефицит витамина К может развиваться из-за нарушения усвоения пищи в кишечнике (такие как закупорка желчного протока), из-за терапевтического или случайного всасывания антагонистов витамина K, или, очень редко, дефицитом витамина К в рационе. В результате приобретенного дефицита витамина К Gla-радикалы формируются не полностью, вследствие чего Gla-белки не в полной мере выполняют свои функции. Вышеописанные факторы могут привести к следующему: обильные внутренние кровоизлияния, окостенение хрящей, серьёзная деформация развивающихся костей или отложения солей на стенках артериальных сосудов.
-
В то же время переизбыток витамина К способствует увеличению тромбоцитов, увеличению вязкости крови, и как следствие крайне нежелательно употребление продуктов богатых витамином К для больных варикозом, тромбофлебитом, некоторыми видами мигреней, людям с повышенным уровнем холестерина (так как формирование тромбов начинается с утолщения артериальной стенки вследствие формирования холестериновой бляшки).
Витамин K участвует в карбоксилировании остатков глутаминовой кислоты в полипептидных цепях некоторых белков. В результате такого ферментативного процесса происходит превращение остатков глутаминовой кислоты в остатки гамма-карбоксилглутаминовой кислоты (сокращенно Gla-радикалы). Остатки гамма-карбоксилглутаминовой кислоты (Gla-радикалы), благодаря двум свободным карбоксильным группам, участвуют в связывании кальция. Gla-радикалы играют важную роль в биологической активности всех известных Gla-белков.[1]