Материал: Виробництво вінілхлориду
2.2 Класична схема виробництва вінілхлориду
.2.1 Опис та технологічна схема виробництва вінілхлориду
Отримання вінілхлориду з ацетилену
Теоретичні основи процесу
Розповсюдженим способом отримання винилхлориду є гідрохлорування ацетилену. Реакція приєднання хлориду воднюдо ацетилену типова для з’єднань з потрійним зв’язком.
≡ CH + HCl→CH2 = CHCl, ∆H°298=
−112,4 кДж/моль
За своєю екзотермічністю вона майже в два рази перевершує реакцію гідрохлорування олефінів.
Реакція гідрохлорування ацетилену в
певному ступені оборотна. Разом з тим при помірних температурах рівновага майже
повністю зміщена в право, так як константи рівноваги дорівнюють 8∙104 при
200°С і 7∙102 при 300°С. До того ж приєднання HCl до ацетилену протікає
послідовно - спочятку утворюється вінілхлорид, а потім 1,1-дихлоретан:
![]()
Отже, для отримання вінілхлориду необхідно використовувати селективні каталізатори, які прискорюють лише першу реакцію. Найбільш прийнятними для цього стали солі Hg(II) та Cu(I). При використанні сулеми HgCl2 також сильно прискорюється реакція гідратації ацетилену з отриманням ацетальдегіду (реакція Кучерова) У звязку з цим процес проводять в газовій фазі при температурах 150-200 °С, використовуючи попередньо осушені реагенти. При цьому утворюється невелика кількість ацетальдегіду та 1,1-дихлоретану (≈1%). Разом з цим можна розглянути можливість сумісного отримання ацетальдегіду та вінілхлориду. В цьому випадку необхідно проводити процес в рідкій фазі[8].
Для рідкофазного гідрохлорування більш придатна сіль Cu(I), так як вона слабо дезактивується і погано прискорює взаємодію ацетилену з водою. (Отже, цей каталізатор не підходить для сумісного отримання вінілхлориду та ацетальдегіду).
Каталітична система являє
собою розчин Cu2Cl2 і хлориду алюмінію в хлороводневій кислоті. Однак на цьому
каталізаторі протікає також димеризація ацетилену з утворенням вінілацетилену:
![]()
Для придушення цієї реакції необхідно використовувати концентровану HCl. У звязку з цим в ходу процесу в каталізаторний розчин безперервно подається HCl для компенсації його витрати на гідрохлорування.
Каталітична дія вказаних
каталізаторів пояснюється утворенням кординаційних комплексів, в яких ацетилен
активується і взаємодіє з хлор-аніонами. При цьому має місце перехідний стан з
метал-вуглицевим зв’язком або маталорганічним звязком, який швидко
розкладається кислотою:
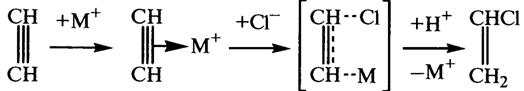
Утворення вінілхлориду в газовій фазі описується наступним кінетичним рівнянням:
= K∙PC2H2∙ PHCl /
(1+bPHCl)
Технологічне оформлення процесу
Як було показано раніше, промисловий процес виробництва вінілхлориду з ацетилену и хлориду водню являє собою гетерогенно-каталітичний процес. Каталізатором в даному випадку служить HgCl2 [1,0 %(мас.)], нанесений на активоване вугілля. Процес проводять на стаціонарному каталізаторі при температурі 160-180 °С в трубчастому реакторі. Суміш ацетилену і хлориду водню пропускають через трубки, заповнені каталізатором. При цьому хлорид водню береться в невеликому надлишку (5-10 %) до ацетилену, що збільшує конверсію останнього. Вихідні речовини піддають попередній осушці з ціллю зменшення утворення ацетальдегіду і корозії апаратури. При 160-180 °С відбувається винос сулеми (за рахунок її летальності), хоча і незначний. У звязку з цим поступово активність каталізатора знажується, і тоді з ціллю підтримання його активності підвищують температуру до 200-220 °С[7].
Технологічна схема виробництва, що розглядається представлена на кресленні 1. очищений ацетилен проходить вогнеперешкоджувач 1, потім холодильник-конденсатор 2 і колону 5, в якій відбувається осушка ацетилену. В конденсаторі осушка відбувається за рахунок конденсації вологи розсолом, а в колоні - твердим NaOH. Зконденсована волога відділяється в сепараторі 3.
Осушений ацетилен змішують з сухим хлоридом водню в змішувачі 4 і поступає в трубний простір реактора 6. В міжтрубний простір подається водний конденсат (для відводу тепла), з якого утворюється пар. Для відводу тепла можна використовувати і органічний теплоносій.
Конверсія ацетилену складає 97-98 %. Реакційні гази містять 93 % вінілхлориду, 5 % HCl, 1,0 - 2,5 % С2Н2 і по 0,3 % ацетальдегіду і 1,1-дихлоретану. Крім того, в ньому містяться сліди віднесеної сулеми. Тому газ охолоджується в холодильнику 7, потім проходить через скрубери 8-10, в яких він очищується від HCl ті від сулеми. Скрубер 8 орошується розбавленою хлороводневою кислотою (20 %), скрубер 9 - водою і скрубер 10 - циркулюючим лугом. Після цього газ осушується в розсольному холодильнику-конденсаторі і зтискується компресором 12 до 0,7- 0,8 МПа. Далі продукти підлягають розділенню на ректифікаційних колонах 13 і 14.
В колоні 13 відділяється вінілхлорид
разом з легкокиплячими компонентами від важкої фракції, головним чином від
1,1-дихлоретану. Далі в колоні 14 відбувається відділення легколетючих
компонентів (ацетилену, ацетальдегіду) від вінілхлориду. Отже, в даному випадку
пропонований варіант на основі другого заданого розділення, має свої переваги
та недоліки. Зокрема, до переваг відноситься те, що в колоні 14 температура
буде нижчою, ніж в аналогічній колоні варіанту, основаного на першому
розділенні (рис 2.2.). А це приводить до менших втрат вінілхлориду за рахунок
термополімеризації.
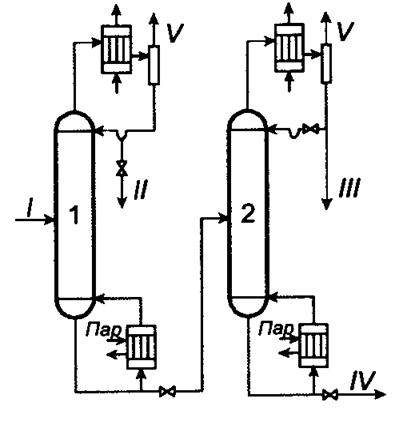
Рис. 2.2 - Технологічна схема
виділення вінілхлориду, заснована на першому заданому розділенні: 1,2 -
ректифікаційні колони; I - вінілхлорид сирець; II - Легкокипляча фракція; III -
вінілхлорид; IV - важкокипляча фракція; V - гази
Принципи в технології гідрохлорування ацетилену
Технологія гідрохлорування ацетиленуз отриманням вінілхлориду відноситься до неперервних і має одну стадію за хімічною складовою. В якості вихідної сировини використовують доступні суміші хлороводню та ацетилену. Хоча останній і дорожче етилену в даний час, але при сприятливій коньюктурі ринку або в регіонах з дешевою електроенергією розглядаєма технологія може бути конкурентноспроможною з етиленовими способами виробництва вінілхлориду. Процес відноситься до високоефективних, володіючи високими конверсіями за один прохід, селективність і продуктивністю. В ряді випадків, оскільки при тих же умовах при наявності в реакційній масі води утворюється ацетальдегід, процес можна спрямувати на одночасне отримання двох товарних продуктів - вінілхлориду та ацетальдегіду. При цьому технологію можна розглядати як сумісну. Високі конверсії реагентів за один прохід роблять застосування рециркуляції недоцільною. З реакційної суміші повністю виділяють вінілхлорид, легко і важкокиплячі фракції, як правила не утилізуються, а піддаються вогневому знешкодженню або глибокому хлоруванню з отриманням чотирихлористого вуглецю. Тому технологія не володіє повнотою використання рідких і твердих відходів[9].
З точки зору реалізації принципів
розробки технології з низьким енергоспоживанням і повнотою використання енергії
системи технологія гідрохлорування ацетилену достатньо досконала. В
розглядаємому випадку в реакційній підсистемі виробляється високопотенційне
тепло. Його наступна утилізація дозволяє забезпечити енергоресурсами підсистему
ректифікаційного розділення або суміжні виробництва. Отримання вінілхлориду
гідрохлоруванням ацетилену неможна віднести до технологій з мінімальними
витратами води, оскільки відходящі гази містять залишкову кількість хлороводню,
що робить необхідним організацію промивки продуктів водою і розчином лугу. Це
приводить до утворення значної кількості водно-солевих стоків і розбавленої
соляної кислоти. Використання реакційних апаратів великої одиничної потужності
утруднено, так як кожухотрубні реактори мають обмеження, звязані з труднощами
розподілення потоку сировини при високих виробництвах, а використання апаратів
з киплячим шаром неможливе через високу токсичність каталітичної системи
(стирання каталізатора в киплячому шарі призводить до підвищення виносу
токсичного каталітичного пилу)[8,10].
2.2.2 Технологічно проблемні стадії виробництва вінілхлориду
Варіант представлений на кресленні 1, має суттєві недоліки: двічі при відповідних флегмових числах випаровується вінілхлорид ( по першому заданому розділенні один раз), що приводить до великих енергетичних затрат. Продуктовий вінілхлорид відбирають з кубу, тому він забруднений важкими домішками (по першому заданому розділенні виводиться у вигляді дистилята).
Якщо роздивитись вцілому пропонований варіант виробництва вінілхлориду, то він на даному етапіне перспективний в наслідок використання дуже токсичного каталізатора і дороговартісного вихідного реагента - ацетилену. Однак, якщо вклад ацетилену в собівартість можна компенсувати технологічними рішеннями, то каталізатор потребує принципової заміни. В даний час групою вчених МДУТХТ ім. М.В. Ломоносова під керівництвом О.Н. Темкина розроблений процес гідрохлорування ацетилену з використанням металкомплексних каталізаторів на основі хлоридів RhCl3 (органічний розчинник). Метод був випробуваний на стендовій установці МНОП «Синтез». При проведенні процесу при 150 °С вдається досягнути повної конверсії ацетилену і продуктивністю 3 моль/л.год. Селективність процесу вище 99 %.
Використання такої каталітичної
системи дозволяє виключити з виробництва токсичні солі ртуті та, при
благополучних цінах на ацетилен, реалізувати промислове виробництво
вінілхлориду[14].
2.3 Новітня схема виробництва вінілхлориду
Вінілхлорид з етану
Компанією Monsanto в 1977 році був запропонований одностадійний метод отримання вінілхлориду з виходом 85 % з етану під дією суміші хлороводню і кисню при температурі 400-650 °С в присутності каталізатора (галогеніду міді і фосфату калію):
- CH3+HCl + O2→CH2=CHCl+2H2O
Фірма Lummus-Armstrong Transcat в 1965-1967 роках розробила технологію прямого оксихлорування в присутності хлориду міді(І) і отримала назву Transcat Process. Етан взаємодіє з Cl2 в присутності розплавів солей міді. На першій стадії одночасно йдуть реакції хлорування, оксихлорування та дегідрохлорування.
Хімія процесу:
CH3+Cl2→CH3CH2Cl+HClCH2Cl→H2C=CH2+HClC=CH2+Cl2→ClCH2-CH2Cl-CH2Cl→H2C=CHCl+HCl
CuCl+O2→2Cu2OCl2OCl2+2HCl→2CuCl+Cl2+H2O
Процес проходив при 450-550 °С і тиску 1 МПа. При цьому мідь(ІІ) відновлюється до міді(І). Друга стадія процесу - окиснення каталізатора сумішю HCl і повітря. Ступінь перетворення етану близько 30 %, селективність менше 40 %. Побічними продуктами реакції являються хлоретан, 1,1-дихлоретан, вінілдихлорид та інші галогенпохідні[15].Vinyls Corp. (Брюссель) пустила пілотну установку потужністю 1 тис.тон на рік в Німечині по виробництву вінілхлориду безпосередньо з етану. Процес йде в одну стадію (собівартість знижується на 30 %). Етан взаємодіє з хлоруючим агентом і киснем при температурі нижче 500 °С. Хлорувальний агент - HCl, Cl2 і дихлоретилен. Селективність процесу вище 90 %. Повідомлялось, що такі процеси можна проводити в твердому розчині каталізатора, який являє собою кристалічну решітку α-Al2-O3, в якій атоми алюмінію заміщені на атоми залаза та іони інших металів.
Цей метод в результаті був оптимізований компанією ІСІ, яка знизила температурний діапазон проведення синтезу і запропонувала інший каталізатор.
Одним з останніх розроблених методів виробництва ( 2005 ) є спосіб отримання вініхлоріду взаємодією метилхлориду і метиленхлориду в газовій фазі при температурі 300-500 °С, тиску від 0,1 до 1 МПа, в присутності каталізаторів (активний оксид або фосфат алюмінію, алюмосилікати, хлорид цинку з оксидом алюмінію).
Всі перераховані способи отримання
вінілхлориду або не були реалізовані в промисловості, чи не вийшли зі стадії
експериментального виробництва, тому технологічні схеми виробництв не
надаються.
РОЗДІЛ 3. ТЕХНОЛОГІЧНІ ПРОЦЕСИ ОХОРОНИ ДОВКІЛЛЯ ПРИ ВИРОБНИЦТВІ ВІНІЛХЛОРИДУ
3.1 Аналіз потоків відходів
В навколишньому середовищі вінілхлорид зявляється виключно внаслідок його викидів під час виробництва та переробки. За оцінкою спеціалістів, більше 99 % викидів вінілхлориду залишається в повітрі, де відбувається його фотохімічна деградація під дією гидроксил-радикалів; при цьому період його напіврозпаду складає 18 годин ( за іншими даними, цей час складає 2.2-2,7 днів).
З поверхні грунту вінілхлорид швидко випаровується, але може мігрувати в глиб нього через грунтові води. В рослинах і тваринах не накопичується. В грунті і воді вінілхлорид піддається аеробній біодеградації (переважно до СО2) під дією мікроорганізмів, наприклад роду Мікобактерії (Mycobacterium); біорозпад в грунтових водах може нести і анаеробний характер, до того ж його продуктами є метан, етилен, вуглекислий газ та вода.
Дослідження показують, що в грунті і
воді під дією мікроорганізмів вінілхлорид розкладається на 30 % протягом 40
днів і на 99 % протягом 108 днів[13].
3.1.1 Газові відходи
Вінілхлорид є як і сировиною, так і основним газовим відходом при виробництві полівінілхлориду. В даному розділі представлені схеми очистки газів від вінілхлориду, саме у виробництві полівінілхлориду.
Уловлювання ВХ з абгазів проводять в декілька стадій. Велика частина незаполімеризованого вінілхлориду міститься в абгазах, здувних з реакторів і колони дегазації. Всі висококонцентровані здувки направляються в Газгольдер мокрого типу (рис.3.1.), що служить накопичувачем газоподібного ВХ і буфером, що виключає нерівномірність работи установки рекуперації.
Газова суміш з газгольдера надходить
в одноступінчатий поршневий компресор, який стискає її до тиску 0,6 МПа, а
потім охолоджуєть у водяному холодильнику до 5-10°С.
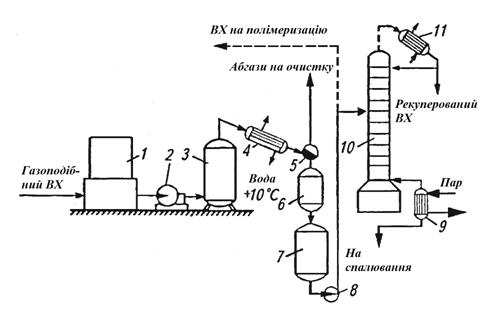
Рис. 3.1 - Принципова технологічна
схема виділення вінілхлориду з висококонцентрованих абгазів: 1 - газгольдер; 2
- компресор; 3 - урівнююча ємність; 4 - холодильник-конденсатор; 5 -
фазороздільник; 6 - осушувач; 7 - збірник сирцю ВХ; 8 - насос; 9 - кипятильник;
10 - колона дистиляції; 11 - конденсатор
Зріджений ВХ через фазораз дільник надходить на осушку твердим лугом і далі на ректифікацію для очищення від домішок, що утворюються в процесі полімеризації. Враховуючи незначну кількість домішок і відносно невелику частку незаполімеризованого ВХ, вловлений ВХ після осушки іноді направляють безпосередньо на полімеризацію, підмішуючи його до основного потоку сировини[13].
Незконденсований ВХ, що залишився в
абгазі, подають на наступний ступінь очищення, змішуючи його з іншими
середньоконцентрованими абгазами виробництва ПВХ. У виробництвах ПВХ для
очищення середньо- і малоконцентрованих абгазів від вінілхлориду застосовують
двоступеневі конденсаційно-адсорбційні установки. На рис. 3.2. представлена
принципова технологічна схема конденсаційно-адсорбційної установки вловлення і
регенерації вінілхлориду із абгазів та вентвикидів.
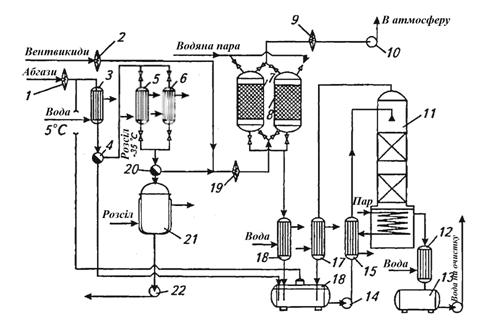
Рис. 3.2 - Принципова технологічна
схема вловлення та регенерації вінілхлориду конденсаційно-адсорбційним методом:
1, 2, 9, 19 - вогнеперешкоджувачі; 3, 17, 18 - конденсатори водяних парів; 4,
20 - фазорозділювачі; 5, 6 - конденсатори ВХ; 7, 8 - адсорбери; 10 -
вентилятор; 11 - десорбер; 12 - холодильник; 13, 16 - збірники конденсату; 14,
22 - насоси; 15 - теплообмінник; 21 - збірник рідкого ВХ
Абгази, що містять до 40 % ВХ, з температурою до 40 °С і відносною вологістю 100 % надходять в конденсатор 3, охолоджуваний захолодженою до 5 °С водою. Пари вологи конденсуються, і конденсат, що містить в розчиненому стані 0,2 % ВХ, відводиться до збірки конденсата 16, а осушений газ поступає з фазорозділювача 4 в один з конденсаторів - 5 або 6, охолоджуваних розсолом при температурі біля -35 °С. Конденсатори працюють почерзі: один - в робочому режимі, а другий - в режимі танення льоду, який утворюється при конденсації залишків вологи з абгазів. Зконденсований вінілхлорид надходить в збірник 21, звідки повертається на стадію полімеризації[13].
Частково очищений в цих умовах абгаз містить до 170 г/м3. Він змішується з вентвикидами, які містять близько 15 г/м3 ВХ, і надходить на адсорбційну ступінь очищення, що складається з двох почергово працюючих вугільних адсорберів, в яких очищується і викидається в атмосферу; ступінь очищення досягає 99,9 %. Вловлений ВХ вилучається з адсорбенту в режимі регенерації гострою водяною парою. Паровий конденсат зливається в збірник 16, а газоподібний ВХ повертається на вхід установки, де змішується з поступаючими на очищення абгазами. Для вилучення з конденсату розчиненого ВХ слугує десорбер 11. Конденсат після обробки парою охолоджується і відводиться на стадію очищення стічних вод, а газоподібний ВХ повертається на вхід установки. Принципова технологічна схема установки для вловлення вінілхлориду з абгазів абсорбційно-адсорбційним методом наведена на рис.3.3.