Материал: Васильева ИА ТЕРМОДИНАМИКА характеристические функции
dAп.в.=dA-d(p∙V). |
(1-36) |
Рассмотрим термодинамический |
процесс перехода системы из |
состояния 1 в состояние 2. Тогда для конечного термодинамического процесса между состояниями 1 и 2 выражение (1-36) преобразуется к виду
∫2 dAп.в. = ∫2 dA − ∫2 d(p V ),
1 |
1 |
1 |
|
иначе |
|
|
|
Ап.в.=А-(p2 |
∙V2-p1∙V1). |
(1-37) |
|
Видим, что полезная внешняя работа системы является в общем случае |
|||
частью работы расширения системы и отличается от нее на величину |
|
||
p2∙V2-p1∙V1=Aпроталк., |
(1-38) |
||
которую обычно называют работой проталкивания. Работа проталкивания,
согласно (1-38), является функцией состояния и всецело характеризуется конечным (p2, V2) и начальным (p1, V1) механическими состояниями системы, а не траекторией, т.е. не зависит от процесса. По физическому смыслу работа проталкивания соответствует той части полной работы системы, которая неизбежно расходуется в процессе на противодействие среды и теряется бесполезно (превращаясь в теплоту) с точки зрения её практического, полезного применения. В то же время разница Ап.в.=(А-Апр) образует именно ту часть работы системы, которую можно использовать в практических целях, т.е. располагать ею с точки зрения полезного применения. По этой причине полезную внешнюю работу иногда называют располагаемой работой.
Приведенные рассуждения и выводы можно дополнить графиком (см. рис. 1.1), иллюстрирующим особенности равновесного расширения газа в цилиндре с поршнем. При переходе системы из состояния 1 в состояние 2
полная работа расширения составляетA = ∫2 p dV и численно совпадает с
1
площадью V1-1-2-V2 (вертикальная штриховка).
Часть этой работы неизбежно расходуется на изменение механического состояния среды
Aпр = ∫2 d(p V )= p2 V2 − p1 V1 .
1
Эти непроизводительные потери не зависят от вида процесса, а определяются только конечным и начальным состоянием системы (а соответственно и среды).
15
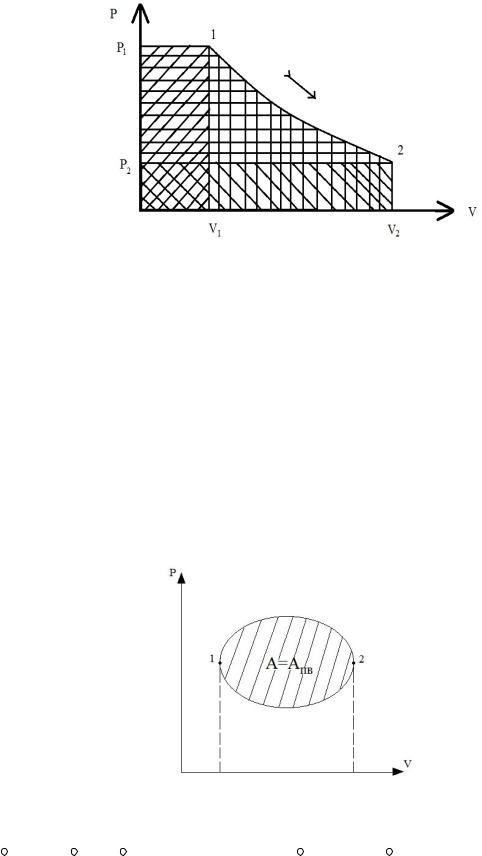
Рис.1.1. Особенности расширения газа в цилиндре с поршнем
Полезная внешняя работа системыAп.в. = −∫2 V dp отражается на
1
графике площадью р1-1-2-р2 (горизонтальная штриховка).
Из графика видно, что в зависимости от соотношения площадей работа проталкивания может быть как положительной, так и отрицательной.
Здесь же пока уместно обратить внимание на то, как трансформируется взаимосвязь между А, Ап.в. и Апр в замкнутых, круговых термодинамических процессах (циклах).
Если система участвует в круговом процессе (рис. 1-2), то соотношение dAп.в.=dA-d(p∙V) после интегрирования по замкнутому контуру дает нам следующий важный результат
Рис. 1.2. Круговой процесс
∫dAп.в. = ∫dA −∫d(p V )→ Aпц.в. = Aц ,∫ p dV = −∫V dp, |
(1-39) |
т.к. в  ∫d(p V ) подынтегральная функция имеет вид полного дифференциала, поэтому
∫d(p V ) подынтегральная функция имеет вид полного дифференциала, поэтому
16
 ∫d(p V )= 0 .
∫d(p V )= 0 .
Таким образом, в круговых процессах полная работа системы равна полезной внешней работе, хотя на отдельных участках цикла такое совпадение отсутствует.
1.6. Уравнения Гиббса – Гельмгольца
Характеристические функции U, I, F, Ф, как мы уже установили, функционально связаны между собой
I=U+p∙V; F=U-T∙S; Ф=U+p∙V-T∙S=I-T∙S.
Следовательно, если известна хотя бы одна из этих функций, то через нее могут быть найдены все другие.
Воспользуемся, в частности, выражением для свободной энергии
F=U-T∙S
и учтем, что для энтропии справедливо тождество
|
∂F |
S = − |
. |
|
∂T V |
Таким образом, внутренняя энергия системы выражается через свободную энергию уравнением
|
∂F |
,или |
|
|
|
F =U +T |
|
|
|
||
|
∂T V |
|
. |
(1-40) |
|
U = F −T |
∂F |
|
|||
|
|
||||
|
|
|
|
||
|
∂T |
V |
|
|
Аналогичным образом удается связать энтальпию системы со свободной энтальпией.
Имеем I=Ф+T∙S, |
|
∂Ф |
и |
|
S = − |
|
|||
|
|
|
∂T p |
|
|
∂Ф |
|
|
(1-41) |
I = Ф−T |
. |
|
|
|
|
∂T p |
|
|
|
Наконец, таким же способом можно выразить через свободную |
||||
энтальпию внутреннюю энергию системы |
||||
|
∂Ф |
|
∂Ф |
(1-42) |
U = Ф−T |
|
− p |
. |
|
|
∂T p |
|
∂p T |
|
Полученные уравнения играют в термодинамике важную роль и носят название уравнений Гиббса-Гельмгольца. Важность этих уравнений обусловлена тем, что свободная энергия и свободная энтальпия более доступны прямым измерениям, чем внутренняя энергия и энтальпия.
17

1.7. Дифференциальные соотношения
Воспользуемся установленными выше свойствами характеристических функции и попытаемся с их помощью изучить количественные связи между термодинамическими параметрами системы.
Рассмотрим интересующую нас проблему в общем её аспекте, на примере системе с n степенями свободы, и разберем последовательно все возможные варианты сопряжения этой системы со средой.
1. Сопряжение по зарядам.
Мы уже знаем, что роль характеристической функции в этом случае играет внутренняя энергия, её частные производные соответственно равны:
∂∂ψk inv = Pk , k=1, 2, …, n.
Выберем из n потенциалов два произвольных k-тый и j-тый
|
|
∂U |
|
|
∂U |
|
|
Pk |
|
|
|
|
|||
|
|
||||||
= |
|
|
и Pj = |
|
|
||
|
|
∂ k inv |
|
∂ j inv |
|||
Заряды lk и lj здесь выступают как независимые, поэтому мы можем перейти к смешанным частным производным для Pk и Рj:
Продифференцируем Pk по lj и Pj по lk
|
∂P |
|
∂2U |
|
|
|
∂P |
|
∂2 |
|
|
||||||||
|
|
k |
|
= |
|
|
|
|
|
; |
|
j |
|
= |
|
|
U |
|
. |
∂ |
|
∂ |
|
∂ |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
∂ |
|
|
|
∂ |
|
∂ |
|
|
|||
|
|
j inv |
|
|
k |
|
j inv |
|
|
k inv |
|
|
k |
|
j inv |
||||
Стоящие справа вторые частные производные от внутренней энергии, вследствие независимости lk и lj, не зависят от последовательности дифференцирования и совпадают между собой.
Следовательно,
|
∂P |
|
∂Pj |
|
||
|
k |
|
|
|
|
(1-43) |
|
|
|||||
|
|
|
= |
|
. |
|
|
∂ j inv |
|
∂ k inv |
|
||
Причем справедливо и обратное соотношение |
|
|||||
|
∂ |
j |
|
|
∂ |
|
|
|
|
|
|
|
|
k |
. |
(1-44) |
|
∂P |
|
|
||||||
|
|
|
= |
∂P |
||||
|
k inv |
|
|
j |
inv |
|
||
Индексы у P, l в числителе и знаменателе относятся к разным степеням свободы.
Получены чрезвычайно важные дифференциальные соотношения (назовем их соотношениями первого типа).
Главным признаком этого типа соотношений является то, что частные производные берутся при фиксированных прочих зарядах системы.
18
И еще одно предварительное замечание. В найденных соотношениях оказались связанными разнородные по степени свободы физические параметры системы.
2. Сопряжение по потенциалам.
Основным свойством соответствующей характеристической функции, как известно, является такое
|
|
|
∂ψ |
, k=1, 2, …, n. |
|
|
|
= − |
|
|
|
|
|
||||
|
k |
|
∂P |
|
|
|
|
|
k P |
|
|
|
|
|
|
inv |
|
Как и в предыдущем случае, выберем два произвольных заряда, k-тый и j-тый и осуществим их смешанное дифференцирование по Рk и Рj
|
|
|
2 |
ψ |
|
|
|
∂ |
j |
|
|
2 |
ψ |
|
|
|
∂ k |
= − |
∂ |
|
|
; |
|
|
= − |
∂ |
|
. |
|||
|
|
|
∂P |
|
|
|
|
||||||||
|
∂P |
|
∂P ∂P |
|
|
|
|
∂P ∂P |
|||||||
|
j P |
|
k |
|
j P |
|
k Pinv |
|
k |
|
j P |
||||
|
inv |
|
|
|
|
inv |
|
|
|
|
|
|
|
|
inv |
Следовательно, как и прежде приходим к важному равенству |
|||||||||||||||
|
∂ |
|
|
|
|
|
∂ |
j |
|
|
|
|
|
|
k |
|
|
|
|
|
, |
(1-45) |
|||
|
|
|
∂P |
|
|
|||||||
|
∂P |
= |
|
|
|
|
||||||
|
|
j P |
|
|
|
k Pinv |
|
|
||||
|
|
|
inv |
|
|
|
|
|
|
|
|
|
которое справедливо и в обращенной форме: |
|
|||||||||||
|
∂P |
|
|
∂Pj |
|
|
|
|
||||
|
|
k |
|
= |
|
|
|
|
|
|
(1-46) |
|
|
|
|
|
|
∂ k |
|
. |
|||||
|
∂ j P |
|
|
|
Pinv |
|
|
|||||
|
|
|
inv |
|
|
|
|
|
|
|
|
|
Равенства |
|
(1-45) |
и (1-46) принято называть |
дифференциальными |
||||||||
соотношениями второго типа. Их главная особенность: частные производные берутся при фиксированных прочих потенциалах.
Индексы у Р и l в числителе и знаменателе относятся к разным степеням свободы.
3. Смешанное сопряжение.
При смешанном сопряжении выполняются соотношения
|
|
|
∂ψ |
|
|
|
|
∂ψ |
|
|||
|
|
= − |
|
|
|
|
, P |
= |
|
|
. |
|
|
|
|
|
∂ |
|
|||||||
|
k |
|
∂P Pinv |
j |
|
|
Pinv |
|||||
|
|
|
k |
|
inv |
|
|
|
j |
inv |
||
Напомним, |
|
что |
при |
|
таком сопряжении в качестве независимых |
|||||||
выступает часть потенциалов (Рk, где k = 1, 2,…, n) и часть координат (lj, где j
= r+1,…, n).
Образуем, как и прежде, из этих равенств вторые смешанные
производные |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
∂ |
|
|
|
∂2ψ |
|
|
|
|
∂P |
|
|
|
|
∂ |
2 |
ψ |
|
|
|||
|
|
k |
|
= − |
|
|
|
|
|
|
; |
j |
|
|
|
= |
|
. |
||||
∂ |
|
∂ |
|
∂P |
|
∂P |
|
|
∂ |
|
∂P |
|||||||||||
|
Pinv |
|
j |
Pinv |
|
Pinv |
|
j |
Pinv |
|||||||||||||
|
|
j |
inv |
|
|
|
k |
inv |
|
k |
|
inv |
|
|
|
k |
inv |
|||||
Сопоставляя оба выражения, приходим к соотношению
19