Материал: Углеродные наноматериалы, производство, свойства, применение (Мищенко), 2008, c.172
Углеродсодержащий газ |
|
Газ на утилизацию |
2 |
3 |
4 |
1 |
|
|
5 |
|
|
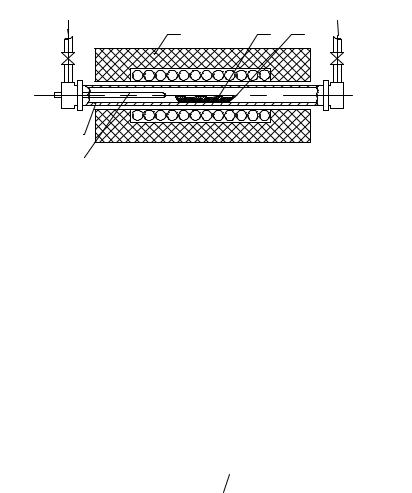
Рис. 1.25. Схема горизонтального периодического ректора для пиролиза углеродсодержащих газов:
1 – кварцевая труба; 2 – изоляция; печь с резистивным обогревом; 3 – слой катализатора; 4 – лодочка; 5 – термопара
Нагретую до температуры пиролиза (550…1000 °С) реакционную зону продувают инертным газом (Ar, He), затем подают углеродсодержащий газ. Движущийся вдоль катализатора газ диффундирует сквозь его слой и сорбируется на поверхности активных центров (металл), где протекает ряд последовательных химических реакций, конечными продуктами которых являются углерод и водород.
Продуктами данного процесса, который классифицируется как газофазное химическое осаждение (ГФХО) или CDVпроцесс, являются УНМ – ОУНТ, МУНТ и УНВ.
Термодинамика процессов ГФХО весьма полно представлена в обзорах [113 – 115]. В общих чертах термодинамические соотношения, описывающие процессы образования УНМ при разложении, к примеру метана CH4 , можно представить следующим образом [46, 116].
Общая реакция образования из газообразного метана CH4 (г) графита – стандартного состояния твердого углерода C (т):
|
CH4 (г) = C (т) + 2H2 (г) K1, |
||||||
где K1 – |
константа равновесия реакции. |
|
|
|
|
|
|
Активность метана аг можно определить соотношением |
|
|
|||||
|
a |
г |
= K |
1 |
(P |
P 2 |
), |
|
|
|
CH4 |
H |
2 |
||
где PCH4 |
– равновесное давление метана; PH2 – равновесное давление водорода. Однако в результате происходит образование не |
||||||
более термодинамически стабильного графита, а метастабильной формы углерода – углеродного волокна. Поэтому, принимая С (т) = С (в) K2, энергию образования Гиббса Gв для углеродного волокна и активность ав = exp (Gв / RT), получаем условие, при котором образование волокна термодинамически разрешено: аг > ав (г – графит, т – твердый углерод, в – волокно).
В условиях проведения процесса (рис. 1.23) обычно нет термодинамических запретов на образование кристаллических углеродных отложений и ход процесса определяют кинетические закономерности [113].
Свойства пиролитических УНМ отличаются от свойств наноструктур, полученных дуговым и абляционным способом. Как правило, они содержат большее количество дефектов, имеют широкий диапазон рассеяния диаметральных размеров и длины, большие межслоевые расстояния.
Поэтому, несмотря на кажущуюся простоту организации пиролизные способы синтеза требуют тщательного подхода к выбору используемых параметров, изучению и оптимизации кинетических характеристик процесса. В этом случае удается получить УНМ с высокими качественными показателями, в том числе и ОУНТ.
Анализ литературных источников позволяет установить основные параметры, влияющие на структуру, морфологию и свойства пиролитических УНМ. Это:
−состав газовой смеси;
−природа каталитических систем;
−температура и давление;
−продолжительность процесса;
−условия осуществления фазовых превращений, определяемых конструкцией реактора.
Для получения УНМ данным способом наиболее часто используют диспропорционирование монооксида углерода [117
– 121], разложение: метана [122 – 132], бутана [133], этилена [121, 134 – 136], пропилена [137], ацетилена [138 – 143].
Практически все авторы обосновывают выбор того или иного газового реагента, подчеркивая его достоинства. Повидимому, следует согласиться с мнением авторов [118], что химическая природа используемого газа существенного влияния на морфологию наноуглеродных отложений не оказывает.
Подчеркивается, к примеру, кинетическая стабильность метана, что вместе с тем требует повышения температуры пиролиза, в особенности для получения качественных нанотрубок. Использование CO приводит к получению трубок с меньшим (< 20 нм) диаметром, вместе с тем сложно представить создание экологически чистых производств в присутствии в качестве сырья CO.
При создании условий для получения УНМ в значительных количествах следует принять во внимание, что связь производительности и качества получаемого материала в зависимости от вида газового сырья проявляется кинетикой процесса. Немаловажным является также доступность сырья и безопасность производства.
Для прикладных нужд важно добиться минимального присутствия в продукте аморфного углерода, с этой целью применяют разбавление углеводорода водородом [144 – 146].

С целью пассивации активных каталитических частиц, препятствующей их закоксовыванию и потере активности, применяют также аммиак [147], а для увеличения выхода УНМ добавляют CO [136, 145].
Важнейшим компонентом пиролитического способа синтеза УНМ является природа каталитической системы. При этом следует учитывать не только состав, но и способ его приготовления и нанесения на подложку.
Круг используемых для получения УНМ пиролизом углеводо-родов катализаторов достаточно обширен [115]. В основ-
ном используются металлы 3d-группы – железо [119, 122, 123, 125, 126, 130, 139, 148 – 151], никель [118, 124, 139, 140, 146, 152], кобальт [138, 139, 153 – 157] – и их бинарные смеси и сплавы с другими металлами: Co / Fe [156], Fe / Mo [121, 129, 158],
Co / Mo [159, 160], Fe/Cu [134].
Использование бинарных составов может привести к повышению эффективности процесса роста УНМ. Так, в работах [159, 160] получали качественные многослойные нанотрубки при каталитическом разложении C2H2 на частицах Co + Mo, нанесенных на Y-цеолиты. Хорошие результаты были получены при использовании катализатора Fe / Mo [129] и метана с температурой пиролиза 680 °C.
Для эффективного роста нанотрубок необходимо, чтобы активные центры катализаторной массы имели малые размеры. Использование высокодисперсных порошков с микрометрическими размерами, достижимыми путем механического диспергирования, представляется малоэффективным. В работе [161] применяли порошок Ni с размером частиц 3 мкм при пиролизе бензола и температуре до 900 °C.
Было получено некоторое количество МУНМ с числом слоев до 65 и диаметром < 100 нм. Вместе с тем наблюдалось спекание частиц Ni и, как следствие, низкий выход (гС / гkt) целевого продукта.
Поэтому при синтезе катализаторов используют различные носители, применяя при этом методы соосаждения, импрегнирования, нанесения суспензий на подложку, термическое разложение и др. В качестве носителей используют нелетучие оксиды и гидроксиды металлов (Mg, Ca, Al, La, Ti, Y, Zr) [149, 156, 157, 162], цеолиты [159, 160], селикогели, пористый Si,
алюмогель и др. [46]. Роль носителей – предотвращение спекания металлических частиц катализатора, обеспечение их равномерного распределения в катализаторной массе, промотирующее воздействие на пиролиз.
Выбор носителя определяется рядом факторов, главный из которых – уровень сложности удаления носителя из УНМ по окончании процесса синтеза. В этом смысле весьма привлекателен оксид магния MgO, легко удаляемый из продукта кислотной обработкой [46, 124].
Труднодостижимая однородность распределения активных частиц катализатора в носителе может быть достигнута применением золь-гель-методов приготовления. Например, в работе [150] катализатор на основе железа готовили путем гидролиза тетраэтилсилоксана в водном растворе нитрата железа. Последующий отжиг при 450 °С и давлении 10–2 торр позволил получить частицы SiO2 с однородными порами, занятыми наночастицами FeO. Хорошим носителем может являться пористый кремний, содержащий после электрохимического травления микропоры (< 2 нм), но он достаточно сложно затем удаляется из УНМ.
Принципиально важное значение имеют природа и состав катализаторов пиролиза углеводородов. Именно они в значительной мере определяют температуру и давление при проведении процессов, характер получаемых наноуглеродных трубок (табл. 1.3 и 1.4).
1.3. Состав и условия применения бинарных порошкообразных катализаторов Ме – Мо/носитель (А) при термическом активировании процесса получения УНТ [27]
А |
|
Ме : Мо : А, моль Ме : Мо |
|
Условия процесса |
|
|
|
Продукты |
||||
|
|
|
|
|
|
|
|
|||||
|
Исходные вещества |
|
t, °С |
|
Р, атм |
|
||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Со : Мо |
|
|
|
|
|
|
МgО |
|
(0…5) : (5…0) : 95 |
|
|
СН4 (20 %) – Н2 |
|
1000 |
|
1,0 |
|
Т-МУНТ, УНВ |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||
МgО |
|
5 |
: 1 : 94 |
|
|
СН4 (20 %) – Н2 |
|
1000 |
|
1,0 |
|
Т-МУНТ, УНВ |
МgО |
|
2,5 |
: 2,5 : 95 |
|
|
С2Н2 (10 %) – Н2 |
|
800 |
|
1,0 |
|
ОУНТ |
МgО |
|
|
1 : 4 |
|
|
СО (100 %) |
|
700 |
|
1,0 |
|
ОУНТ |
SiO2 |
|
0,5 |
: 1,5 : 98 |
|
|
СО (100 %) |
|
750 |
|
5,0 |
|
ОУНТ |
МgО |
|
1,0 |
: 1,0 : 20 |
|
|
СН4 (9 %) – Ar |
|
800…850 |
|
1,0 |
|
ДУНТ |
Al2O3 |
|
1 : 4 : 50 |
|
|
СН4 (50 %) – Ar |
|
550…850 |
|
1,0 |
|
МУНТ |
|
|
|
|
|
|
|
Fе : Мо |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
МgО |
|
10 : 2,5 : 87,5 |
|
|
СН4 – С2Н4 – Н2 |
|
900 |
|
− |
|
Т-МУНТ |
|
МgО |
|
1,0 : 1,0 : 11 |
|
|
С2Н2 (2 %) – Ar |
|
800…950 |
|
− |
|
ОУНТ |
|
Al2O3 |
|
1,0 : 0,16 : 10 |
|
|
СН4 (50 %) – Н2 |
|
950 |
|
− |
|
ОУНТ |
|
SiO2 + Al2O3 |
|
1,0 : 0,17 : (16 + 16) |
|
СН4 |
|
900 |
|
− |
|
ОУНТ |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
– массовые проценты; – массовое соотношение.

1.4. Состав и условия применения бинарных порошковых катализаторов Ме – Ме′/А (Ме, Ме′ = Fе, Со или Ni, А – носитель) [27]
|
Ме : Ме′, |
|
Условия процесса |
|
|
|
|
Ме – Ме′/А |
|
|
|
|
Способ |
Продукты |
|
моль (Ме : Ме′) |
|
Исходные |
t, °С |
|
активирования |
||
|
|
Р, атм |
|
||||
|
|
|
вещества |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fе – Со / Цеолит |
(0…5) : (5…0) : 95 |
|
С2Н2 (10 %) – N 2 |
700 |
1,0 |
Термический |
Т-МУНТ, |
|
|||||||
|
|
|
|
|
|
|
МУНТ |
Fе – Со / МgAl2O4 |
6,5 : 3,5 : 90 |
|
СН4 (18 %) – Н2 |
700…1070 |
1,0 |
Термический |
Т-МУНТ, |
|
|
|
|
|
|
|
УНВ |
Fе – Со / Al2O3 |
2,5 : 2,5 : 95 |
|
С2Н4 (27 %) – N 2 |
1080 |
1,0 |
Термический |
ОУНТ |
Со – Ni / МgAl2O4 |
80 |
|
СН4 (18 %) – Н2 |
1070 |
1,25 |
Термический |
ОУНТ |
|
|
|
|
|
|
|
|
– массовые проценты; |
|
|
|
|
|
|
|
– отношение Fе : Со;
– содержание МgО около 97 мас. %.
До сих пор четко неясны факторы, определяющие скорость деструкции углеводородов и роста УНТ, что не позволяет получить аналитические выражения кинетических уравнений. Вместе с тем важнейшими факторами роста [27] считаются следующие:
1. Характер и природа реакций, протекающих как на поверхности катализатора, так и в газовой фазе. Однако только этим вряд ли можно объяснить экспериментально наблюдаемый факт влияния длины тонкопленочного катализатора на скорость образования и выход ОУНТ [27]. Так, на катализаторе Мо – F е / Al2O3 с размером пленки 1 × 1 см УНТ из СН4 не образуются. Вместе с тем, увеличение размера до 1 × 15 см приводит к росту "леса" УНТ.
2. Размер частиц катализатора. Поверхность катализаторов энергетически неоднородна, но при этом изотермы адсорбции на них ни исходных углеводородов, ни промежуточных продуктов неизвестны. На их поверхности могут протекать и вторичные процессы – утолщение нанотрубок в результате отложения аморфного углерода, адсорбции полиароматических соединений или графитизированных частиц.
Повышение температуры усиливает рост отложений, но, естественно, ингибирует процессы не только физической, но и химической адсорбции. Некоторые экспериментальные данные, характеризующие скорость роста УНТ, приведены в табл. 1.5. Легко видеть, что среди данных отсутствуют кинетические параметры. Табл. 1.5 включает лишь чисто технологические параметры – нет данных по константам скоростей, кажущейся энергии активации процесса. Исходя из табл. 1.5, даже из самых общих соображений нельзя ответить на вопрос, в каком режиме: кинетическом, диффузионном или смешанном реализуется процесс роста УНТ. Следовательно, не ясно как управлять его кинетикой.
1.5. Скорость линейного роста УНТ как функция условий реализации процесса [27]
|
|
t, °С |
|
Способ |
|
Диаметр |
Скорость |
|
Реагент |
Катализатор |
Р, атм |
Морфология |
наночастиц, |
роста, |
|||
активирования |
||||||||
|
|
|
|
|
нм |
мкм/мин |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
СН4 |
NiОх |
700 |
1,0 |
Плазма |
МУНТ |
50…80 |
0,2 |
|
СН4 + Н2 |
Fe + Ti |
600 |
0,1 |
Плазма |
Т-МУНТ |
~ 5 |
~ 10 |
|
СН4 |
Fe |
70 |
2,6 × 10−2 |
Плазма |
МУНТ |
20 |
5,4…16,8 |
|
С2Н2 |
Fe |
750…950 |
1,0 |
Термический |
МУНТ |
30…130 |
0,5…2,0 |
|
С2Н2 |
Fe |
750 |
1,0 |
Термический |
МУНТ |
10…15 |
20 |
|
С2Н2 |
Fe – Мо |
730 |
1,0 |
Термический |
ОУНТ + МУНТ |
1…20 |
> 17 |
|
С2Н2 |
Ni |
480 |
(2,6 × 13,0) × 10−5 |
Термический |
МУНТ |
- |
2,3 |
|
С2Н2 |
Fe + Мо |
535…600 |
1,0 |
Термический |
Т-МУНТ |
- |
12…30 |
|
С2Н4 |
Ni – Fe |
850…1000 |
3,2 × 10−4 |
Плазма |
МУНТ |
10…50 |
0,25 |
|
С2Н5ОН |
Со – Мо |
800 |
1,3 × 10−2 |
Термический |
ОУНТ |
1,0…2,0 |
0,3 |
|
С2Н5ОН |
Fe |
900 |
1,0 |
Термический |
ОУНТ |
1,3…2,2 |
660 |
|
|
|
|
|
|
|
|
|
Кинетика процессов каталитического пиролиза углеводородов изучена крайне недостаточно. Так, порядок реакции по СН4 меняется от 1,2 до 1,8 [27], средняя величина 1,5. Это нельзя объяснить усилением параллельного некаталитического разложения метана с ростом Р(СН4). Вклад некаталитического разложения метана при этом в общую скорость процесса в том и другом случае должен быть одинаков.
С другой стороны, получены экспериментальные результаты, указывающие, что формальный порядок пиролитического образования УНВ является функцией температуры, возрастая от 1,0 (600 °С) до 1,3 (700 °С). Получены и достаточно странные результаты, указывающие на независимость скорости пиролиза с образованием ОУНТ от Р (СН4), т.е. на нулевой порядок реакции по метану. Это нельзя объяснить контролем процесса объемной или латеральной диффузии, при которых кинетический порядок должен быть равен 1 [164]. Скорее всего лимитирующей становится иная стадия многостадийного процесса, не связанная с участием углеродсодержащих частиц.
Изучение кинетики роста МУНТ при пиролизе С2Н2 показало [27], что порядок реакции по ацетилену равен 1, а энергия активации составила 120…160 кДж/моль, что вновь указывает на кинетический контроль процесса (Т = 873…953 К,
Р(С2Н2) =10 кПа, катализатор – F е).
Вотсутствии его кинетических закономерностей, в принципе, нельзя рассматривать стадийный механизм синтеза УНТ. Для его даже предположительной формулировки необходимо знать порядки реакций по всем реагирующим веществам при постоянной температуре и в условиях постоянства активности катализатора. Необходимы данные по степеням заполнения поверхности катализатора молекулами реагентов или продуктами их деструкции. Только в этом случае можно, в первом приближении, сформулировать состав промежуточного комплекса.
Следует отметить, что необходимо исследовать и особенности латеральной диффузии частиц адсорбата на поверхности катализатора, как функции его природы, температуры системы и парциального (а не общего в системе) давления реагента. Без детального исследования этих процессов пока рано ставить вопрос о реально обоснованном механизме процесса. Тем более, что он сам или, по крайней мере, природа лимитирующей стадии, несомненно, являются функцией природы катализатора. Пока же в литературе [27] говорится о предполагаемом брутто-процессе или, вернее, о некоторых его стадиях, хотя, возможно, и лимитирующих.
Все рассмотренные подходы, их уточнение нуждаются в постановке специальных исследований, подчас весьма дорого-
стоящих. Но без получения соответствующих данных, причем не на одной, а на целом ряде систем: СnH2n + 2 / катализатор, СnH2n / катализатор, СnH2n – 2 / катализатор – нельзя создать научных основ синтеза УНТ каталитическим пиролизом. В таком случае будет отсутствовать прогнозная база и всякая научная работа обречена на использование метода последовательного приближения – метода чрезвычайно дорогостоящего и длительного.
Вкачестве базового метода, реализованного нами впоследствии для получения УНМ в промышленном объеме, использовалась методика, изложенная в [124].
Катализатор получали восстановлением в атмосфере водорода при 873 К прекурсора NiO / MgO, приготовленного соосаждением в кислой среде солей никеля и магния. Приблизительное равенство ионных радиусов Mg2+ и Ni2+ способствует тому, что NiO и MgO обладают хорошей взаимной растворимостью и в бинарной системе NiO / MgO образуют твердый рас-
твор Nix Mg1 – x O. Из-за этого ионы никеля распределены разреженно и равномерно по объему решетки MgO и при взаимодействии прекурсора с водородом только небольшая часть ионов никеля восстанавливается до металлического Ni, причем полному восстановлению всего никеля препятствует также и валентная стабилизация кристаллическим полем MgO. В результате кластеры металлического никеля редко и равномерно распределены на поверхности носителя и имеют малые размеры.
Вочередной раз отмечая важнейшую роль, которую играет катализатор в процессах ГФХО, необходимо также констатировать, что количество активного металла в катализаторной массе может быть фактором регулирования параметров получаемых УНМ и, в частности, их диаметров. Проведенные в РХТУ им. Д.И. Менделеева исследования на Ni/MgO катализаторе при пиролизе CH4 выявили следующий эффект:
Ni / Mg |
2 : 1 |
1 : 3 |
1 : 5 |
1 : 10 |
1 : 20 |
|
|
|
|
|
|
T, °C |
510 |
580 |
620 |
630 |
650 |
DМУНТ, нм |
35 |
– |
21 |
17 |
13 |
|
|
|
|
|
|
Для получения результата экспериментаторы ступенчато повышали также и температуру процесса.
1.4. МЕХАНИЗМ РОСТА УГЛЕРОДНЫХ НАНОСТРУКТУР
Первой и основной стадией процесса роста углеродных наноструктур является гетерогенная реакция пиролиза углеводорода на поверхности металла катализатора. Достаточно подробно механизм данных процессов описан авторами [113, 164], исходя из предположения, что образование УНМ протекает по механизму "карбидного цикла" [165], согласно которому молекула углеводорода, хемосорбируясь на поверхности металлического катализатора, претерпевает последовательный отрыв атомов водорода с последующим проникновением атома углерода через данную поверхность в объем металлической частицы катализатора. При этом образуется карбид металла или твердый раствор углерода в металле. Карбиды металлов могут быть либо промежуточными, либо побочными продуктами процесса роста углеродных волокон. Например, в [166] авторы считают возможным образование карбидов в поверхностном слое частиц металлического катализатора.
Однако образование карбидов металлов не является обязательным процессом, сопровождающим рост углеродных структур на поверхности катализаторов. Например, авторы [122, 167], использовавшие железный катализатор, полагают, что рост нанотрубок протекает через образование раствора углерода в аустените (γ-Fe).
В работе [168], где для получения углеродных волокон использовался в качестве катализатора никель, авторы также не наблюдали образование карбида металла. В работе [169] было показано, что для всех 3d-переходных металлов в процессе роста углеродных волокон образования карбида металла вообще не происходит.
Вторая стадия образования углеродного волокна требует более детального изучения, так как непосредственно затрагивает механизм зарождения и роста углеродных структур на металлических катализаторах. Этому посвящены работы [118, 123, 169 – 175] и обзоры [114, 115,
176].
Авторы, изучавшие рост УНВ на частицах железа [167, 170, 171], сходятся во мнении, что процесс протекает благодаря диффузии углерода от одного участка поверхности каталитической частицы, на котором разлагается углеводород, к другому, на котором происходит высаждение углерода, причем слой металла вблизи поверхности роста УНВ находится в состоянии насыщения углеродом (рис. 1.26).
Диффузия углерода идет от области с высоким химическим потенциалом углерода к области, где он ниже. При этом возможны два случая: либо диффузия идет преимущественно из-за градиента температуры [170, 171], либо концентрации атомов С в растворе [167, 172]. Надо заметить, что авторы работы [167] показали, что при росте УНВ на частицах железа температурный градиент не может достичь заметных значений из-за высокой теплопроводности металла, а в работе [169] показана невозможность температурной диффузии углерода в частице катализатора для случаев, когда рост углеродных волокон происходит при разложении углеводородов на 3d-катализаторах.
В общем принято, что диффузия углерода через объем частицы катализатора является стадией процесса, лимитирующей скорость роста углеродных волокон.
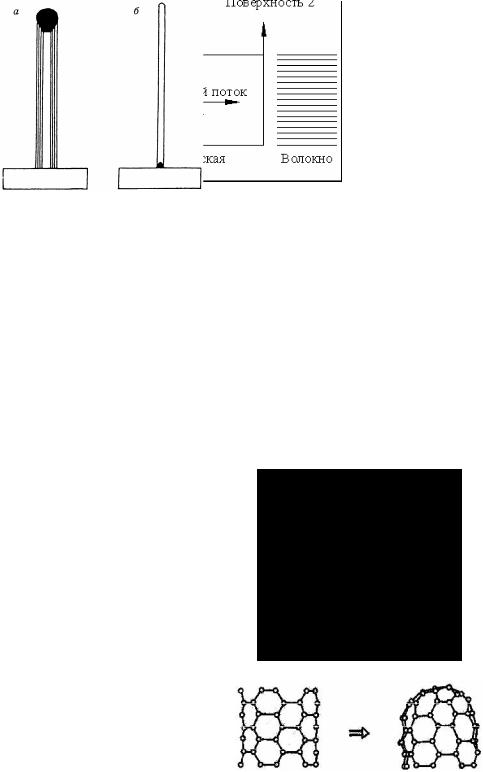
Рис. 1.26. Модель роста углеродных отложений [168]:
на поверхности 1 каталитической частицы происходит адсорбция и разложение углеводорода; на поверхности 2 – рост УНВ
Качественное описание образования УНТ разных типов с единой точки зрения предложено в [177]. В качестве базового механизма авторы рассматривают механизм пар – жидкость – кристалл и применяют его к разным наноуглеродным объектам. В частности, для образования ОУНТ авторы [178] дают чисто кинетическую иллюстрацию: отрыв искривленного монослоя (пентагональной шапочки) происходит, если атом углерода имеет в поверхностном слое достаточную кинетическую энергию для преодоления адгезии и поверхностного натяжения графитового листа. Предложенная схема весьма привлекательна, но не позволяет количественно определить тип возникающей наноструктуры.
Формально механизмы каталитического образования УНТ делят на вершинный и корневой (рис. 1.27).
Образование УНВ на Ni-катализаторах, по мнению некоторых авторов [46], протекает по механизму, который получил название вершинного: частицы катализатора находятся на растущих кончиках УНВ и перемещаются вместе с ними. При этом катализатор может дробиться, что приводит к разветвлению УНТ.
Рост ОУНТ, напротив, идет по корневому механизму, когда частицы катализатора остаются на поверхности подложки или носителя. В этом случае существенный вклад в механизм процесса вносит взаимодействие частиц металла с подложкой. Механизм образования МУНТ, имеющих небольшое число слоев, скорее всего также корневой.
Рост ОУНТ, получаемых в электрической дуге и лазерной абляцией, с узким распределением по диаметрам критически зависит от состава катализатора. Путем классического молекулярно-динамического моделирования, используя реалистичный многочастичный углерод-углеродный потенциал [179], показано, что широкие нанотрубки, которые первона-
Рис. 1.27. Вершинный (а) и корневой (б) механизмы роста углеродных нанотрубок